Оригинальные исследования
ОБОСНОВАНИЕ. Несмотря на значимый прогресс в лечении детей с сахарным диабетом 1 типа (СД1), достижение целевых показателей углеводного обмена у них остается одной из наиболее сложных задач. Становится все более очевидным влияние психосоциального состояния семьи на возможность достижения метаболической компенсации. Однако изучение факторов социального риска (СР) в семьях, имеющих детей с СД1, и их влияния на обмен веществ остается явно недостаточным.
ЦЕЛЬ ИССЛЕДОВАНИЯ. Определение факторов СР, наиболее характерных для семей детей с СД1 в нашей стране и анализ их связи с компенсацией СД1 на основании опроса родителей.
МАТЕРИАЛЫ И МЕТОДЫ. Исследование проводилось в эндокринологических отделениях детских стационаров и отделениях медико-социальной помощи детских поликлиник в 4 регионах: Вологодской, Тюменской, Челябинской областях и в Ханты-Мансийском автономном округе.
Всего в исследовании приняло участие 325 респондентов. 1 группа — стаж СД1 у детей >1 года и плохой метаболический контроль (уровень гликированного гемоглобина ((HbA1c) >7,5%) — 195 чел.; 2 группа — стаж СД1 у детей >1 года и хороший метаболический контроль (HbA1c<7,5%) — 60 чел. Дополнительную группу составили 73 пациента со стажем СД1 у детей <1 года, независимо от метаболического контроля, с целью анализа распространенности факторов социального риска уже на первом году заболевания СД.
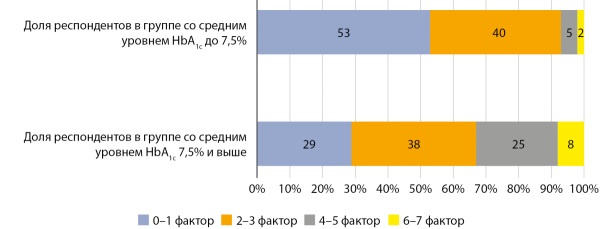
РЕЗУЛЬТАТЫ. В общей группе HbA1c составил 9,1% (4,9–17%). Пятерку самых распространенных факторов СР составили низкий уровень образования родителей (отсутствие высшего и среднего образования), отсутствие постоянной работы, одинокое воспитание ребенка, отсутствие поддержки со стороны близких, доход ниже прожиточного минимума.
1 группа (192 человека). Средний уровень HbA1c — 9,8% (7,5–17%). Среди факторов СР, достоверно влияющих на уровень HbA1c, выявлены уровень образования родителей, одинокое воспитание ребенка, низкий доход в семье и количество детей в семье. Отрицательное влияние на метаболический контроль оказывает и количество воздействующих факторов СР.
2 группа (60 человек). HbA1с — 6,6% (5,3%–7,3%). Распространенность факторов СР оказалась значительно ниже, чем в предыдущей группе. Различия были достоверны для отсутствия высшего образования, одинокого воспитания ребенка и низкого дохода в семье.
3 группа (73 человека). HbA1c — 9,3% (4,9–15,1%), что может быть обусловлено длительностью СД менее 3 мес. у части детей. Через 3 мес. уровень HbA1c составил 7,9% (4,8–13,4%). Перечень факторов СР практически совпадает по составу и частоте с таковым в семьях 1 группы. Таким образом, нерешенные вовремя социальные трудности с течением времени усугубляют положение семьи и негативно влияют на компенсацию углеводного обмена.
ЗАКЛЮЧЕНИЕ. Нами выделены наиболее значимые факторы СР в семьях, имеющих детей с СД1 в РФ. Ухудшение социальных условий в семье — это фактор, негативно влияющий на уровень контроля СД1 и на развитие осложнений в последующем. В итоге семьи, имеющие детей с СД1, особенно с хронической декомпенсацией, нуждаются в оценке факторов СР и сопровождении социальной службы.
ВВЕДЕНИЕ. Скелетные мышцы играют ключевую роль в углеводном метаболизме организма. Дисрегуляция инсулин-зависимого захвата глюкозы в скелетной мускулатуре нарушает обмен углеводов в организме и может приводить к развитию ожирения и сахарного диабета 2 типа (СД2).
ЦЕЛЬ. Выявить экспрессионные маркеры (гены) скелетной мышцы человека, ассоциированные с нарушениями глюкозного метаболизма в базальном состоянии и после приема смешанной пищи, нормированной на массу тела.
МАТЕРИАЛЫ И МЕТОДЫ. В исследовании приняли участие три группы по 8 человек: здоровые добровольцы, пациенты с ожирением без и с СД2. Пробы венозной крови брали утром натощак (09:00) и через 30 мин, 60 мин, 90 мин, 120 мин и 180 мин после приема смешанной пищи, нормированной на массу тела (6 ккал/кг). Биопсические пробы из m. vastus lateralis брали до и через 1 ч после приема пищи для оценки экспрессии генов (РНК-секвенирование) и поиска генов, коррелирующих с маркерами нарушения глюкозного метаболизма в базальном состоянии и после приема пищи.
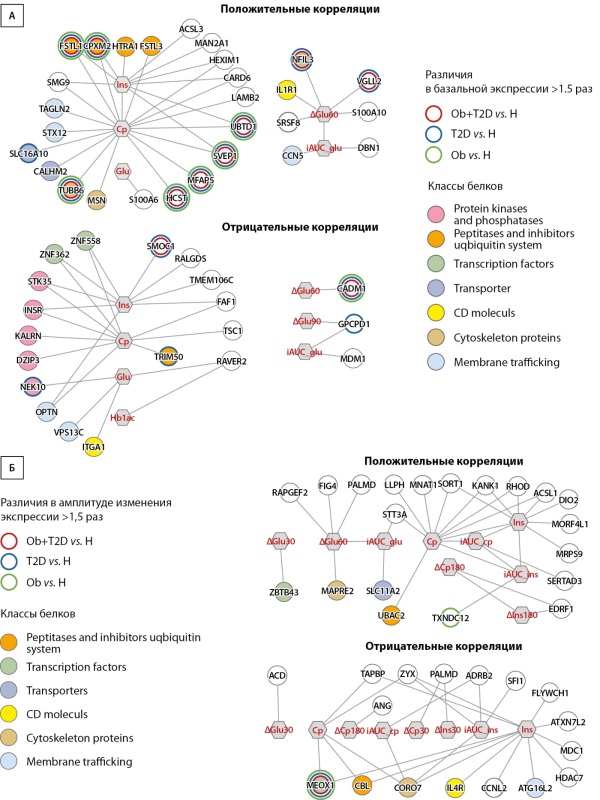
РЕЗУЛЬТАТЫ. Для 75 генов была найдена сильная корреляция (|ρ|>0,7 и р<0,001) между их экспрессией и уровнем инсулина, C-пептида, глюкозы или гликированного гемоглобина в базальном и/или постпрандиальном состоянии. Экспрессия 17 из этих генов имела выраженные отличия (>1,5 раза) между здоровыми людьми и пациентами либо выраженные изменения в ответ на прием пищи. Для них можно отметить такие гены, роль которых в нарушении метаболизма глюкозы уже была показана ранее (FSTL1, SMOC1, GPCPD1), а также другие — которые перспективны для дальнейшего изучения механизмов возникновения инсулиновой резистентности в скелетной мышце.
ЗАКЛЮЧЕНИЕ. Были выявлены экспрессионные маркеры скелетной мышцы, являющиеся перспективными кандидатами для будущих целевых исследований, направленных на изучение механизмов возникновения инсулинорезистентности и поиск потенциальных терапевтических мишеней.
ОБОСНОВАНИЕ. Микроциркуляторная дисфункция у пациентов с сахарным диабетом (СД) приводит к возникновению недостаточной трофики тканей, снижению резервов адаптации и развитию осложнений. Осуществить прижизненную оценку структурно-функциональных изменений системы микроциркуляции возможно методом лазерной допплеровской флоуметрии. Амплитуды его спектральных колебаний позволяют расшифровать локальные и системные механизмы модуляции микроциркуляции. Наличие микроциркуляторных нарушений установлено в веках при хронических блефаритах и дисфункции мейбомиевых желез. У доминирующего числа пациентов с СД выявляют наличие либо изолированного поражения мейбомиевых желез, либо сочетания с блефаритом. В статье представлены результаты исследования, касающиеся особенностей неоангиогенеза как механизма развития хронического блефарита и дисфункции мейбомиевых желез при СД.
ЦЕЛЬ. Выявить особенности микроциркуляторных нарушений век при хроническом смешанном блефарите у пациентов с СД 2 типа (СД2).
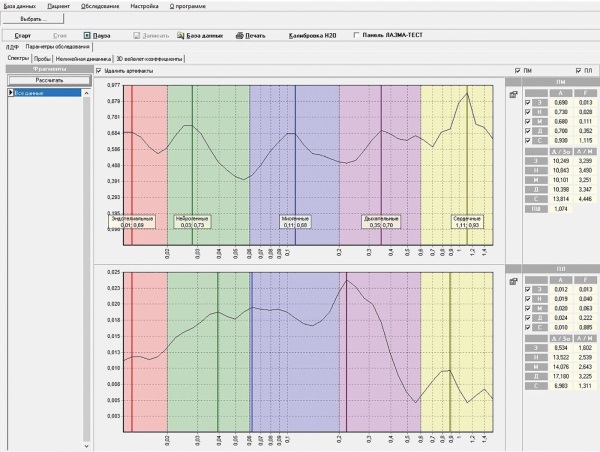
МАТЕРИАЛЫ И МЕТОДЫ. Исследование проведено у 57 пациентов: 37 человек с хроническим смешанным двусторонним блефаритом и верифицированным диагнозом СД2 (группа 1, n=74 глаза, средний возраст 69,5±7,5 года; подгруппа 1а, n=38 глаз — больные с СД2 и средним уровнем гликированного гемоглобина (HbA1с 6,7±1,2); подгруппа 1б, n=36 глаз — больные с СД2 и средним уровнем HbA1с 8,2±1,3) и 20 пациентов с хроническим смешанным двусторонним блефаритом без СД (группа 2, n = 40 глаз, средний возраст 67,2±4,3 года). Лазерную допплеровскую флоуметрию проводили на приборе «ЛАЗМА МЦ-1».
РЕЗУЛЬТАТЫ. У пациентов с хроническим блефаритом на фоне СД2 обнаружено развитие ишемии ткани век с возрастанием напряженности функционирования регуляторных систем микроциркуляции кровотока и лимфотока, а у лиц без СД — венозный застой с умеренным угнетением вазомоторных, дыхательных и доминированием сердечных осцилляций кровотока, а также недостаточностью нейрогенных осцилляций лимфотока. При этом в подгруппе пациентов 1а выявлено доминирование нейрогенных осцилляций кровотока, в подгруппе пациентов 1б — миогенных. Микроциркуляторные изменения лимфотока в подгруппе пациентов 1б были более выраженными в сравнении с результатами, полученными у пациентов подгруппы 1а.
ЗАКЛЮЧЕНИЕ. Анализ результатов доказывает отрицательное влияние СД2 на микроциркуляторное русло пациентов с хроническим смешанным блефаритом. Нарушения, выявленные с помощью лазерной допплеровской флоуметрии, варьируют в зависимости от уровня HbA1с.
ОБОСНОВАНИЕ. Диабетический дистресс (ДД) относится к негативным эмоциональным или аффективным переживаниям, возникающим в результате жизни в условиях диабета. ДД — одно из самых распространенных психических нарушений наряду с депрессией. Депрессия и диабетический дистресс увеличивают риск смерти при сахарном диабете (СД), способствуют развитию осложнений, связанных с диабетом, снижают качество жизни и увеличивают общие медицинские затраты здравоохранения, являются отрицательным предиктором контроля уровня глюкозы в крови и качества жизни и могут приводить к снижению приверженности к лечению. Выявление данных состояний среди пациентов с сахарным диабетом 1 и 2 типов (СД1) и (СД2) может способствовать их своевременной коррекции. Для диагностики ДД применяются специализированные опросники для скрининга эмоционального состояния и психосоциальных аспектов.
ЦЕЛЬ. Провести языковую и культурную адаптацию опросника «Шкала дистресса при диабете» (The Diabetes Distress Scale) и оценить психометрические свойства русскоязычной версии опросника DDS на русскоязычной выборке пациентов с СД1 и СД2.
МАТЕРИАЛЫ И МЕТОДЫ. Проведено исследование на выборке из 198 пациентов с СД1 и СД2, собраны данные по применению русскоязычной версии шкалы DDS, а также шкал EQ-5D-5L (Европейского опросника оценки качества жизни), SPANE (Шкалы позитивных и негативных переживаний) и HADS (Госпитальной шкалы тревоги и депрессии). Последние три шкалы использовались для оценки конвергентной валидности адаптируемого опросника. Надежность опросника DDS оценивалась с помощью коэффициента внутренней согласованности Кронбаха и повторного тестирования участников спустя 1–4 месяца.
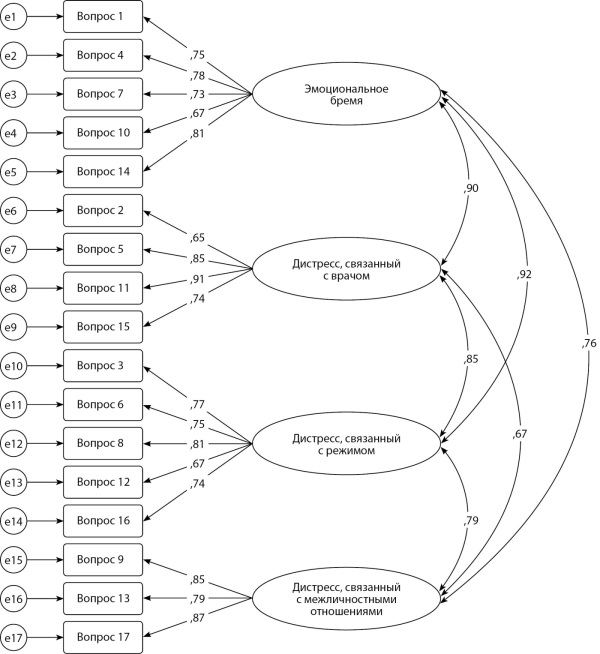
РЕЗУЛЬТАТЫ. Факторная структура опросника DDS полностью воспроизводится при включении всех 17 вопросов (показатели пригодности измерительной модели: CFI=0,981, RMSEA=0,055, TLI=0,967). Внутренняя согласованность субшкал (α ϵ [0,836; 0,874]) и опросника в целом (α=0,948) оценивается как высокая. Получены значимые корреляции адаптируемой методики и ее субшкал со шкалами опросников EQ-5D-5L, SPANE, HADS, наиболее тесные связи (Rho ϵ [0,370; 0,437], p<0,01), что говорит о хорошей внешней валидности адаптируемой методики.
ЗАКЛЮЧЕНИЕ. Русскоязычная версия анкеты DDS обладает хорошими психометрическими свойствами, является валидным и надежным инструментом для оценки дистресса среди пациентов с СД1 и СД2 и может быть рекомендована к применению в клинической практике для дифференциальной диагностики депрессии и ДД.
ОБОСНОВАНИЕ. С момента появления коронавирусной инфекции в клинической практике особое внимание уделялось ее острой фазе. Однако на сегодняшний день остается открытым вопрос прямого и косвенного воздействия на пациентов с сахарным диабетом 2 типа (СД2) после выздоровления от коронавирусной инфекции.
ЦЕЛЬ. Определить клинико-лабораторные особенности постковидного периода у больных СД2 в разные периоды инфекции.
МАТЕРИАЛЫ И МЕТОДЫ. Проведено описательное ретроспективное исследование с использованием электронных медицинских карт 134 пациентов, перенесших коронавирусную инфекцию.
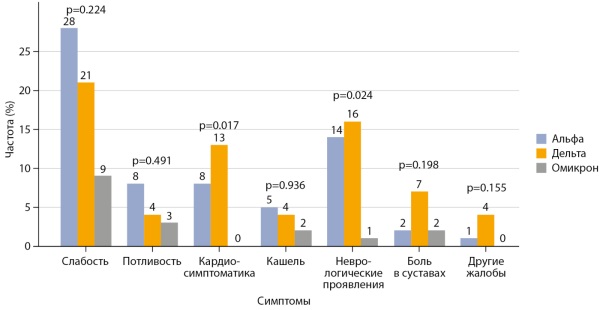
РЕЗУЛЬТАТЫ. Большую часть пациентов составили женщины, распределение по возрасту и по полу в группах не различалось (р=0,384 и p=0,207). В периоде «Омикрон» наблюдалось меньшее количество сопутствующих заболеваний и меньшее количество госпитализированных пациентов по сравнению с другими группами (р<0,0167). При изучении состояний, связанных с сахарным диабетом, частое мочеиспускание присутствовало только у пациентов периода «Альфа», а частота гипогликемии, гипергликемии, степень хронической болезни почек (ХБП) и проявлений полинейропатии не различались между группами (р>0,0167). При изучении впервые выявленных заболеваний разница оказалась статистически значимой только в отношении заболеваний опорно-двигательного аппарата (16,7% «Альфа» против 30,2% «Дельта» против 3,7% «Омикрон», р=0,015). При изучении лабораторных показателей была обнаружена разница в отношении тромбоцитов и АЧТВ: медианы тромбоцитов были статистически значимо ниже в группах «Альфа» и «Дельта» по сравнению с группой «Омикрон» (210 (179,2–249,7) 10⁹/л и 218 (196,5–281) 10⁹/л против 255 (208–327) 10⁹/л соответственно, p=0,016); АЧТВ был статистически значимо более продолжительным для «Альфа» и «Дельта» по сравнению с «Омикрон» 28 (23,6–31,3) сек против 30,3 (26,1–34,9) сек против 27,1 (22,4–30,3) сек соответственно (p=0,013).
ЗАКЛЮЧЕНИЕ. Данные реальной клинической практики позволяют проследить за развитием новой симптоматики и новых заболеваний пациента в постковидном периоде. Пациенты с СД во временной вариант-ассоциированный период «Омикрон» имели меньший риск развития новых симптомов и заболеваний. Необходимо внедрять решения для контроля целевых показателей HbA1c через медицинские информационные системы и повышать стандарты качества репортирования симптоматики пациентов для более точного анализа данных реальной клинической практики (Real world data, RWD).
ОБОСНОВАНИЕ. Бариатрическая хирургия доказала свою эффективность в качестве метода лечения метаболических осложнений ожирения, в том числе сахарного диабета 2 типа (СД2). В настоящее время данный метод лечения является наиболее эффективным способом достижения стойкой ремиссии СД2. Принимая во внимание прогрессирующий рост выполняемых бариатрических вмешательств и выраженную гетерогенность группы пациентов, претендующих на оперативное лечение ожирения, важным этапом развития данного направления является разработка персонализированного подхода.
ЦЕЛЬ. Разработка шкалы предоперационного прогнозирования ремиссии СД2 у пациентов российской популяции с ожирением, перенесших бариатрическое вмешательство (продольная резекция желудка или гастрошунтирование).
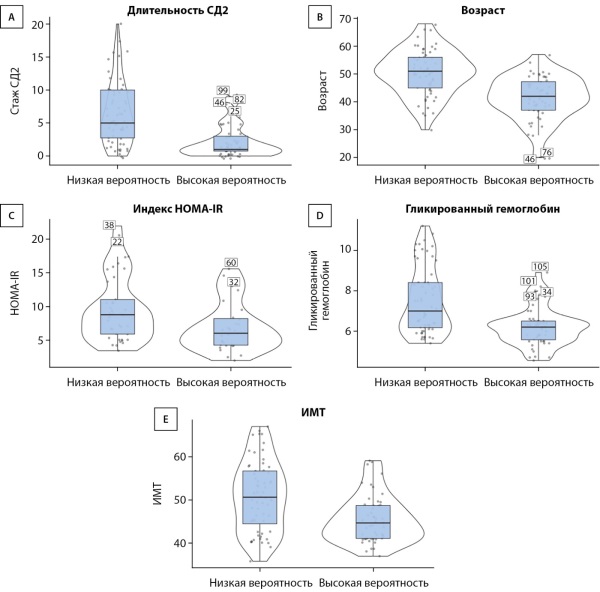
МАТЕРИАЛЫ И МЕТОДЫ. Проведено ретроспективное многоцентровое когортное исследование, по итогу в исследование было включено 112 пациентов, среди них — 75 женщин и 37 мужчин, средний возраст — 46,25±9,29 года, средний индекс массы тела (ИМТ) — 48,71±7,66 кг/м2. В дальнейшем проведен математический анализ 17 дооперационных клинических критериев для поиска независимых предикторов ремиссии СД2: возраст, ИМТ, длительность СД2, количество сахароснижающих препаратов, терапия метформином, терапия препаратами сульфонилмочевины (ПСМ), инсулинотерапия, предоперационный уровень гликированного гемоглобина (HbA1с), С-пептид, индекс инсулинорезистентности HOMA-IR, повышение уровня печеночных трансаминаз, гиперурикемия, уровень общего холестерина (ХС), триглицеридов (ТГ), липопротеинов высокой плотности (ЛПВП), уровень витамина 25(ОН)D.
РЕЗУЛЬТАТЫ. В результате из 112 пациентов ремиссия СД2 регистрировалась у 85 человек (75,9%), отсутствие ремиссии СД2 наблюдалось у 27 пациентов (24,1%). По итогам многоэтапного математического анализа выяснено, что наиболее важными прогностическими факторами стали: стаж СД2, возраст, индекс инсулинорезистентности HOMA-IR, HbA1с, ИМТ, терапия метформином, ПСМ, инсулинотерапия, повышение уровня печеночных трансаминаз, уровень общего ХС. По результатам проведенного статистического анализа был вычислен относительный коэффициент важности каждого из параметров, в результате чего была разработана формула, позволяющая прогнозировать высокую или низкую вероятность ремиссии СД2 после бариатрического лечения. Для удобства применения в клинической практике на основании разработанной формулы был предложен онлайн-калькулятор DRAMS (Diabetes Remission After Metabolic Surgery).
ЗАКЛЮЧЕНИЕ. По результатам проведенного исследования удалось разработать онлайн-калькулятор для прогнозирования вероятности ремиссии СД2 после бариатрического вмешательства. Накопленный в настоящий момент набор характеристик дает возможность для построения качественной шкалы «высокий риск»/«низкий риск». Ряд выявленных в рамках настоящего исследования предикторов требует дальнейшего исследования на больших выборках пациентов.
ОБОСНОВАНИЕ. Внедрение в клиническую практику современных технологий: помповая инсулинотерапия (НПИИ) и непрерывный мониторинг глюкозы (НМГ) значительно облегчил жизнь людей с сахарным диабетом 1 типа (СД1). Однако сопровождается ли это достижением лучшей компенсации у детей и подростков — этот вопрос пока не получил утвердительного ответа.
ЦЕЛЬ. Проанализировать взаимосвязь гликемического контроля с использованием НПИИ и НМГ у детей.
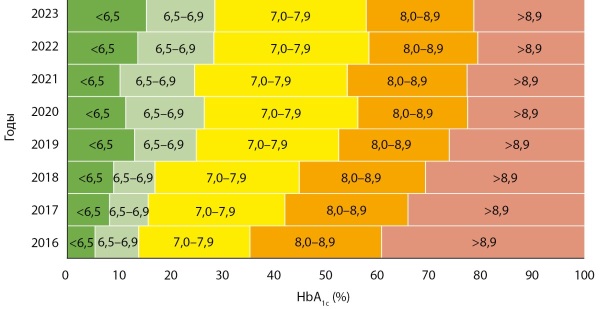
МАТЕРИАЛЫ И МЕТОДЫ. В исследование включены 6382 ребенка с СД1 в возрасте от 1 года до 18 лет, наблюдавшиеся в течение 8 лет (2016–2023 гг). Оценивали частоту использования НПИИ и НМГ и исследовали уровень гликированного гемоглобина (HbA1c) и % детей, имеющих HbA1с<7,0%.
РЕЗУЛЬТАТЫ. Уровень HbA1c снижался с 8,6% в 2016 г. до 7,7% в 2023 г. (р<0,001). Параллельно увеличивался % детей, достигших HbA1c<7,0% c 11 до 29%. За этот период использование НМГ выросло с 11,6 до 84%, НПИИ — с 38,7 до 42,3% (р<0,001).
ЗАКЛЮЧЕНИЕ. Внедрение в клиническую практику НПИИ и НМГ значимо сопровождается улучшением компенсации СД1 у детей как по уровню HbA1c, так и увеличению процента детей, достигающих целевых значений HbA1c<7,0%.
ЦЕЛЬ. Оценить влияние добавления фиксированной комбинации инсулина гларгин (100 Ед/мл) и ликсисенатида (иГларЛикси) пациентам российской популяции с сахарным диабетом 2 типа (СД2) и неудовлетворительным гликемическим контролем на терапии пероральными сахароснижающими препаратами (ПССП) ± инсулин.
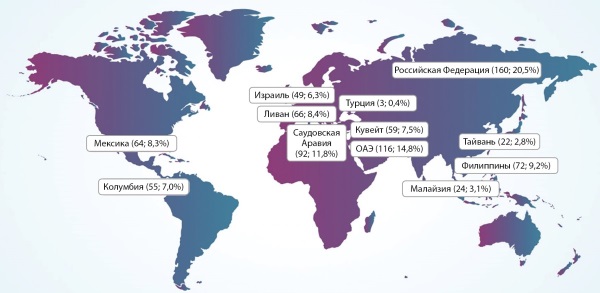
МАТЕРИАЛЫ И МЕТОДЫ. В Российский субанализ международного многоцентрового проспективного наблюдательного исследования SUCCESS было включено 160 пациентов с СД2 из 11 регионов Российской Федерации, начавших терапию иГларЛикси в течение 1 мес до включения, вне связи с исследованием. Первичная конечная точка: изменение уровня гликированного гемоглобина (HbA1c) от исходного уровня через 6 мес. Вторичные конечные точки: изменение HbA1c через 12 мес; достижение индивидуального целевого HbA1c через 6 и 12 мес; изменение ГПН, ППГ и массы тела через 6 и 12 мес; динамика дозы иГларЛикси. Конечные точки безопасности: оценка частоты всех нежелательных явлений (НЯ), серьезных НЯ и НЯ, представляющих особый интерес, частота гипогликемий за период исследования.
РЕЗУЛЬТАТЫ. Средний возраст пациентов в российской популяции составил 60,8±9,4 года; длительность СД2 — 11,4 года, HbA1c — 9,3±1,5%, ИМТ — 33,3 кг/м2. До включения в исследование большинство пациентов находились на терапии 2 ПССП (36,3%) и 3 ПССП (27,5%), на терапии инсулином — 32,5%. Среднее снижение HbA1c через 6 мес составило -1,81%, через 12 мес -2,03%. Через 12 мес 51,3% пациентов достигли индивидуальных целевых значений HbA1c и 46,7% пациентов достигли 3-компонентной цели по HbA1c с отсутствием подтвержденных или тяжелых гипогликемий и набора массы тела. Снижение массы тела через 12 мес составило -3,3±4,4 кг. За период исследования было зарегистрировано 17 случаев гипогликемии (0,106 событий на пациенто-год); 1 эпизод тяжелой гипогликемии (0,006 событий на пациенто-год). Общее число НЯ — 43 (26,9%), серьезных НЯ — 10 (6,3%).
ЗАКЛЮЧЕНИЕ. Российский субанализ наблюдательного исследования показал, что в реальной клинической практике включение в схему терапии иГларЛикси у пациентов с СД2, не достигающих цели на ПССП±инсулин, значимо улучшает показатели гликемического контроля с низким риском гипогликемий и без увеличения массы тела.
ОБОСНОВАНИЕ. Основной причиной слепоты у пациентов с сахарным диабетом (СД) является диабетическая ретинопатия (ДР) — наиболее распространенное микрососудистое осложнение СД — и нарушение зрения. Висфатин — это адипоцитокин, который способствует активности инсулина при гестационном диабете и беременности.
ЦЕЛЬ. Целью данного исследования было оценить уровни висфатина в сыворотке крови у пациентов с СД 2 типа (СД2), пролиферативной ДР, непролиферативной ДР и у здоровых лиц.
МАТЕРИАЛЫ И МЕТОДЫ. В исследовании приняли участие 120 пациентов с историей СД2 более 5 лет и 30 здоровых участников. Группа пациентов была разделена на три подгруппы: СД2, с пролиферативной и с непролиферативной ДР. Уровни висфатина измерялись с использованием коммерчески доступного набора для иммуноферментного анализа. Были оценены уровни триглицеридов (ТГ), общего холестерина (ОХ), холестерина липопротеинов низкой плотности (ЛПНП), холестерина липопротеинов высокой плотности (ЛПВП) и гликированного гемоглобина (HbA1c).
РЕЗУЛЬТАТЫ. У пациентов с пролиферативной ДР и пациентов с плохим гликемическим контролем наблюдалось значительное повышение уровней висфатина по сравнению с группой здоровых контролей и пациентами с СД2 без ДР. Уровни ОХ, ТГ и ЛПНП в группе ДР были заметно выше и значительно превышали показатели в группе здоровых контролей.
ЗАКЛЮЧЕНИЕ. Уровни висфатина связаны как с тяжестью, так и с наличием ДР, и более высоки у пациентов с плохим гликемическим контролем. Повышенный уровень липидов ассоциирован с риском ДР.
Обзоры
Ретинопатия недоношенных (РН) является сложной и нерешенной проблемой детской офтальмологии, приводящей к инвалидности по зрению. Низкий вес при рождении и недоношенность являются основными факторами риска, и они легли в основу клинических рекомендаций по скринингу на РН у всех детей с гестационным возрастом до 35 недель и массой тела менее 2000 г. Однако многие исследователи указывают и на другие факторы риска, которые можно разделить на материнские, пренатальные и перинатальные. В данном обзоре мы рассматриваем сахарный диабет (СД) матери как фактор риска РН. Изменения в сетчатой оболочке у недоношенных детей и матерей с СД имеют некоторые общие черты, поскольку в основе этих заболеваний имеет место патологический ангиогенез. Кроме того, диабет является фактором риска преждевременных родов, а недоношенность — ведущей причиной неонатальной заболеваемости, включая развитие РН. Это позволяет предположить, что СД матери может оказывать как прямое, так и косвенное влияние на развитие РН. Для разработки прогностических моделей необходимо понимание факторов риска РН, патофизиологии сосудистых заболеваний сетчатки и болезней недоношенных.
Сахарный диабет (СД) — это хроническое метаболическое расстройство, которое часто приводит к угрожающим жизни заболеваниям и постоянно снижает ожидаемую продолжительность жизни. Он характеризуется гипергликемией, возникающей в результате нарушения секреции инсулина, его действия или того и другого. На протяжении тысячелетий наши предки использовали лекарственные растения для профилактики, лечения или даже излечения СД. В последние два-три десятилетия использование этих травяных растений стремительно возросло благодаря их меньшей токсичности и экономической эффективности по сравнению с синтетическими препаратами. В этом обзоре описано около 30 лекарственных растений, которые являются родными для Индии и традиционно используются жителями Шиваликского хребта Гималаев в Уттаракханде (особенно в Дехрадуне и Харидваре) для лечения СД. Данные о этих растениях были собраны из Science Direct, PubMed, Web of Science, Scopus, MDPI, Google Scholar и других поисковых систем и веб-сайтов. Обзор представлен в систематизированном виде, включая ботаническое название, семью, народные названия, используемые части и фармакологическое применение растений в табличной форме. Имеются различные научные доказательства применения некоторых лекарственных растений, которые также упоминаются вместе с кратким описанием каждого из них. Все растения и травы, рассмотренные в этом обзоре, легко доступны в этих районах Уттаракханда, и местные жители традиционно используют их как овощи, приправы и ароматизаторы, обычно включая в свой рацион. Существуют некоторые ограничения фитотерапии, которые не позволяют ей полностью заменить аллопатическую терапию, такие как низкая биодоступность, медленная скорость абсорбции и медленная скорость растворения. Однако с использованием различных современных лекарственных форм (фитосомы, неосомы, липосомы, наночастицы, нанопузырьки, наноалмазы, наношары и т. д.) и методов доставки (различные инвазивные и неинвазивные методы), можно обойти все проблемы, связанные с потенцией и эффективностью фитохимических веществ.
Клинический случай
Сахарный диабет 1 типа (СД1) продолжает оставаться одной из глобальных медико-социальных проблем ввиду своей широкой распространенности, полиморфизма, развития тяжелых осложнений и необратимости изменений. Несмотря на существующие четкие алгоритмы и схемы выбора инсулинотерапии, сложную задачу представляет преодоление инсулинорезистентности (ИР) ввиду невозможности применения препаратов из группы бигуанидов и глитазонов, так как их использование при СД1 не предусмотрено инструкцией. В представленном наблюдении показана клиническая картина ИР на фоне метаболического синдрома и длительно существующей гипергликемии у пациентки с СД1 и акцентировано внимание на важности назначения адекватной инсулинотерапии и индивидуального подхода к ведению больной. Основной стратегией в данном случае является постепенное увеличение доз инсулина до тех пор, пока не будут достигнуты целевые показатели гликемии. При этом после достижения адекватных доз и нахождения пациента в пределах околоцелевых значений в течение некоторого периода времени возможно закономерное снижение потребности в инсулине на фоне нейтрализации действия глюкозотоксичности на периферические ткани.
Артифициальная гипогликемия (синдром Мюнхгаузена, искусственная гипогликемия) — это состояние, вызванное низким показателем глюкозы крови вследствие преднамеренного введения инсулина или приема пероральных гипогликемических препаратов. Искусственная гипогликемия остается одной из проблем, с которыми сталкиваются эндокринологи в своей практике, диагностический поиск ее этиологического фактора может приводить к дорогостоящим и ненужным исследованиям. Диагностика искусственной гипогликемии у пациентов с сахарным диабетом (СД) на инсулинотерапии представляется трудоемкой задачей, так как в отличие от большинства симулятивных расстройств, на которые могут указывать нетипичные проявления заболевания или противоречивые медицинские сведения о пациенте, у больных СД гипогликемический синдром является ожидаемым нежелательным явлением вследствие терапии инсулином. Поэтому преднамеренное введение инсулина часто не диагностируется до тех пор, пока самоиндуцированные гипогликемии не становятся рецидивирующими и/или тяжелыми. При подозрении на искусственную гипогликемию вследствие введения аналогов инсулина в настоящее время ряд авторов рекомендуют исследование С-пептида и сочетание двух методов количественного определения инсулина в крови с использованием систем анализаторов с разной чувствительностью к гормону, а также качественную детекцию препарата с помощью высокоэффективной жидкостной хроматографии с тандемной масс-спектрометрией. Активное сотрудничество специалистов клинической и лабораторной служб является залогом успешного решения такой диагностической задачи.
В данной статье представлен клинический случай синдрома Мюнхгаузена у пациентки 28 лет с сахарным диабетом 1 типа в течение 21 года с рецидивирующими гипогликемиями, многократными тяжелыми гипогликемиями, в том числе с потерей сознания, и доказанным во время пребывания в стационаре преднамеренным введением препарата аналога инсулина; описан сложный диагностический путь, пройденный до постановки верного диагноза.

Контент доступен под лицензией Creative Commons Attribution-NonCommercial-NoDerivatives 4.0 International License (CC BY-NC-ND 4.0).
ISSN 2072-0378 (Online)