Оригинальные исследования
ОБОСНОВАНИЕ. Гипогликемия и страх перед гипогликемией остаются критическими проблемами в лечении подростков с сахарным диабетом 1 типа (СД1) и являются факторами, ограничивающими надлежащий контроль гликемии, а также препятствующими достижению метаболической компенсации заболевания. Применение помповой инсулинотерапии предполагает профилактику гипогликемических состояний.
ЦЕЛЬ. Провести анализ распространенности, частоты и продолжительности эпизодов гипогликемии, а также оценить влияние данных показателей на метаболическую компенсацию СД1 у подростков в реальной клинической практике в зависимости от способа введения инсулина.
МАТЕРИАЛЫ И МЕТОДЫ. В исследовании приняли участие 117 подростков с СД1 в возрасте от 12 до 19 лет (средний возраст 15,5 лет). Методом непрерывной подкожной инфузии инсулина (НПИИ) получали терапию 37 подростков; 80 подростков получали терапию методом множественных инъекций инсулина (МИИ). У всех подростков проводилось определение уровня гликированного гемоглобина (HbA1c), а также с помощью 6-суточного непрерывного мониторирования глюкозы (НМГ) «слепым» методом профессиональной системой с датчиком iPro2 (Medtronic MiniMed) проведена оценка его основных показателей.
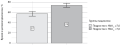
РЕЗУЛЬТАТЫ. Эпизоды снижения уровня глюкозы <3,9 ммоль/л зарегистрированы у 87% пациентов (n=102), у 63% (n=74) выявлено снижение уровня глюкозы <3,0 ммоль/л. Эпизоды снижения уровня глюкозы <3,9 ммоль/л в ночные часы зарегистрированы у 68% пациентов (n=80), а с уровнем глюкозы <3,0 ммоль/л — у 46% (n=54). Частота эпизодов снижения уровня глюкозы <3,9 ммоль/л за период проведения НМГ не имела статистически значимых различий в зависимости от метода введения инсулина (НПИИ или МИИ), однако чаще они встречались у подростков с HbA1c <7,0% (p=0,03). Время в диапазоне <3,9 ммоль/л составило 5% в сутки, более продолжительное время нахождения в данном диапазоне отмечалось у пациентов с HbA1c <7,0% (p=0,006). Время в диапазоне <3,0 ммоль/л составило 1% в сутки и не имело значимых различий в зависимости от уровня HbA 1с (p=0,559). Также не выявлено значимых отличий времени в диапазонах <3,9 ммоль/л и <3,0 ммоль/л в группах, использующих НПИИ и МИИ (p=0,640 и p=0,250).
ЗАКЛЮЧЕНИЕ. Эпизоды снижения глюкозы в диапазоне <3,9 ммоль/л по данным НМГ встречаются чаще у подростков с целевыми значениями HbA1c вне зависимости от способа введения инсулина. Значимо больше времени в диапазоне <3,9 ммоль/л проводят подростки с целевыми значениями HbA1с, т.е. <7,0%, по сравнению с подростками с HbA1c ≥7,0%, однако в обеих группах у большого количества пациентов время в диапазоне ниже целевого уровня было выше рекомендуемых значений.
ОБОСНОВАНИЕ. У пациентов с терминальной стадией хронической болезни почек (тХБП), получающих заместительную почечную терапию программным гемодиализом (ЗПТ ПГД), тяжесть осложнений связана с метаболическими нарушениями: накоплением уремических токсинов, нефрогенной анемией, вторичным гиперпаратиреозом, внекостной кальцификацией, нарушением клиренса и ритма секреции гормонов.
ЦЕЛЬ. Оценить основные биохимические и гормональные показатели, а также структуру минеральных и костных нарушений у пациентов, получающих ЗПТ ПГД, до и после гемодиализа (ГД) с учетом наличия или отсутствия сахарного диабета (СД).
МАТЕРИАЛЫ И МЕТОДЫ. В исследование вошли 40 пациентов с тХБП, находящихся на ЗПТ ПГД: 1-я группа — 24 пациента с СД 1 типа (СД1); 2-я — 16 пациентов без СД. Статистический анализ проведен в программных пакетах Statistica v.13 (StatSoft, США) и SPSS (IBM, США). Критический уровень статистической значимости при проверке гипотез принят равным 0,05.
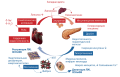
РЕЗУЛЬТАТЫ. Уровень интактного паратгормона (иПТГ) до и после ГД был ниже в группе 1 (р<0,001). Уровень щелочной фосфатазы был значимо выше в группе 2 (р=0,012). В обеих группах до ГД была выявлена высокая частота гипокальциемии (по альбумин-скорректированному кальцию в 1-й группе — в 58,3%, во 2-й группе — в 43,7% случаев, р=0,366) и гиперфосфатемии (в 66,7 и в 43,7% случаев соответственно, р=0,151). Гипокальциемия после ГД в 1-й группе сохранялась в 14%, во 2-й группе — в 20% случаев (р>0,05); гиперфосфатемия в 1-й группе полностью нивелировалась, во 2-й группе сохранялась в 7% случаев (р=0,417). До сеанса ГД в группе 1 были значимо выше уровни эндогенного рецептора к конечному продукту гликирования (RAGE) , глюкагона, иммунореактивного инсулина (ИРИ), кортизола и глюкозы, чем после сеанса ГД (р<0,05). Во 2-й группе после ГД значимо снизились уровни глюкагона, ИРИ и кортизола (р<0,05), а уровень 3-нитротирозина значимо увеличился (р=0,026). В 1-й группе фиброкальциноз клапанов сердца по данным Эхо-КГ и кальцификация артерий нижних конечностей по данным ультразвуковой допплерографии встречались чаще, чем во 2-й группе (42% vs 25%, p<0,001 и 75% vs 37,5%, р=0,018 соответственно (χ2)). Компрессионные переломы встречались с одинаковой частотой в обеих группах (60%). Снижение минеральной плотности костной ткани до уровня остеопении отмечалось чаще в группе 1 (50% vs 18,8%), а остеопороз встречался чаще в группе 2 (68,8% vs 33,3%) (p<0,001, χ2).
ЗАКЛЮЧЕНИЕ. Пациенты с СД1 имели повышенный риск почечной остеодистрофии с низким обменом костной ткани из-за ряда метаболических факторов, присущих СД. Низкий уровень ПТГ в группе 1 может отражать влияние СД на фосфорно-кальциевый обмен. В то же время динамика показателей фосфора и кальция во время процедуры ГД была аналогичной.
ОБОСНОВАНИЕ. Немедикаментозное лечение — неотъемлемая часть терапии всех пациентов с сахарным диабетом 2 типа (СД2). Ввиду многих факторов, несмотря на высокий уровень доказательности эффективности данного вида лечения диабета, пациенты и врачи склонны недооценивать или пренебрегать такими эффективными методами управления течением болезни. Поэтому продолжается разработка новых эффективных программ нефармакологического лечения, адаптированных под особенности конкретной системы здравоохранения.
ЦЕЛЬ. Изучить влияние 24-недельной структурированной программы нефармакологического лечения на снижение уровня гликированного гемоглобина (HbA1c) и массы тела у пациентов среднего возраста с компенсированным СД2, принимающих метформин.
МАТЕРИАЛЫ И МЕТОДЫ. Было разработано двухгрупповое рандомизированное контролируемое исследование в параллельных группах со слепой оценкой результатов. Пациенты с установленным диагнозом СД2 в стадии компенсации (HbA1c ≤7%) в возрасте 45–59 лет, принимавшие метформин, были рандомизированы для получения либо стандартного нефармакологического лечения СД2, предусмотренного клиническим протоколом Казахстана (контрольная группа), либо курс нефармакологического лечения по разработанной авторами структурированной программе, основными принципами которой явились диетотерапия, физическая реабилитация, обучение самоконтролю заболевания под руководством эндокринолога, диетолога и врача лечебной физкультуры (группа вмешательства). Продолжительность вмешательства составила 24 нед. Первичными исходами были уровень HbA1c, масса тела. Вторичные исходы: артериальное давление, окружность талии, индекс инсулинорезистентности (HOMA-IR), липидный профиль: общий холестерин, липопротеиды высокой и низкой плотности, триглицериды. Показатели исхода участников обеих групп оценивались на первоначальном уровне, через 12 и 24 нед после рандомизации. Исследование зарегистрировано на ClinicalTrials.gov NCT04632823.
РЕЗУЛЬТАТЫ. В исследование были включены 200 пациентов, в соответствии с протоколом завершили исследование 67 человек: группа вмешательства — 33, контрольная группа — 34. Через 24 нед наблюдения пациенты в группе вмешательства показали значимое снижение HbA1c с 6,34 до 6,22%, p<0,001, в группе контроля уровень HbA1c значимо не изменился: с 6,54 до 6,53% (p=0,703). За период наблюдения пациенты обеих групп значимо снизили массу тела, однако в группе вмешательства снижение произошло в большей степени значимо: медиана массы тела снизилась на 5,53% от исходного уровня, тогда как в контрольной — всего на 0,1%. Также в группе вмешательства значимо улучшились некоторые сердечно-сосудистые и метаболические показатели: систолическое и диастолическое артериальное давление, глюкоза, холестерин, HOMA-IR. Пациенты обеих групп показали значимое снижение окружности талии и инсулина. За период наблюдения в обеих группах уровни триглицеридов и липопротеинов низкой плотности значимо не изменились.
ЗАКЛЮЧЕНИЕ. Применение структурированной программы нефармакологического лечения СД2 среди компенсированных пациентов среднего возраста, принимавших метформин, на протяжении 24 нед значительно снизило уровень HbA1c и массу тела.
Обзоры
Инсулинорезистентность, являющаяся фундаментальным патогенетическим фактором предиабета, тесно связана с абдоминальным ожирением, с одной стороны, и развитием сердечно-сосудистых заболеваний, хронической сердечной недостаточности (ХСН), — с другой. Патогенетическая роль инсулинорезистентности многогранна и заключается в акселерации атеросклероза, формировании гипертрофии миокарда левого желудочка, в том числе через механизмы, не зависящие от артериального давления, а также развитии его диастолической дисфункции. Последняя является отправной точкой для старта ХСН с сохраненной фракцией выброса (ХСНсФВ).
По сравнению с пациентами с ХСН со сниженной фракцией выброса наличие ХСНсФВ определяет большую частоту госпитализаций не в связи с декомпенсацией сердечной недостаточности, а из-за сопутствующих заболеваний, таких как дестабилизация течения артериальной гипертензии, декомпенсация сахарного диабета 2 типа, курация которых в целом оказывает большее влияние с точки зрения улучшения прогноза. Таким образом, у пациентов с предиабетом и ХСНсФВ коррекция инсулинорезистентности как первопричины и триггера кардиометаболических нарушений потенциально может улучшить не только показатели инсулин-глюкозного гомеостаза, но и параметры диастолической функции миокарда. Данный литературный обзор посвящен накопленному опыту применения метформина как «стратегического» антидиабетического препарата при ХСНсФВ и рассмотрению потенциально новых точек его приложения в роли протектора сердечно-сосудистой системы.
Негативное влияние сахарного диабета (СД) на сердечно-сосудистую систему подтверждено многочисленными клиническими исследованиями. Однако существуют экспериментальные исследования, в которых показано повышение устойчивости сердца к ишемическим и реперфузионным повреждениям у животных с СД. Этот феномен характеризуется меньшим размером зоны инфаркта, лучшим сохранением сократительной функции миокарда, меньшей частотой возникновения ишемических и реперфузионных аритмий. Предполагается, что на определенной стадии развития СД формируется «метаболическое окно», при котором метаболические изменения на клеточном уровне запускают адаптивные механизмы, способствующие повышению жизнеспособности кардиомиоцитов. Опубликованные данные подтверждают, что выраженность защитного действия, индуцированного СД, сопоставима, а в некоторых случаях даже превышает эффект феномена прекондиционирования. Признается, что механизмы, обеспечивающие защиту сердца от ишемических и реперфузионных повреждений на фоне СД, являются универсальными и связаны с модуляцией антиоксидантной системы, факторов апоптоза, провоспалительных цитокинов, а также сигнальных систем, обеспечивающих выживаемость клеток. Одним из основных патогенетических факторов при СД является гипергликемия, однако при стрессе она выполняет роль адаптивного механизма, направленного на удовлетворение повышенной потребности в энергии в патологических условиях. На определенном этапе СД гипергликемия становится пусковым механизмом развития защитных эффектов и активирует не только сигнальные пути, но и перестройку энергетического метаболизма, что позволяет поддерживать продукцию аденозинтрифосфата на достаточном уровне для сохранения жизнедеятельности клеток сердца в условиях ишемии/реперфузии. Возможно, повышенный уровень глюкозы, сопровождающийся активацией инсулиннезависимых механизмов поступления ее в клетки, а также доступностью этого энергетического субстрата, будет способствовать лучшему восстановлению энергопродукции в клетках сердца после инфаркта, что, в свою очередь, существенно снизит степень повреждения миокарда и будет способствовать сохранению сократительной функции сердца. Выявление условий и механизмов кардиопротекторного феномена, индуцированного СД, позволит моделировать метаболическое состояние, при котором реализуется защита клеток сердца от повреждающих факторов.
Базальный инсулин (БИ) — основная терапевтическая опция у больных сахарным диабетом 2 типа (СД2), не достигших целевых значений гликемии на пероральных сахароснижающих препаратах и/или агонистах рецепторов глюкагоноподобного пептида-1. Результаты эпидемиологических исследований свидетельствуют о том, что большинство больных СД2 не достигают индивидуальных целевых показателей гликемического контроля и на БИ. В данном обзоре проанализированы результаты исследований в реальной клинической практике, в которых оценивались предикторы успеха или неудачи терапии БИ у больных СД2. В ряде исследований продемонстрировано, что отсроченное начало инсулинотерапии с высоким уровнем гликированного гемоглобина (HbA1c) на старте лечения снижает вероятность достижения целевых значений гликемического контроля на БИ. Гипогликемия в первые недели или месяцы лечения БИ может являться ограничивающим фактором в достижении целей гликемического контроля и снижать приверженность лечению. Гларгин 300 Ед/мл и деглудек, длительно действующие аналоги инсулина II поколения, продемонстрировали больший потенциал в снижении уровня HbA1c при меньшем риске гипогликемии по сравнению с другими БИ в исследованиях в условиях реальной клинической практики. В исследованиях DUNE, ATOS и других показан недостаток титрации дозы инсулина у больных СД2, нуждающихся в назначении или интенсификации лечения БИ. Низкая приверженность лечению (пропуск инъекций, неправильный выбор дозы, временное или постоянное прекращение введения инсулина), нарушения техники инъекций инсулина и формирование участков липогипертрофии в местах инъекций также являются широко распространенными проблемами, препятствующими достижению хорошего гликемического контроля у этих больных. Следовательно, обучение пациентов c акцентом на технику инъекций, принципы титрации дозы и профилактику гипогликемии, а также применение аналогов БИ II поколения повышают шансы на успех в достижении целей гликемического контроля больных СД2, начинающих лечение БИ или нуждающихся в интенсификации терапии БИ.
Начало инсулиновой терапии с аналогов базального инсулина стало стандартом лечения сахарного диабета 2 типа (СД2). Своевременное назначение инсулина позволяет не только замедлить прогрессирование СД2, но и снизить частоту и тяжесть связанных с ним осложнений. В настоящей работе проведен обзор эффективности и безопасности применения новейших базальных аналогов инсулина при СД2 с позиции современных клинических рекомендаций, а также рассмотрены обновленные данные по эффективности и безопасности терапии различными представителями класса с учетом их влияния на риск гипогликемий и вариабельность гликемии. Имеющиеся данные свидетельствуют о том, что инсулин деглудек 200 Ед/мл может быть препаратом выбора при высоком риске развития тяжелых форм гипогликемии. Поскольку тяжелая гипогликемия и высокая вариабельность гликемии являются важными факторами риска сердечно-сосудистых событий и смертности, в настоящее время представляется целесообразным подходить более дифференцированно к назначению конкретного инсулина при лечении СД2 с учетом влияния на риск гипогликемий и вариабельность гликемии.
Клинический случай
Проблема нарушений пищевого поведения в настоящее время занимает особое место в медицине. Нервная булимия — одна из основных форм нарушений пищевого поведения, характеризующаяся трудностью лечения, длительным, рецидивирующим течением. Расстройства пищевого поведения часто встречаются у пациентов с сахарным диабетом 1 типа (СД1), особенно у девочек в подростковом возрасте.
В данной статье мы представляем клинический случай пациентки с СД1, нервной булимией, развившейся до манифестации СД1 и прогрессирующей на его фоне.
Пациентка чрезмерно озабочена контролем массы тела, специально ограничивала прием углеводов, принудительно вызывала рвоту. Во время беременности неоднократно выявлялась кетонурия («голодные кетоны»). Минимальный вес 36 кг (ИМТ 15,2 кг/м2). Особый интерес представляет течение беременности у этой пациентки, закончившейся антенатальной гибелью, поскольку ограничения углеводсодержащей пищи и длительное нахождение в состоянии кетоза могли привести к развитию патологии беременности. В результате обследования у пациентки также были выявлены множественные осложнения сахарного диабета и рекуррентное депрессивное расстройство, что требует дальнейшего совместного наблюдения эндокринолога и психиатра.
Сочетание СД1 и расстройства пищевого поведения у беременной пациентки не позволяет отнести данный случай к типичному течению заболевания.
Новости
Принимая во внимание высокую вероятность неблагоприятных исходов у пациентов с сахарным диабетом 1 типа (СД1), а также бремя, создаваемое болезнью, поиск методов, предупреждающих разрушение бета-клеток, имеет первостепенное значение. До недавнего времени все попытки иммунотерапевтических вмешательств не достигали существенных успехов, позволяя в лучшем случае уменьшить скорость разрушения бета-клеток, не останавливая иммунный процесс и не позволяя нормализовать гликемию. В ноябре 2022 г. Управление по санитарному надзору за качеством пищевых продуктов и медикаментов США (FDA) одобрило препарат теплизумаб для замедления развития клинической стадии СД1. Целью публикации является оценка результатов применения препарата теплизумаб у людей на второй (доклинической) стадии СД1, а также рассмотрение дальнейших перспектив данного лечения.

Контент доступен под лицензией Creative Commons Attribution-NonCommercial-NoDerivatives 4.0 International License (CC BY-NC-ND 4.0).
ISSN 2072-0378 (Online)