Перейти к:
Практические аспекты инициации и применения ингибиторов SGLT2 в стационаре и на амбулаторном этапе.
https://doi.org/10.14341/DM12855
Аннотация
В современной терапии сахарного диабета 2 типа (СД2) ингибиторы натрий-глюкозного котранспортера 2 типа (SGLT2) закономерно заняли достойное место благодаря как своим позитивным сахароснижающим свойствам, так и выдающимся кардиоренометаболическим эффектам. Данные последних рандомизированных клинических исследований, таких как DAPAHF, EMPEROR-Reduced и EMPEROR-Preserved, показавших пользу их применения при лечении больных с хронической сердечной недостаточностью без учета наличия или отсутствия СД2, значительно расширяют ареал применения SGLT2 в практике врачей различных специальностей. В настоящем обзоре представляются не только результаты наиболее значимых исследований ингибиторов SGLT2, но и основные подходы к старту терапии этим классом препаратов в условиях различных клинических ситуаций как в стационаре, так и на амбулаторном этапе. Помимо этого, подробно рассматриваются потенциальные нежелательные явления и ограничения, связанные с использованием ингибиторов SGLT2, которые необходимо учитывать при назначении каждому конкретному пациенту. Отдельно изложены практические аспекты назначения ингибиторов SGLT2 через призму их безопасного применения в периоперационный и ранний постинфарктный периоды, а также при других особых состояниях. Особое внимание уделено вопросам мониторинга объективных данных, лабораторных и инструментальных показателей при использовании ингибиторов SGLT2, учет которых позволит минимизировать нежелательные явления и получить максимальную пользу для большого числа пациентов с СД2, так же как больных кардиологического, нефрологического профиля вне зависимости от статуса гликемии.
Ключевые слова
Для цитирования:
Салухов В.В., Галстян Г.Р., Ильинская Т.С. Практические аспекты инициации и применения ингибиторов SGLT2 в стационаре и на амбулаторном этапе. Сахарный диабет. 2022;25(3):275-287. https://doi.org/10.14341/DM12855
For citation:
Salukhov V.V., Galstyan G.R., Ilyinskay T.A. Practical aspects of initiation and use of SGLT2 inhibitors: inpatient and outpatient perspectives. Diabetes mellitus. 2022;25(3):275-287. (In Russ.) https://doi.org/10.14341/DM12855
АКТУАЛЬНОСТЬ
В настоящий момент невозможно представить современное управление сахарным диабетом 2 типа (СД2) без внедрения в терапевтическую практику инновационных сахароснижающих препаратов, которые бы обладали значимым гипогликемическим эффектом, и соответствовали жесткому профилю кардиоренальной безопасности. Последнее десятилетие мировой диабетологии ознаменовано появлением такого класса сахароснижающих препаратов, как ингибиторы натрий-глюкозного котранспортера 2 типа (иSGLT2), или глифлозины [1].
Отличительной особенностью этой группы препаратов является уникальный подход к терапии СД2, реализованный особенным инсулинонезависимым механизмом действия и точками терапевтического приложения. Сахароснижающее действие препаратов этой группы связано с уменьшением реабсорбции глюкозы в почках за счет обратимой блокады вышеупомянутой специфической транспортной системы, и этот механизм уверенно демонстрирует множество клинических преимуществ, включая снижение уровня гликированного гемоглобина, массы тела, артериального давления, уровня мочевой кислоты [2].
иSGLT2, изначально разрабатываемые как сахароснижающие препараты, в многоцентровых клинических исследованиях, посвященных кардиоренальной безопасности, практически в равной степени продемонстрировали позитивное влияние как на сердечно-сосудистые, так и на почечные исходы, уверенно заняв нишу в лечении пациентов с СД2 с сердечно-сосудистой патологией. Востребованность в таком классе препаратов предопределена высокой частотой коморбидности пациентов с СД2 [3], поскольку именно кардиоваскулярные риски наиболее тесно ассоциированы с развитием его неблагоприятных макро- и микрососудистых осложнений [4]. Более того, доказанная в последнее время польза применения иSGLT2 у больных с явлениями сердечной недостаточности и/или хронической болезнью почек без СД2 заметно расширяет диапазон их назначения.
Учитывая вышесказанное, активное внедрение иSGLT2 в клиническую практику требует всестороннего осмысления подходов по их безопасному применению как на амбулаторном этапе, так и в различных клинических ситуациях при стационарном лечении.
НЕДАВНИЕ ОТКРЫТИЯ В ОБЛАСТИ КАРДИОРЕНАЛЬНОЙ БЕЗОПАСНОСТИ ПРЕПАРАТОВ КЛАССА иSGLT2
Состоявшиеся рандомизированные клинические исследования класса иSGLT2 показали выдающиеся кардиоренометаболические эффекты у больных СД2 [5]. Первыми были представлены вдохновляющие результаты проспективного рандомизированного клинического исследования (РКИ) EMPA-REG OUTCOME (терапия эмпаглифлозином в 2 дозах в дополнение к стандартной сахароснижающей терапии), включавшего в себя пациентов с СД2 и подтвержденными сердечно-сосудистыми заболеваниями (табл. 1) [6][7].
Таблица 1. Основные сердечно-сосудистые исходы в исследованиях ингибиторов натрий-глюкозного котранспортера 2 типа
Смерть по сердечно-сосудистым причинам, нефатальный инфаркт, нефатальный инсульт: (первичная комбинированная конечная точка MACE) | Смерть по сердечно-сосудистым причинам (вторичная конечная точка) | Госпитализация по поводу сердечной недостаточности (вторичная конечная точка) | ||
ОР (95% ДИ) | ОР (95% ДИ) | ОР (95% ДИ) | ||
Эмпаглифлозин vs плацебо | EMPA-REG OUTCOME | 0,86* (0,74–0,99) | 0,62* (0,49–0,77) | 0,65* (0,5–0,85) |
Канаглифлозин vs плацебо | CANVAS | 0,86* (0,75–0,97) | 0,87 (0,72–1,06) | 0,67* (0,52–0,87) |
Дапаглифлозин vs плацебо | DECLARE-TIMI 58 | 0,93 (0,84–1,03) | 0,98 (0,82–1,17) | 0,73* (0,61–0,88) |
Эртуглифлозин vs плацебо | VERTIS CV | 0,97 (0,85–1,11) | 0,92 (0,77–1,11) | 0,70* (0,54–0,90) |
В результате исследования CANVASProgram (исследования CANVAS и CANVAS-R), включавшего больных СД2 с подтвержденными сердечно-сосудистыми заболеваниями или множественными факторами риска, были установлены позитивные кардиометаболические эффекты еще одного препарата группы иSGLT2 — канаглифлозина [8].
В исследовании DECLARE-TIMI 58 изучались сердечно-сосудистые исходы на фоне приема еще одного представителя класса — дапаглифлозина. В это исследование, как и в исследование CANVAS Program, были включены пациенты с СД2 с подтвержденными сердечно-сосудистыми заболеваниями или множественными факторами риска [9].
Несколько особняком стоит исследование VERTIS CV, схожее по дизайну с исследованием EMPA-REG OUTCOME, где изучаемый эртуглифлозин, так же как и дапаглифлозин в исследовании DECLARE-TIMI 58, не показал значимого влияния на атеросклеротические события, однако, как и другие представители класса, характеризовался снижением риска госпитализации по причине сердечной недостаточности (ГСН) [7][10][11].
Обнадеживающие результаты вышеупомянутых исследований чрезвычайно заинтересовали исследователей на предмет изучения эффективности иSGLT2 в специальных когортах больных — пациентов с различными фенотипами хронической сердечной недостаточности (ХСН) или хронической болезни почек (ХБП).
Cпособность иSGLT2 реализовывать свое кардио- и ренопротективное действие в отношении больных с ХБП значимо подтвердилась при анализе результатов таких крупномасштабных исследований, как CREDENCE (у больных СД2) и DAPA-CKD (безотносительно статуса диабета) [12]. Результаты оценивали по комбинированной почечной точке — возникновению нефропатии или ее прогрессированию (с некоторым варьированием суррогатных критериев). В рамках исследования DAPA-CKD было продемонстрировано, что первичная композитная конечная точка (время до снижения расчетной скорости клубочковой фильтрации (рСКФ)>50% по сравнению с исходным уровнем, время до терминальной стадии болезни почек, определенное как рСКФ<15 мл/мин/1,73 м2, необходимость в хроническом диализе или трансплантации почки, время до почечной или сердечно-сосудистой смерти) значимо реже встречалась у больных, получавших дапаглифлозин, по сравнению с пациентами, получавшими плацебо (9,2 и 14,5% случаев соответственно) [13].
Также на терапии дапаглифлозином реже достигали вторичных конечных точек (сочетание снижения рСКФ>50%, терминальной стадии болезни почек или почечной смерти; сердечно-сосудистая смерть или ГСН; а также смерть от любой причины). Положительный эффект дапаглифлозина отмечался у больных с ХБП независимо от наличия СД2 и уровня рСКФ [14].
Особенностью исследования CREDENCE являлось включение в исследование пациентов с высоким уровнем альбуминурии (более 300 мг/г) и в большинстве случаев с рСКФ менее 60 мл/мин/1,73 м2 [12]. У пациентов со столь скомпрометированной почечной функцией, получавших в течение 2,6 года канаглифлозин, состоялось снижение на 30% относительного риска (ОР) развития первичной конечной точки (удвоение креатинина крови, развившаяся терминальная почечная недостаточность или летальный исход от почечных/кардиоваскулярных причин). Это сопровождалось устойчивым снижением альбуминурии, а также замедлением снижения рСКФ по сравнению с плацебо (табл. 2) [15].
Таблица 2. Основные результаты почечных исходов в исследованиях CREDENCE и DAPA-CKD
Первичная конечная комбинированная почечная точка | Вторичная почечная точка | Госпитализация по поводу сердечной недостаточности или сердечно-сосудистая смерть (вторичная конечная точка) | ||
ОР (95% ДИ) | ОР (95% ДИ) | ОР (95% ДИ) | ||
Канаглифлозин vs плацебо | CREDENCE | 0,70* (0,59–0,82) | 0,66 (0,53–0,81) | 0,69 (0,5–0,83) |
Дапаглифлозин vs плацебо | DAPA-CKD | 0,61** (0,51–0,72) | 0,56 (0,45–0.68) | 0,71 (0,55–0,92) |
**Время до снижения рСКФ≥50% по сравнению с исходным уровнем подтверждено повторным измерением в течение 28 дней и более по уровню креатинина сыворотки, время до терминальной стадии болезни почек определяется как рСКФ<15 мл/мин/1,73 м2, необходимость в хроническом диализе (оба подтверждены в течение 28 дней и более) или трансплантация почки, время до почечной или сердечно-сосудистой смерти.
Возможно, еще более важным открытием стали результаты исследований, включающих пациентов с ХСН. Действительно, ХСН — одна их главных причин всех госпитализаций у больных в возрасте старше 65 лет. При этом прогноз для жизни пациентов зачастую все равно остается тяжелым, а годичная смертность у госпитализированных и амбулаторных (стабильных) пациентов составляет 17 и 7% соответственно. Действующая классификация ХСН подразумевает ранжирование ее на 3 группы в зависимости от величины фракции выброса (ФВ) левого желудочка (ЛЖ), а именно ХСН с низкой ФВ ЛЖ (СНнФВ) (<40%), СН с несколько сниженной ФВ ЛЖ (40–49%); СН с сохраненной ФВ ЛЖ (СНсФВ) (>50%) [16].
Причем более 50% пациентов из общего количества — это пациенты с СНсФВ, и их доля с учетом эскалации современной кардиотропной терапии значительно увеличивается в отсутствие методов лечения, способных изменить их неблагоприятный прогноз.
Первым крупным исследованием, специально разработанным для оценки пациентов с СНнФВ, стало исследование DAPA-HF (n=4744), в котором было показано, что применение дапаглифлозина безотносительно статуса СД2 приводит к снижению на 26% ОР комбинированной конечной точки, включающей в себя комбинацию сердечно-сосудистой смертности и ухудшения СН (госпитализация или экстренное обращение из-за СН; ОР 0,75; 95% ДИ 0,63–0,90 для больных СД2 и ОР 0,73; 95% ДИ 0,60–0,88 без СД2). Важно отметить, что при изучении компонентов первичной конечной точки выявлено снижение на 18% смертности от сердечно-сосудистых заболеваний (ОР 0,82; 95% ДИ 0,69–0,98). Вместе с тем в исследовании DAPA-HF не состоялось значимого влияния дапаглифлозина на комбинированную почечную точку (табл. 3).
В рамках программы исследований EMPOWER представлены результаты двух ее крупных ветвей EMPEROR-Reduced по влиянию применения эмпаглифлозина на сердечно-сосудистые исходы у пациентов с СНнФВ с/без СД2 и по влиянию на сердечно-сосудистые исходы у пациентов с СНсФВ с/без СД. Первичная и вторичная конечные точки были схожи для обоих исследований. Первичная точка была определена как время до первой подтвержденной сердечно-сосудистой смерти или ГСН, вторичные точки включали первую или повторные ГСН и угловой коэффициент изменения рСКФ по сравнению с исходным уровнем.
По результатам EMPEROR-Preserved (n=5988), включившего пациентов с СД2 и без СД2, возраст старше 18 лет, ФВ ЛЖ >40% (ФК II–IV по NYHA), эмпаглифлозин на 21% снижал риск подтвержденного случая сердечно-сосудистой смерти или подтвержденной ГСН (ОР 0,79; 95% ДИ 0,69–0,90; p<0,001) и на 27% снижал риск первой или повторных ГСН (ОР 0,73; 95% ДИ 0,61–0,88; p<0,001). Важно отметить, что позитивное влияние эмпаглифлозина наблюдалось независимо от гликемического статуса и по всему спектру ФВ, с некоторым ослаблением эффекта у пациентов с ФВ ЛЖ≥60%. Исследование EMPEROR-Reduced, в котором участвовали 3730 пациентов с ХСН II–IV функциональных классов и ФВ ЛЖ≤40%, продемонстрировало существенное положительное многофакторное влияние эмпаглифлозина независимо от наличия CД: по сравнению с плацебо снижение риска сердечно-сосудистой смерти или ГСН на 25% (ОР 0,75; 95% ДИ 0,65–0,86; p<0,001), общего числа ГСН на 30% (ОР 0,70; 95% ДИ 0,58–0,85; p<0,001), скорости ухудшения почечной функции (абсолютная разница снижения рСКФ 1,73 (95% ДИ 1,10–2,37; р<0,001)) [17]. Вместе с тем, анализируя влияние эмпаглифлозина на функцию почек в исследовании EMPEROR-Reduced, было установлено, что в группах больных СНнФВ с разной исходной функцией почек риск развития комбинированной конечной почечной точки (хронический диализ, или трансплантация почек, или устойчивое снижение рСКФ на 40% и более, или устойчивое снижение рСКФ<15 мл/мин/1,73 м2 у пациентов с исходной рСКФ≥30 мл/мин/1,73 м2 либо <10 мл/мин/1,73 м2 у пациентов с исходной рСКФ<30 мл/мин/1,73 м2) снижался на 50% (ОР 0,50; 95% ДИ 0,32–0,77) и статистически значимо темп прогрессирования ХБП был уменьшен вне зависимости от наличия СД (табл. 3) [18].
Таблица 3. Основные результаты кардиоренальных исходов в рандомизированных клинических исследованиях [17, 18]
Исследование | Первая госпитализация по поводу СН или сердечно-сосудистая смерть смерть | Сердечно-сосудистая смерть | Комбинированная почечная точка | |
ОР (95% ДИ) | ОР (95% ДИ) | ОР (95% ДИ) | ||
DAPA-HF | Дапаглифлозин vs плацебо | 0,74 (0,65–0.85) | 0,83 (0,71–0,97) | 0,71 (0,44–1,16) |
EMPEROR-Reduced | Эмпаглифлозин vs плацебо | 0,75 (0,65–0,86) | 0,92 (0,77–1,10) | 0,50 (0,32–0,79) |
EMPEROR- Preserved | Эмпаглифлозин vs плацебо | 0,71 (0,60–0,83) | 0,91 (0,76–1,09) | 0,95 (0,73–1,24) |
Однако в отношении почечных исходов между двумя исследованиями была обнаружена значительная гетерогенность. В частности, в РКИ EMPEROR-Reduced ОР для крупных почечных событий составило 0,50 (95% ДИ 0,32–0,79) по сравнению с 0,95 (95% ДИ 0,73–1,24) в EMPEROR-Preserved, что указывает на то, что применение эмпаглифлозина скажется в отношении почечных исходов в первую очередь у пациентов с СНнФВ. Наконец, тот факт, что эмпаглифлозин в исследовании EMPEROR-Preserved привел к значительной разнице в темпе снижения рСКФ в год по сравнению с плацебо (-1,25 против -2,62; p<0,001), позволяет предположить, что рСКФ не может быть надежным суррогатным показателем почечных исходов в популяции пациентов с ХСН в целом.
Таким образом, результаты, представленные выше, демонстрируют высокую эффективность применения дапаглифлозина у пациентов с СНсФВ как у пациентов с СД2, так и лиц с ХСН без нарушенной толерантности к глюкозе и эмпаглифлозина — у пациентов с ХСН — вне зависимости от ФВ ЛЖ безотносительно статуса СД2 [19]. Результаты исследования EMPEROR-Preserved особенно значимы с учетом отсутствия эффективных стратегий лечения СНсФВ. Следующим крупным исследованием иSGLT2 у пациентов с СНсФВ станет РКИ DELIVER, которое позволит оценить эффективность дапаглифлозина, результаты его ожидаются в 2022 г.
Следует учесть, что во всех крупных исследованиях, посвященных кардиоренальной безопасности класса иSGLT2, соблюдался принцип гликемического равенства, дабы исключить влияние контроля гликемии на полученные результаты. Средние различия между группами составляли менее 0,6%, при значительно большей необходимости для поддержания контроля гликемии в интенсификации гипогликемизирующей терапии в группе плацебо. Представленные результаты должны мотивировать врачей различного профиля к более широкому обоснованному применению препаратов из класса иSGLT2 в области диабетологии, кардиологии, нефрологии, терапии с доказанными сердечно-сосудистыми и почечными эффектами у пациентов. Однако назначение этих препаратов подразумевает соблюдение некоторых правил, что и стало основным предметом изучения данных литературы и личного опыта применения авторов статьи.
ПОЧЕЧНЫЕ И ГЕМОДИНАМИЧЕСКИЕ ОГРАНИЧЕНИЯ
Учитывая тесную связь СД2 с развитием диабетической нефропатии, использование иSGLT2 в указанной группе больных длительное время было дискутабельно. Однако доказанная нефропротективная направленность в сочетании с эффективностью в отношении сердечно-сосудистой патологии у больных СД2 позволили данному классу препаратов занять приоритетное место в лечении больных СД2 и ХБП и получить одобрение как Американской диабетической ассоциации (ADA), так и Европейской ассоциации по изучению сахарного диабета (EASD). Консенсусом по управлению гипергликемией у больных СД2 (2018) и в обновленной версии этого документа (2019 г.) даны разъяснения, что иSGLT2 приоритетны к назначению у больных ХБП (в частности, при рСКФ≥30 и ≤60 мл/мин/1,73 м2 или с альбумин-креатининовым соотношением >30 мг/г, особенно с альбумин-креатининовым соотношением >300 мг/г). При этом сформулировано, что их применение у больных СД2 и ХБП рекомендуется для снижения прогрессирования снижения почечной функции, риска госпитализаций по причине ХСН и риска сердечно-сосудистой смерти и MACE [13][14].
При назначении иSGLT2 необходимо учитывать, что разные представители этого класса ранжированы по уровню допустимой СКФ, прописанному в инструкции по применению лекарственного средства, поэтому обязательным условием для инициации терапии иSGLT2 является определение уровня исходной СКФ у пациентов (табл. 4).
Таблица 4. Противопоказания к назначению представителей класса ингибиторов натрий-глюкозного котранспортера 2 типа по уровню расчетной скорости клубочковой фильтрации. Адаптировано из [20]
Противопоказание | Форсига (дапаглифлозин) | Джардинс (эмпаглифлозин) | Инвокана (канаглифлозин) | Суглат (ипраглифлозин) | Стиглатра (эртуглифлозин) |
<25 мл/мин/1,73 м2 | <30 мл/мин/1,73 м2 | <30 мл/мин/1,73 м2 | <30 мл/мин/1,73 м2 | <45 мл/мин/1,73 м2 |
иSGLT2 часто входят в схемы комбинированной терапии с тиазидами и петлевыми диуретиками, что ведет к усилению действия последних и, следовательно, к увеличению риска гиповолемии/дегидратации и гипотонии, поэтому важным аспектом является соблюдение адекватного питьевого режима на протяжении всего лечения. Возможное снижение рСКФ (3–5 мл/мин/1,73 м2) в первые дни/недели терапии ингибиторами иSGLT2 обусловлено механизмом их действия и не является поводом для отмены препаратов, так как сопровождается последующей стабилизацией клубочковой фильтрации [21].
Терапия иSGLT2 во всех крупных РКИ была ассоциирована с небольшим, но клинически значимым снижением как систолического (САД), так и диастолического артериального давления (ДАД). В ряде исследований показано, что иSGLT2 вызывают снижение САД в диапазоне 3–5 мм рт.ст. и ДАД 2–3 мм рт.ст., уменьшают пульсовое давление и среднее АД [22]. Важно отметить, что снижение АД не сопровождается повышением частоты сердечных сокращений, что связано с отсутствием влияния иSGLT2 на повышение активности симпатической нервной системы.
Гипотензивный эффект глифлозинов связывают с ингибированием SGLT2 в проксимальных канальцах почек, что приводит к диуретическому и слабому натрийуретическому эффектам. Соответственно, при выборе терапии для пациентов, имеющих потенциальный риск гиповолемии, врачу следует руководствоваться клинической оценкой ситуации во избежание развития гипотензии.
Риск побочных эффектов, связанных с гиповолемией /гипотензией, особенно важно учитывать у пожилых и ослабленных больных, пациентов, которые получают лечение диуретиками и/или гипотензивными средствами [23]. Поэтому перед началом применения иSGLT2 следует оценить АД пациента и его объемный статус. В целях минимизации риска развития гипотензии следует воздержаться от назначения иSGLT2 у пациентов с САД<100 мм рт. ст. и ДАД<60 мм рт. ст., а также исключить их применение у гемодинамически нестабильных больных. При нормоволемии/нормотензии у пациентов, принимающих мочегонную и гипотензивную терапию, могут потребоваться снижение на 50% суточной дозы диуретика и пересмотр схемы приема антигипертензивных средств [24]. При этом важно учесть, что в исследованиях, посвященных изучению различных иSGLT2, пациенты должны были принимать максимально переносимые дозы блокаторов ренин-ангиотензиновой системы (РАС). Аналогичная стратегия должна реализовываться в клинической практике, и блокаторы РАС следует рассматривать как приоритетные базовые гипотензивные препараты для комбинации с иSGLT2, которые отменяются последними [25]. В этом смысле монотерапия иSGLT2 будет целесообразна у пациентов, которые не переносят блокаторы РАС.
Если у пациента гиперволемия/гипертензия, то терапию иSGLT2 можно инициировать без коррекции дозы других антигипертензивных или диуретических средств [26].
ПОТЕНЦИАЛЬНЫЕ НЕЖЕЛАТЕЛЬНЫЕ ЯВЛЕНИЯ ПРИ ПРИМЕНЕНИИ SGLT2
Диабетический эугликемический кетоацидоз
Диабетический эугликемический кетоацидоз (эуДКА), ассоциированный с применением иSGLT2, представляет собой серьезное осложнение СД, возникающее при умеренной гипергликемии или даже нормальных значениях глюкозы крови. Согласно данным метаанализа, применение иSGLT2 приводило к 2,5 раза более высокому риску развития эуДКА по сравнению с плацебо или препаратами сравнения (ОР 2,46; 95% ДИ 1,16–5,21), однако частота эуДКА среди пациентов, рандомизированных для приема иSGLT2, была низкой и варьировалась от 0,6 до 2,2 случая на 1000 пациенто-лет [27].
Трудности верификации данного состояния обусловлены особенностями его клинических проявлений (обычно кетоацидоз характеризуется выраженной гипергликемией и/или его развитию предшествует длительный период выраженной гипергликемии), что подразумевает необходимость своевременной диагностики с последующим выбором правильной тактики ведения таких пациентов [28]. С одной стороны, иSGLT2 снижают соотношение инсулина и глюкагона в плазме, что приводит к усилению липолиза и окисления свободных жирных кислот в печени, а также усиленному печеночному кетогенезу (рис. 1).
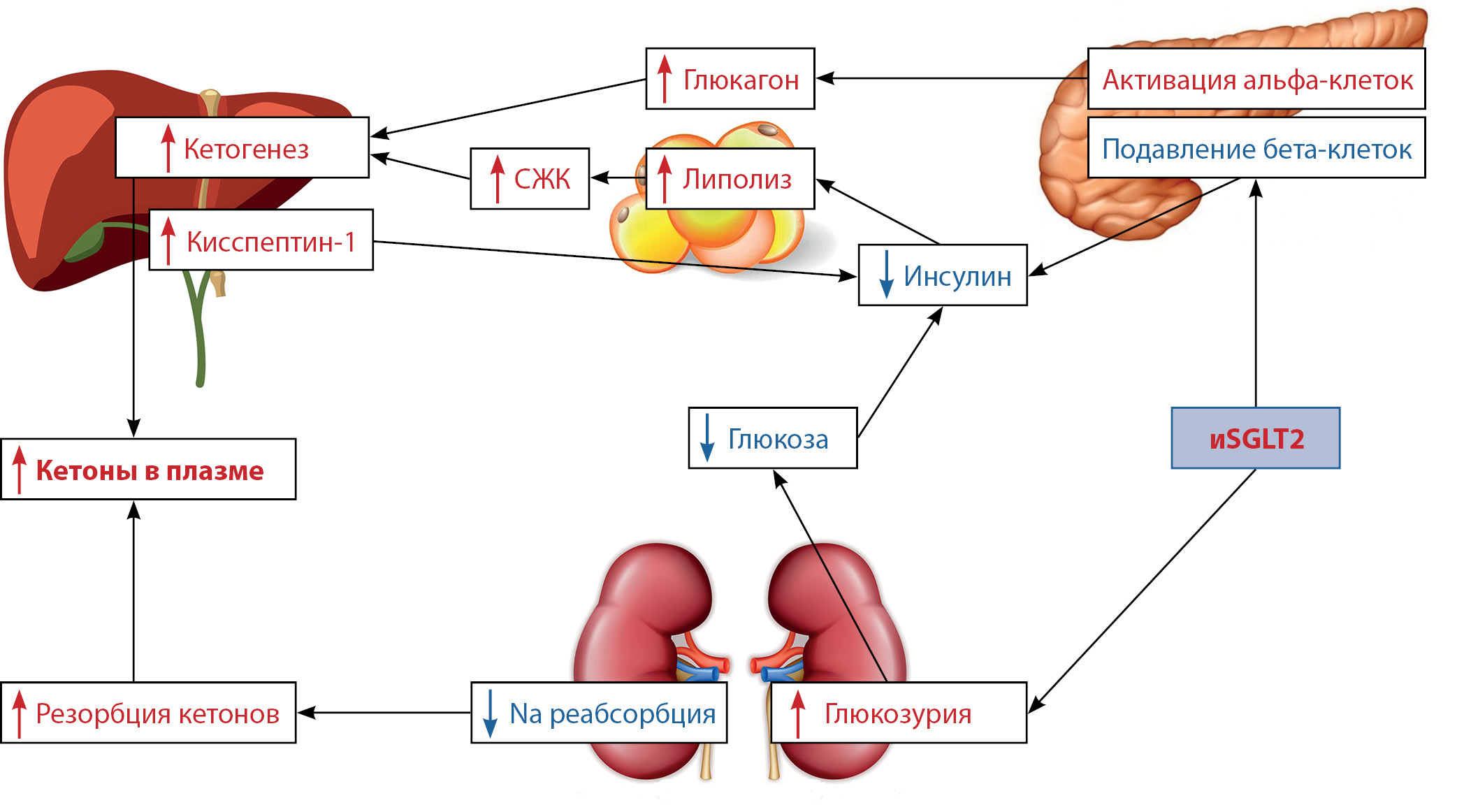
Рисунок 1. Механизмы, лежащие в основе диабетического эугликемического кетоацидоза на фоне приема ингибиторов натрий-глюкозного котранспортера 2 типа. Адаптировано из [29].
Примечание. СЖК - свободные жирные кислоты. иSGLT2 - ингибиторы натрий-глюкозного котранспортера 2 типа
В результате снижения глюкозы в крови секреция инсулина уменьшается, что приводит к активации секреции глюкагона [30]. Кроме того, α-клетки островков Лангерганса экспрессируют рецепторы SGLT2, которые функционируют как чувствительный сенсор глюкозы и блокируются ингибиторами SGLT2 [31]. Блокада этого сенсора имитирует гипогликемию, тем самым запуская порочный круг в виде увеличения секреции глюкагона.
Гиперглюкагонемия, в свою очередь, стимулирует в печени продукцию нейропептида кисспептина-1, который, действуя на β-клетки поджелудочной железы, подавляет секрецию инсулина.
С другой стороны, иSGLT2 увеличивают реабсорбцию кетоновых тел почками, предотвращая обратное всасывание натрия в проксимальных извитых канальцах и тем самым создавая повышенную концентрацию натрия в дистальных частях канальца. Это приводит к появлению электрохимического градиента, способствующего повторной абсорбции отрицательно заряженных кетоновых тел. Следовательно, у пациента может развиться кетоацидоз в отсутствие кетонурии, что в случае ее оценки в качестве инструмента скрининга может дезориентировать врача и затруднить постановку диагноза и, безусловно, диктует необходимость определять уровень кетоновых тел в плазме [32].
Существует ряд провоцирующих факторов эуДКА, о которых нужно помнить при использовании иSGLT2 (табл. 5).
Таблица 5. Факторы, предрасполагающие к диабетическому эугликемическому кетоацидозу при применении ингибиторов натрий-глюкозного котранспортера 2 типа
Провоцирующий фактор | Рекомендации по ведению |
Острые состояния, такие как острая инфекция, диарея, инфаркт миокарда | Отменить прием иSGLT2 до стабилизации состояния |
Среднее и большое оперативное вмешательство | Отменить прием иSGLT2 за 72 ч до операции |
Бариатрическая операция с предварительной гипоуглеводной диетой (в течение 1–2 нед) | Отменить прием иSGLT2 за 2 нед |
Состояния гиповолемии, например, подготовка к колоноскопии; чрезмерная физическая нагрузка (марафонский бег) | Отменить прием иSGLT2 за 48 ч |
Злоупотребление алкоголем (длительное — более суток — употребление алкогольных напитков) | Незамедлительная отмена иSGLT2 |
Соблюдение низкоуглеводной диеты | Отменить прием SGLT2 |
Резкое снижение дозы инсулина | Постепенное уменьшение дозы инсулина |
Наиболее частыми причинами являются такие состояния, как обезвоживание, голодание или соблюдение пациентом низкоуглеводной диеты, интоксикация алкоголем, а также стрессовые состояния, сопровождающиеся повышенной потребностью в инсулине, такие как острые инфекции и хирургические вмешательства.
Именно поэтому каждый пациент должен быть проинформирован врачом о правилах «больничного дня»: при острой инфекции, диарее, рвоте, если пациент не может поддерживать адекватное потребление жидкости и/или пищи и обезвоживается, прием иSGLT2 необходимо прекратить, а возобновить только после возвращения к нормальному режиму питья и питания. В период отмены иSGLT2 для исключения ситуаций утраты гликемического контроля в зависимости от клинической ситуации целесообразно рассмотреть назначение препаратов инкретинового ряда или временной инсулинотерапии.
Слишком значимое снижение дозы инсулина пациентам на фоне применения иSGLT2 может приводить к дефициту инсулина, активации липолиза и кетогенезу в печени и тем самым способно также спровоцировать развитие эуДКА [33].
При диабетическом кетоацидозе, ассоциированном с иSGLT2, жалобы пациентов, как правило, неспецифичны, что затрудняет диагностический поиск, поэтому крайне важно при сборе анамнеза получить данные, указывающие на прием сахароснижающей терапии этой группой препаратов.
Биохимические критерии диагностики кетоацидоза включают значимое увеличение кетонов в плазме (>3 ммоль/л), pH<7,3, уровень бикарбоната сыворотки <15 ммоль. Преобладающий кетон, который можно измерить в самом начале развития кетоацидоза, — это ß-гидроксибутират, составляющий ~78% всех кетоновых тел (ацетоацетат составляет лишь 20%). Содержание кетонов в моче может быть обманчиво низким, поскольку, как изложено выше, иSGLT2 способствуют канальцевой реабсорбции кетоновых тел, а современные анализы кетонурии с использованием экспресс-теста мочи на основе нитропруссида обнаруживают только ацетоацетат. Ацетоацетат в моче становится определяемым только через 2–4 ч после начала нарастания кетонемии [34]. Уровень калия в плазме часто находится в пределах нормы или на ее нижней границе, что связано с экскрецией калия с мочой в сочетании с глюкозурией.
В случае развития эуДКА на фоне приема иSGLT2 препарат незамедлительно отменяют, обеспечивая адекватную инсулинотерапию и регидратацию. Лечение эуДКА должно проводиться только в стационаре в условиях отделения реанимации и интенсивной терапии [35]. Учитывая особенности периода полувыведения препарата из организма, возможны пролонгация периода кетонемии сроком до 12 дней и сохранение кетонурии вплоть до 9 дней после полной отмены, поэтому динамическое наблюдение за пациентом должно осуществляться весь период даже после стабилизации основных витальных показателей. Противопоказано назначение или возобновление иSGLT2 при наличии в анамнезе у пациента эуДКА. Дальнейший выбор сахароснижающей терапии после отмены иSGLT2 должен носить персонифицированный характер в каждом конкретном случае и определяться как состоянием пациента, так и поставленными целями лечения.
Генитальная инфекция
По данным масштабного метаанализа, включавшего 11 состоявшихся РКИ, риск развития инфекций мочевыводящего тракта на фоне приема глифлозинов незначителен и составляет лишь 7% (ОР 1,07; 95% ДИ 1,02–1,13) [36]. Исключением является урогенитальный кандидоз — нередкое нежелательное явление, связанное с применением SGLT2 у пациентов с СД2 и без него, обусловленное глюкозурическим эффектом препаратов, протекающее в виде вульвовагинита/баланита (в гинекологической практике более принят термин вульвовагинальный кандидоз (ВВК)). Также свой вклад вносят и предрасполагающие факторы, такие как восприимчивость больных СД к инфекционным заболеваниям, скомпрометированный гуморальный и клеточный иммунитет, частые медицинские манипуляции, ношение синтетического облегающего белья, лечение антибиотиками широкого спектра, недостаточное соблюдение гигиенических норм.
Однако, несмотря на более высокую частоту возникновения, проявления обычно носят легкую или умеренную степень тяжести и легко поддаются лечению. Исследования реальной клинической практики убедительно демонстрируют, что при приеме иSGLT2 соблюдение определенных правил позволяет минимизировать риск инфекционной урогенитальной патологии. Во-первых, при назначении данных препаратов необходимо определить риск возникновения генитальной инфекции у пациентов, и, как показывают данные A.P. McGovern и соавт., предрасполагающими факторами являются женский пол и предшествующая инфекция в анамнезе [37]. В соответствии с этими данными продемонстрировано, что высокий уровень гликированного гемоглобина (HbA1c) не является фактором риска ВВК, вызванного иSGLT2. Кроме того, кортикостероиды, иммуномодулирующие препараты и терапия эстрогенами не были связаны с дополнительным риском инфицирования ВВК у принимающих глифлозины.
Во-вторых, ключевым моментом является своевременное информирование пациентов, что позволит повысить приверженность к лечению. Пациентам и их партнерам должны быть даны разъясняющие практические рекомендации по соблюдению гигиенических правил, позволяющих минимизировать риск кандидозной инфекции [38]. К ним следует отнести важность гигиены половых органов (например, поддержание сухости половых органов, особенно после мочеиспускания), а также адекватного водного режима. В большинстве случаев генитальные инфекции проходят после стандартной противогрибковой терапии (табл. 6).
Таблица 6. Современные схемы лечения урогенитального кандидоза при приеме ингибиторов натрий-глюкозного котранспортера 2 типа [38][39]
Генитальная инфекция у женщин | |
Острый неосложненный вульвовагинальный кандидоз | Любой из подходов. •Клотримазол (миконазол) вагинальный суппозиторий 100 мг на ночь в течение 7 дней. •Клотримазол (миконазол) вагинальный суппозиторий 200 мг на ночь в течение 3 дней. •Бутоконазол 2%, влагалищный крем по 5 г однократно. •Сертаконазол 300 мг (1 влагалищный суппозиторий) однократно. •Кетоконазол по 1 влагалищной свече (400 мг) в сутки 3–5 дней. •Итраконазол внутрь по 200 мг 2 раза в сутки 3 дня или 200 мг (вагинальная таблетка) 10 дней. •Флуконазол 150 мг per os однократно. •Флуконазол 50 мг перорально один раз в день в течение 7 дней. •Нистатин, влагалищные таблетки по 100 000 ЕД в сутки 14 дней. |
Хронический (рецидивирующий) вульвовагинальный кандидоз | Итраконазол по 200 мг внутрь 2 раза в сутки в течение 3 дней или флуконазол по 150 мг 1 раз в сутки в течение 3 дней и местное лечение препаратами азолового ряда (обычно в течение 14 дней). Профилактика рецидивов: •итраконазол по 200 мг внутрь или флуконазол по 150 мг внутрь в 1-й день менструации в течение 6 мес; •лечение местными препаратами 1 раз в неделю в течение 6 мес |
Генитальная инфекция у мужчин | |
Неосложненный кандидозный баланит | Любой из подходов: •клотримазол 1% крем 2 раза в день в течение 10 дней; •миконазол 2% крем 2 раза в день в течение 10 дней |
Тяжелый кандидозный баланит | Добавить 1% гидрокортизон |
Острая урогенитальная инфекция и лечение местными или системными антимикотиками не требуют прекращения приема иSGLT2, однако рецидивирующая форма ВВК подразумевает отмену терапии глифлозинами и обязательную курацию гинекологом.
Контроль лечения: при остром ВВК эффективность антимикотической терапии оценивают через 7 дней после ее окончания с микроскопией мазков вагинального отделяемого.
При хроническом рецидивирующем ВВК эффективность лечения оценивают в течение трех менструальных циклов в 1-й день после окончания менструации.
Риск ампутаций
Определенная озабоченность в отношении повышенного риска ампутаций на фоне применения канаглифлозина в сравнении с плацебо (ОР 1,97; 95% ДИ 1,41–2,75) возникла в рамках реализации программы CANVAS. Исследование CREDENCE показало, что на фоне применения канаглифлозина в дозе 100 мг не наблюдалось значимого повышения риска ампутаций в сравнении с плацебо (ОР 1,11; 95% ДИ 0,79–1,56), хотя в целом их риск был выше, чем в исследованиях по оценке других иSGLT2 [40]. Это могло быть связано с используемыми стратегиями снижения риска: исключение пациентов с анамнезом травматической ампутации в течение 12 мес скрининга или с активной язвой стопы, остеомиелитом, гангреной либо критической ишемией нижней конечности в течение 6 мес скрининга; кроме того, предусматривалось прерывание терапии в случае возникновения любого из вышеперечисленных явлений с тщательным рассмотрением индивидуальных рисков и преимуществ до возобновления применения канаглифлозина после разрешения явления. В метаанализе (OBSERVE-4D) данных обсервационных исследований влияния канаглифлозина и других сахароснижающих препаратов (включая как иSGLT2, так другие) на риск ампутации ниже колена у пациентов с СД2 не было получено доказательств, указывающих на разницу в риске ампутации между канаглифлозином и другими сахароснижающими препаратами [41]. В 2020 г. FDA удалило специальное предостережение от 2017 г. о повышенном риске ампутаций из инструкции препарата инвокана (канаглифлозин). В уже упоминавшемся выше масштабном метаанализе N. Staplin и соавт. было показано, что влияние применения иSGLT2 на риск ампутации нижних конечностей после исключения результатов исследования CANVAS не имеет статистической значимости и составляет 6% (ОР 1,06; 95% ДИ 0,93–1,21) [36]. В обновленном консенсусе эксперты ADA и EASD дали пояснение, что пациентам с язвами на стопах или больным с высоким риском ампутаций лечение иSGLT2 следует назначать после коллегиального обсуждения с учетом всех рисков и преимуществ, а также при условии комплексного обучения пациента уходу за стопами и принятия соответствующих мер по профилактике ампутаций [42].
ПРАКТИЧЕСКИЕ РЕКОМЕНДАЦИИ ПО КОМБИНАЦИИ ИSGLT2 С ДРУГИМИ САХАРОСНИЖАЮЩИМИ ПРЕПАРАТАМИ У БОЛЬНЫХ СД2
В большинстве случаев лечение иSGLT2 может быть безопасно инициировано у больных СД2 при соблюдении следующих правил.
Необходимо проинформировать пациента о признаках или симптомах кетоацидоза (тошнота, рвота, боль в животе, нарастающая слабость) и проинструктировать о необходимости немедленно обратиться за медицинской помощью при их появлении.
Начало терапии иSGLT2 необходимо предварить исследованием HbA1с. В случае если HbA1с>8%, лечение иSGLT2 может быть инициировано без каких-либо модификаций общей схемы лечения [43].
Если HbA1с 7–8% и пациент получает сахароснижающие препараты с низким риском гипогликемии (метформин, ингибиторы дипептидилпептидазы 4 типа (иДПП-4), агонисты рецепторов глюкагоноподобного пептида 1 (арГПП-1)), возможно назначить иSGLT2 без пересмотра другой терапии. В случае если пациент на такой терапии достигает целевых значений HbA1c (<7%), а клиническая ситуация требует назначения иSGLT2, возможно замещение им метформина или иДПП-4.
Если HbA1с <8% и пациент получает сахароснижающие препараты с высоким риском гипогликемии, например, препараты сульфонилмочевины (СМ) или инсулин, иSGLT2 может быть назначен после корректировки этой терапии.
Если HbA1с <7% или в диапазоне 7–8% и пациент получает и препарат СМ, и инсулин, перед назначением иSGLT2 необходимо скорректировать данную терапию в соответствии с рис. 2.
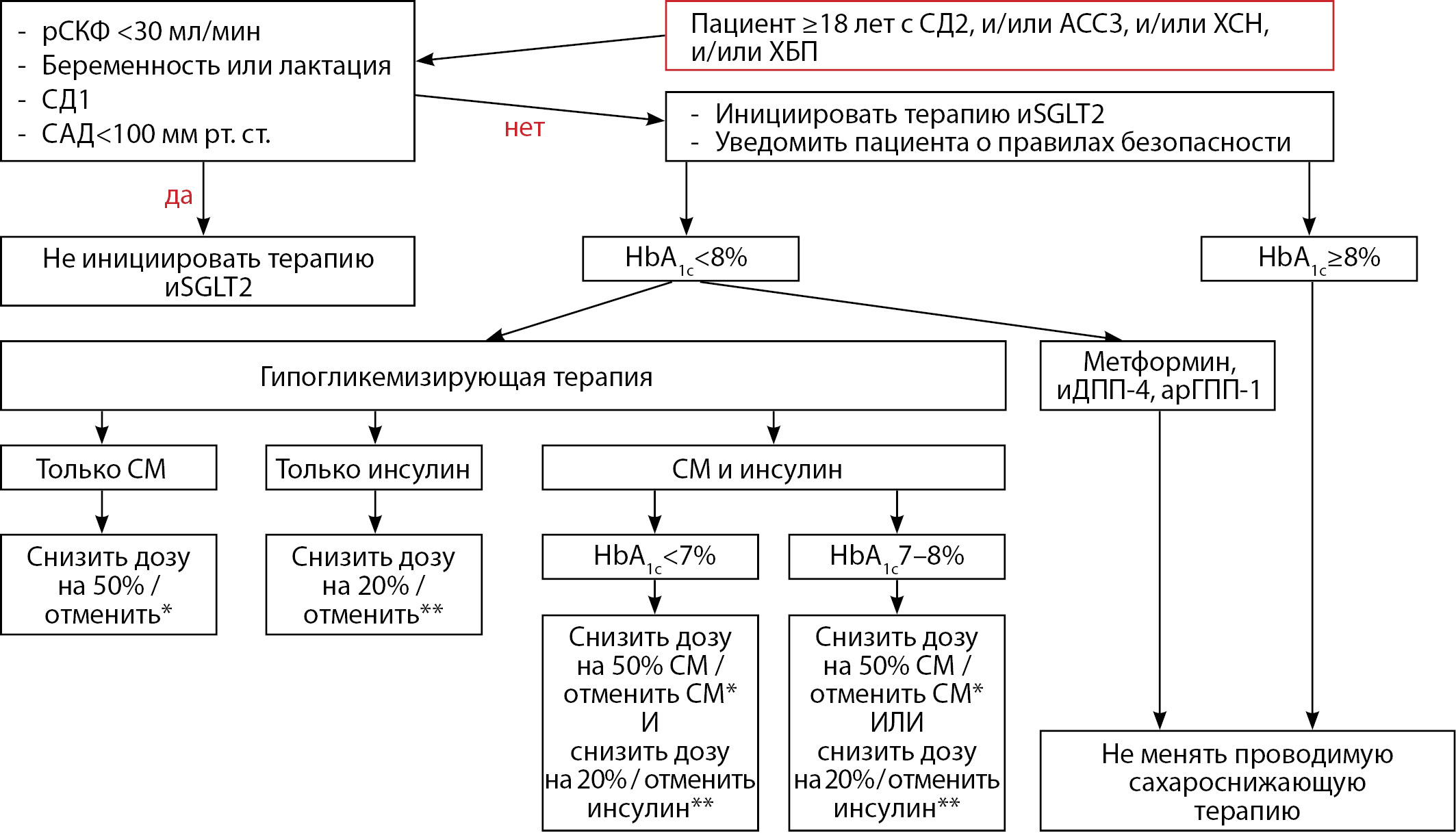
Рисунок 2. Алгоритм коррекции сахароснижающей терапии при назначении ингибитора натрий-глюкозного котранспортера 2 типа. Адаптировано из [43].
* — отменить СМ, если пациент принимает глибенкламид ≤5 мг/сут, или гликлазид ≤60 мг/сут, или глимепирид ≤ 2 мг/сут. В остальных случаях снизить дозу СМ на 50%.
** — отменить инсулин, если суточная доза составляет до 12 ЕД. В остальных случаях снизить общую суточную дозу на 20%.
Примечание. рСКФ — расчетная скорость клубочковой фильтрации. САД — систолическое артериальное давление. АССЗ — атеросклеротическое сердечно-сосудистое заболевание. ХСН — хроническая сердечная недостаточность. ХБП - хроническая болезнь почек. иSGLT2 — ингибиторы натрий-глюкозного котранспортера 2 типа. СМ — сульфонилмочевина. иДПП-4 — ингибиторы дипептидилпептидазы 4 типа. арГПП-1 — агонисты рецепторов глюкагоноподобного пептида 1.
ОСОБЕННОСТИ ВЕДЕНИЯ ПАЦИЕНТОВ, ПОЛУЧАЮЩИХ SGLT2 В ПЕРИОПЕРАЦИОННОМ ПЕРИОДЕ
По статистике, пациенты, страдающие СД, значительно чаще нуждаются в оперативном лечении, а из-за патогенетических аспектов заболевания более подвержены риску послеоперационных хирургических осложнений. Поэтому особенности ведения таких больных на всех этапах периоперационного периода требует неукоснительного соблюдения рекомендаций и коллегиальной работы врачей-клиницистов различных специальностей [44]. Причинами декомпенсации СД в процессе лечения хирургического заболевания могут стать хирургическая травма, наркоз, эмоциональное состояние пациента, предоперационный период вынужденного голодания, пропуски приема пищи и отсутствие аппетита в послеоперационный период [45]. Своевременная отмена и коррекция сахароснижающей терапии в периоперационном периоде имеют важное значение для минимизации осложнений. Операционный стресс, снижение калорийности пищи на фоне приема иSGLT2 создают риск развития эуДКА [35]. Сроки отмены препарата зависят от объема и длительности операции. При проведении малого хирургического вмешательства, позволяющего выполнить операцию под местным обезболиванием, отмена препарата не требуется. С целью минимизировать риск развития эуДКА Американская ассоциация клинических эндокринологов (AACE) и Американский колледж эндокринологов (ACE) в случае планового среднего или большого оперативного вмешательства (т.е. требующих изменения питания, регионарной анестезии или наркоза), терапию иSGLT2 следует временно прекратить за 72 ч до операции. Также рекомендуется временно прекратить прием иSGLT2 за 48 ч перед такими инвазивными процедурами, как колоноскопия, подразумевающими особый водный и гипоуглеводный режим подготовки пациента [30][46]. Эти рекомендации согласуются и с 10-м пересмотром Алгоритмов оказания специализированной помощи больным сахарным диабетом [20]. Если пациенту требуется экстренное хирургическое вмешательство, рекомендуется как можно раньше прекратить прием иSGLT2, оценив исходный уровень кетонов, и по возможности пролонгировать время до начала операции. В этом случае необычайно важно в течение последующих 72 ч поддерживать надлежащую гидратацию организма, обеспечивать достаточное поступление углеводов и контролировать уровень гликемии и кетонов. После операции необходимо проводить строгий контроль маркеров эуДКА до тех пор, пока состояние пациента не стабилизируется и не нормализуются показатели водно-электролитного обмена. Если ранее пациент принимал инсулин, следует продолжить его прием до и после операции, с осторожностью корректируя дозу (во избежание развития эуДКА вследствие дефицита инсулина) [47].
Бариатрические операции заслуживают особого внимания, поскольку за 1–2 нед до операции пациентов часто переводят на низкоуглеводную диету с высоким содержанием белка, чтобы улучшить визуализацию операционного поля во время лапароскопических процедур [48]. В связи с этим за 2 нед до бариатрической операции необходимо приостановить прием иSGLT2.
Возобновление терапии иSGLT2 после хирургического вмешательства следует осуществлять после восстановления нормального режима питания и водного баланса при условии нормоволемии, отсутствия кетоза или смещения метаболических процессов в сторону катаболизма (примерно через 3–5 дней после операции для большинства пациентов, до 4–6 нед для тех, кто перенес бариатрическую операцию).
Не следует начинать или продолжать прием иSGLT2 у пациентов на парентеральном питании, при голодании или соблюдении низкокалорийной диеты (менее 900 ккал/сут) либо низкоуглеводной диеты для снижения массы тела — если суточный рацион предполагает употребление менее 40 г углеводов [47][49].
ОСОБЕННОСТИ НАЗНАЧЕНИЯ ИSGLT2 ПАЦИЕНТАМ В СТАЦИОНАРЕ ПОСЛЕ ПЕРЕНЕСЕННОГО СЕРДЕЧНО-СОСУДИСТОГО СОБЫТИЯ
Особенностями проведения крупных РКИ являются строгий отбор и рандомизация пациентов в группы на основе жестких критериев включения и исключения, и, как правило, это происходит в рамках амбулаторного этапа. Вопрос о своевременности и инициации терапии иSGLT2 в условиях стационарного лечения, несмотря на внушительную доказательную базу позитивного влияния на сердечно-сосудистые и почечные исходы, требует дополнительного прояснения. В клинических рекомендациях нет однозначных противопоказаний для назначения иSGLT2 в стационаре у пациентов, перенесших такие состояния как острое нарушение мозгового кровообращения, декомпенсация ХСН или острый коронарный синдром, однако тяжесть этих состояний, требует от клинициста взвешенного и продуманного решения с учетом соотношения вреда и пользы, а также соблюдения инструкции к препаратам и прочих правил.
Позитивное влияние на большие атеросклеротические события, продемонстрированное в РКИ, эмпаглифлозина и канаглифлозина, наводят на мысль о том, что их применение протективным образом влияет на состояние миокарда и кардиомиоцитов. Действительно, на экспериментальных моделях острого инфаркта миокарда применение иSGLT2 приводило к прямым и отсроченным эффектам с уменьшением зоны инфаркта и последующим снижением выраженности развивающейся ХСН [50]. При этом была показана польза применения различных иSGLT2, назначаемых до экспериментального инфаркта миокарда, во время инфаркта и после состоявшегося повреждения миокарда, в последнем случае — тоже значимо, но в более отдаленном периоде [51]. По-видимому, многофакторное действие ингибирования SGLT2, связанное с улучшением энергетики миокарда, антифибротической, противовоспалительной и антиапоптотической активностью, минимизирует ремоделирование миокарда, замедляет прогрессирование ХСН и позволяет миокарду легче переносить эпизоды ишемии. Немаловажно, что подобная кардиопротективная эффективность иSGLT2 продемонстрирована независимо от диабетического статуса. Таким образом, сегодня уже имеется экспериментальная доказательная база, позволяющая считать целесообразным назначение иSGLT2 у пациентов после инфаркта миокарда при соблюдении барьерных ограничений, изложенных ниже.
До начала инициации терапии иSGLT2 у стационарного пациента, недавно перенесшего сердечно-сосудистое событие, необходимо удостовериться, что состояние пациента является стабильным и соответствует основным критическим критериям, затрагивающим гемодинамический статус пациента, оценку функции почек с обязательным определением рСКФ, наличие жизнеугрожающих состояний и перспективу проведения определенных медицинских вмешательств (рис. 3).
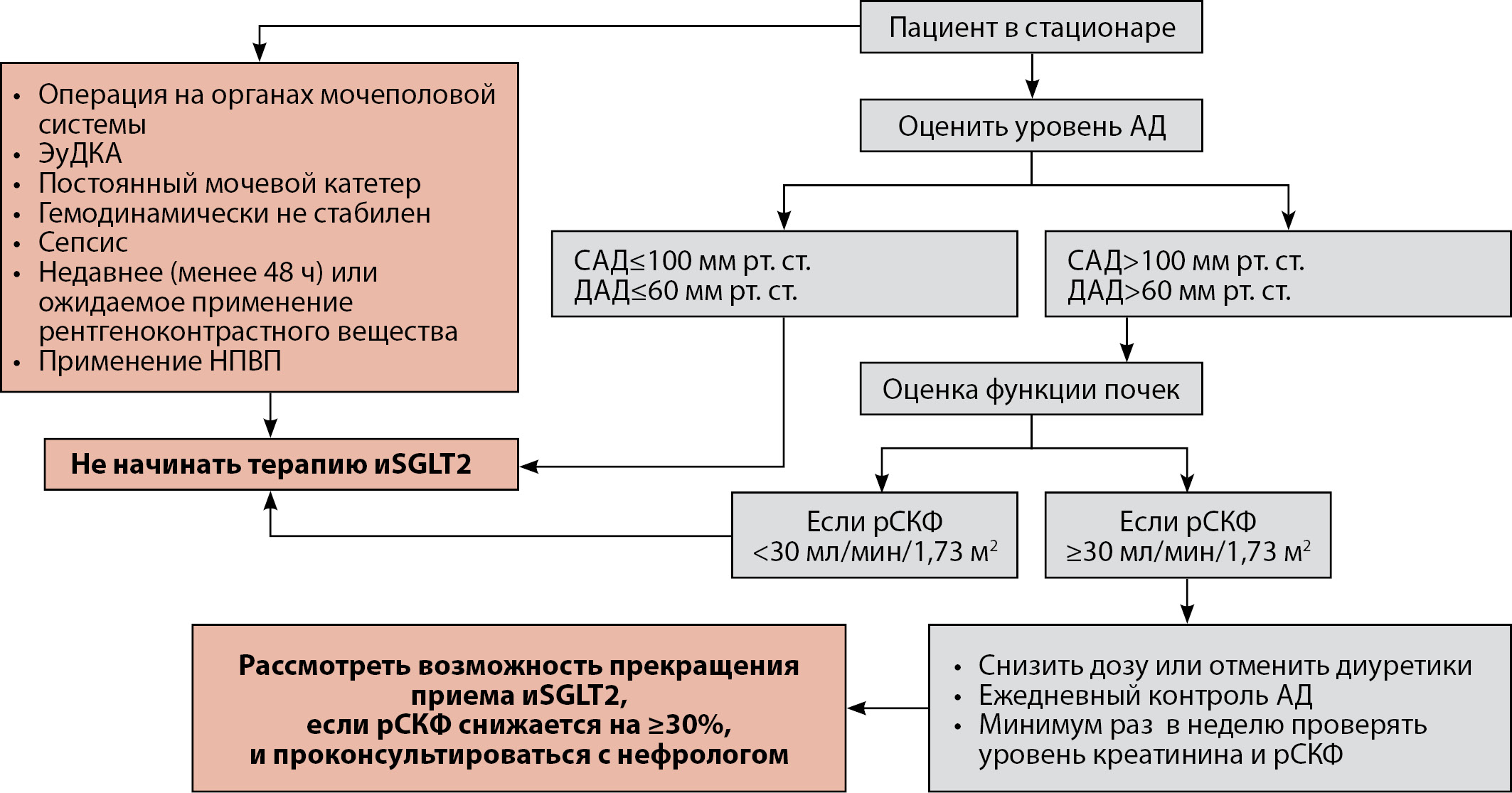
Рисунок 3. Общие рекомендации по старту терапии ингибиторами натрий-глюкозного котранспортера 2 типа у пациентов с сахарным диабетом 2 типа и атеросклеротическими сердечно-сосудистыми заболеваниями в стационаре. Адаптировано из [47].
Примечание. ЭуДКА — диабетический эугликемический кетоацидоз. НПВП — нестереоидные противовоспалительные препараты. рСКФ —расчетная скорость клубочковой фильтрации. АД — артериальное давление. САД — систолическое артериальное давление. ДАД — диастолическое артериальное давление. иSGLT2 — ингибиторы натрий-глюкозного котранспортера 2 типа.
Впервые назначая терапию иSGLT2, необходимо обсудить с пациентом схему приема препарата, рассказать о возможном риске развития эуДКА и его симптомах, необходимости контроля артериального давления, функции почек и гликемии, оценить приверженность к лечению. Следует также уведомить пациента обо всех ожидаемых преимуществах, касающихся улучшения прогноза жизни, снижения вероятности развития новых событий и стабилизации функции почек. До инициации терапии, иSGLT2 должна быть оценена действующая схема сахароснижающей терапии во избежание нежелательного гипогликемического эффекта от комбинации с другими препаратами, а пациентам, находящимся на инсулинотерапии следует запланировать постепенное снижение суточной дозы инсулина, но не более чем на 10–20% от общего количества из-за риска развития эуДКА [52]. Учитывая, что накопленные данные о назначении иSGLT2 в стационаре пока ограничены, за пациентом в течение 3 нед должен осуществляться динамический контроль на амбулаторном этапе.
ЗАКЛЮЧЕНИЕ
Резюмируя, следует отметить, что при неукоснительном соблюдении правил назначения и использования иSGLT2 полностью удовлетворяют строгим требованиям безопасности во всех исследуемых направлениях. Нежелательные явления иSGLT2 в большинстве случаев предотвратимы и управляемы. При назначении иSGLT2 обязательной является оценка гемодинамической стабильности пациентов, рСКФ с пересмотром сахароснижающей, гипотензивной и диуретической терапии. Временное прекращение приема иSGLT2 рекомендовано у пациентов с повышенным риском обезвоживания, включая подготовку к плановым или экстренным оперативным вмешательствам, а сроки отмены зависят от характера и длительности планируемой операции. При инициации терапии иSGLT2 необходим более тщательный лабораторный мониторинг пациента по основным показателям в ближайшее время после назначения.
ДОПОЛНИТЕЛЬНАЯ ИНФОРМАЦИЯ
Источники финансирования. Исследование и публикация работы проведены без внешнего финансирования.
Конфликт интересов. Авторы декларируют отсутствие явных и потенциальных конфликтов интересов, связанных с содержанием настоящей статьи.
Участие авторов. Салухов В.В. — концепция и дизайн статьи, анализ литературы, написание текста, редакционная правка; Галстян Г.Р. — концепция статьи и анализ литературы, написание текста, внесение существенных правок; Ильинская Т.А. — анализ данных, написание текста, подготовка рисунков. Все авторы одобрили финальную версию статьи перед публикацией, выразили согласие нести ответственность за все аспекты работы, подразумевающую надлежащее изучение и решение вопросов, связанных с точностью или добросовестностью любой части работы.
Список литературы
1. Tancredi M, Rosengren A, Svensson A-M, et al. Excess Mortality among Persons with Type 2 Diabetes. N Engl J Med. 2015;373(18):1720-1732. doi: https://doi.org/10.1056/NEJMoa1504347
2. Mintz ML. Role of the Kidney in Type 2 Diabetes and Mechanism of Action of Sodium Glucose Cotransporter-2 Inhibitors. JFP-Diabetes. [Internet] 2016;65(12) Available from: https://www.mdedge.com/content/role-kidney-type-2-diabetes-and-mechanism-actionsodium-glucose-cotransporter-2-inhibitors
3. Вербовой А.Ф., Вербовая Н.И., Долгих Ю.А. Симбиоз кардиологии и эндокринологии // Медицинский совет. — 2020. — №14. — С. 80–89. doi: https://doi.org/10.21518/2079-701X-2020-14-80-89
4. Рубцов Ю.Е., Крюков Е.В., Халимов Ю.Ш. Сосудистое старение и сахарный диабет 2 типа // Эндокринология: новости, мнения, обучение. — 2021. — Т. 10. — №1. — C. 52–61. doi: https://doi.org/10.33029/2304-9529-2021-10-1-52-61
5. Салухов В.В., Котова М.Е. Основные эффекты, вызываемые ингибиторами SGLT2 у больных сахарным диабетом типа 2, и механизмы, которые их определяют // Эндокринология: новости, мнения, обучение. — 2019. — Т. 8. — №3. — С. 61-74. doi: https://doi.org/10.24411/2304-9529-2019-13007
6. Fitchett D, Zinman B, Wanner C, et al. Heart failure outcomes with empagliflozin in patients with type 2 diabetes at high cardiovascular risk: results of the EMPA-REG OUTCOME® trial. Eur Heart J. 2016;37(19):1526-1534. doi: https://doi.org/10.1093/eurheartj/ehv728
7. Zinman B, Wanner C, Lachin JM, et al. Empagliflozin, Cardiovascular Outcomes, and Mortality in Type 2 Diabetes. N Engl J Med. 2015;373(22):2117-2128. doi: https://doi.org/10.1056/NEJMoa1504720
8. Neal B, Perkovic V, Mahaffey KW, et al. Canagliflozin and Cardiovascular and Renal Events in Type 2 Diabetes. N Engl J Med. 2017;377(7):644-657. doi: https://doi.org/10.1056/NEJMoa1611925
9. Шестакова М.В. Исследование DECLARE-TIMI 58 вконтексте EMPA-REG OUTCOME и CANVAS // Сахарный диабет. — 2019. — Т. 22. — №6. — С. 592-601. doi: https://doi.org/10.14341/DM10289
10. Салухов В.В., Ильинская Т.А. Новый ингибитор SGLT2 эртуглифлозин: безопасная эффективность в управлении сахарным диабетом 2-го типа // Медицинскийсовет. — 2020. — №7. — С. 32-41. doi: https://doi.org/10.21518/2079-701X-2020-7-32-41
11. Wiviott SD, Raz I, Bonaca MP, et al. Dapagliflozin and cardiovascular outcomes in type 2 diabetes. N Engl J Med. 2019;380(4):347-357. doi: https://doi.org/10.1056/NEJMoa1812389
12. Батюшин М.М. Дапаглифлозин и профилактика неблагоприятных исходов при хронической болезни почек: результаты исследования DAPA-CKD // Терапевтический архив. — 2021. — Т. 93. — №6. — С. 713-723. doi: https://doi.org/10.26442/00403660.2021.6.200891
13. Дедов И.И., Шестакова М.В., Майоров А.Ю., и др. Алгоритмы специализированной медицинской помощи больным сахарным диабетом: Клинические рекомендации (Вып. 9) // Сахарный диабет. — 2019. — Т. 22. — №S1. — С. 1-144. doi: https://doi.org/10.14341/DM221S1
14. Салухов В.В., Халимов Ю.Ш., Шустов С.Б., Попов С.И. Ингибиторы SGLT2 и почки: механизмы и основные эффекты у больных сахарным диабетом 2 типа // Сахарный диабет. — 2020. — Т. 23. — №5. — С. 475-491. doi: https://doi.org/10.14341/DM12123
15. Rhee JJ, Jardine MJ, Chertow GM, Mahaffey KW. Dedicated kidney disease‐focused outcome trials with sodium‐glucose cotransporter‐2 inhibitors: Lessons from CREDENCE and expectations from DAPA‐HF, DAPA‐CKD, and EMPA‐KIDNEY. Diabetes, Obes Metab. 2020;22(S1):46-54. doi: https://doi.org/10.1111/dom.13987
16. Bozkurt B, Coats AJS, Tsutsui H, et al. Universal definition and classification of heart failure: a report of the Heart Failure Society of America, Heart Failure Association of the European Society of Cardiology, Japanese Heart Failure Society and Writing Committee of the Universal Definition. Eur J Heart Fail. 2021;23(3):352-380. doi: https://doi.org/10.1002/ejhf.2115
17. Anker SD, Butler J, Filippatos GS, Jamal W, Salsali A, Schnee J, Kimura K, Zeller C, George J, Brueckmann M, Zannad F, Packer M; EMPEROR-Preserved Trial Committees and Investigators. Evaluation of the effects of sodium-glucose co-transporter 2 inhibition with empagliflozin on morbidity and mortality in patients with chronic heart failure and a preserved ejection fraction: rationale for and design of the EMPEROR-Preserved Trial. Eur J Heart Fail. 2019 Oct;21(10):1279-1287. doi: 10.1002/ejhf.1596
18. Williams DM, Evans M. Are SGLT-2 Inhibitors the Future of Heart Failure Treatment? The EMPEROR-Preserved and EMPEROR-Reduced Trials. Diabetes Ther. 2020;11(9):1925-1934. doi: https://doi.org/10.1007/s13300-020-00889-9
19. Виллевальде С.В., Галявич А.С., Виноградова Н.Г., и др. Резолюция онлайн-совещания экспертов Приволжского федерального округа по результатам исследования EMPEROR-Reduced «Новая эра в лечении пациентов с ХСН. От исследования EMPA-REG OUTCOME к исследованию EMPEROR-Reduced» // Российский кардиологический журнал. — 2021. — Т. 26. — №2S. — С. 4562. doi: https://doi.org/10.15829/1560-4071-2021-4562
20. Дедов И.И., Шестакова М.В., Майоров А.Ю., и др. Алгоритмы специализированной медицинской помощи больным сахарным диабетом. (10-й выпуск) // Сахарный диабет. — 2021. — Т. 24 — №S1. — С. 1-232. doi: https://doi.org/10.14341/DM12802
21. Barnett AH, Mithal A, Manassie J, et al. Efficacy and safety of empagliflozin added to existing antidiabetes treatment in patients with type 2 diabetes and chronic kidney disease: a randomised, double-blind, placebo-controlled trial. Lancet Diabetes Endocrinol. 2014;2(5):369-384. doi: https://doi.org/10.1016/S2213-8587(13)70208-0
22. Gulsin GS, Graham-Brown MPM, Squire IB, et al. Benefits of sodium glucose cotransporter 2 inhibitors across the spectrum of cardiovascular diseases. Heart. 2022;108(1):16-21. doi: https://doi.org/10.1136/heartjnl-2021-319185
23. Cherney DZI, Udell JA. Use of Sodium Glucose Cotransporter 2 Inhibitors in the Hands of Cardiologists. Circulation. 2016;134(24):1915-1917. doi: https://doi.org/10.1161/CIRCULATIONAHA.116.024764
24. Gomez-Peralta F, Abreu C, Lecube A, et al. Practical Approach to Initiating SGLT2 Inhibitors in Type 2 Diabetes. Diabetes Ther. 2017;8(5):953-962. doi: https://doi.org/10.1007/s13300-017-0277-0
25. Cai Y, Shi W, Xu G. The efficacy and safety of SGLT2 inhibitors combined with ACEI/ARBs in the treatment of type 2 diabetes mellitus: A meta-analysis of randomized controlled studies. Expert Opin Drug Saf. 2020;19(11):1497-1504. doi: https://doi.org/10.1080/14740338.2020.1817378
26. Lam D, Shaikh A. Real-Life Prescribing of SGLT2 Inhibitors: How to Handle the Other Medications, Including GlucoseLowering Drugs and Diuretics. Kidney360. 2021;2(4):742-746. doi: https://doi.org/10.34067/KID.0000412021
27. Colacci M, Fralick J, Odutayo A. et al. Sodium-Glucose Cotransporter-2 Inhibitors and Risk of Diabetic Ketoacidosis Among Adults With Type 2 Diabetes: A Systematic Review and Meta-Analysis. Can J Diabetes. 2022;46(1):10-15. doi: https://doi.org/10.1016/j.jcjd.2021.04.006
28. Pfützner A, Klonoff D, Heinemann L, et al. Euglycemic ketosis in patients with type 2 diabetes on SGLT2-inhibitor therapy—an emerging problem and solutions offered by diabetes technology. Endocrine. 2017;56(1):212-216. doi: https://doi.org/10.1007/s12020-017-1264-y
29. Somagutta M R, Agadi K, Hange N, et al. Euglycemic Diabetic Ketoacidosis and Sodium-Glucose Cotransporter-2 Inhibitors: A Focused Review of Pathophysiology, Risk Factors, and Triggers. Cureus. 2021;13(3):e13665. doi: https://doi.org/10.7759/cureus.13665
30. Burke KR, Schumacher CA, Harpe SE. SGLT2 Inhibitors: A Systematic Review of Diabetic Ketoacidosis and Related Risk Factors in the Primary Literature. Pharmacother J Hum Pharmacol Drug Ther. 2017;37(2):187-194. doi: https://doi.org/10.1002/phar.1881
31. Bonner C, Kerr-Conte J, Gmyr V, et al. Inhibition of the glucose transporter SGLT2 with dapagliflozin in pancreatic alpha cells triggers glucagon secretion. Nat Med. 2015;21(5):512-517. doi: https://doi.org/10.1038/nm.3828
32. Goldenberg RM, Berard LD, Cheng AYY, et al. SGLT2 Inhibitor–associated Diabetic Ketoacidosis: Clinical Review and Recommendations for Prevention and Diagnosis. Clin Ther. 2016;38(12):2654-2664.e1. doi: https://doi.org/10.1016/j.clinthera.2016.11.002
33. Handelsman Y, Henry RR, Bloomgarden ZT, et al. American Association of Clinical Endocrinologists and American College of Endocrinology Position Statement on the Association of SGLT-2 Inhibitors and Diabetic Ketoacidosis. Endocr Pract. 2016;22(6):753-762. doi: https://doi.org/10.4158/EP161292.PS
34. Bonora BM, Avogaro A, Fadini GP. Sodium‐glucose co‐transporter‐2 inhibitors and diabetic ketoacidosis: A n updated review of the literature. Diabetes, Obes Metab. 2018;20(1):25-33. doi: https://doi.org/10.1111/dom.13012
35. Storgaard H, Bagger JI, Knop FK, et al. Diabetic Ketoacidosis in a Patient with Type 2 Diabetes After Initiation of Sodium-Glucose Cotransporter 2 Inhibitor Treatment. Basic Clin Pharmacol Toxicol. 2016;118(2):168-170. doi: https://doi.org/10.1111/bcpt.12457
36. Staplin N, Roddick AJ, Emberson J, et al. Net effects of sodium-glucose co-transporter-2 inhibition in different patient groups: a meta-analysis of large placebo-controlled randomized trials. eClinicalMedicine. 2021;41(2):101163. doi: https://doi.org/10.1016/j.eclinm.2021.101163
37. McGovern AP, Hogg M, Shields BM, et al. Risk factors for genital infections in people initiating SGLT2 inhibitors and their impact on discontinuation. BMJ Open Diabetes Res Care. 2020;8(1):e001238. doi: https://doi.org/10.1136/bmjdrc-2020-001238
38. Unnikrishnan A, Kalra S, Purandare V, Vasnawala H. Genital infections with sodium glucose cotransporter-2 inhibitors: Occurrence and management in patients with type 2 diabetes mellitus. Indian J Endocrinol Metab. 2018;22(6):837. doi: https://doi.org/10.4103/ijem.IJEM_159_17
39. Farr A, Effendy I, Frey Tirri B, et al. Guideline: Vulvovaginal candidosis (AWMF 015/072, level S2k). Mycoses. 2021;64(6):583-602. doi: https://doi.org/10.1111/myc.13248
40. Rådholm K, Figtree G, Perkovic V, et al. Canagliflozin and Heart Failure in Type 2 Diabetes Mellitus. Circulation. 2018;138(5):458-468. doi: https://doi.org/10.1161/CIRCULATIONAHA.118.034222
41. Ryan PB, Buse JB, Schuemie MJ, et al. Comparative effectiveness of canagliflozin, SGLT2 inhibitors and non‐ SGLT2 inhibitors on the risk of hospitalization for heart failure and amputation in patients with type 2 diabetes mellitus: A real‐world meta‐analysis of 4 observational databases (OBSER. Diabetes, Obes Metab. 2018;20(11):2585-2597. doi: https://doi.org/10.1111/dom.13424
42. Buse JB, Wexler DJ, Tsapas A, et al. 2019 Update to: Management of Hyperglycemia in Type 2 Diabetes, 2018. A Consensus Report by the American Diabetes Association (ADA) and the European Association for the Study of Diabetes (EASD). Diabetes Care. 2020;43(2):487-493. doi: https://doi.org/10.2337/dci19-0066
43. Zwart K, Velthuis S, Polyukhovych YV, et al. Sodiumglucose cotransporter 2 inhibitors: a practical guide for the Dutch cardiologist based on real-world experience. Netherlands Hear J. 2021;29(10):490-499. doi: https://doi.org/10.1007/s12471-021-01580-9
44. Nathan DM. Long-term complications of diabetes mellitus. N Engl J Med. 2017;3(28):76-85
45. Milder DA, Milder TY, Kam PCA. Sodium-glucose cotransporter type-2 inhibitors: pharmacology and perioperative considerations. Anaesthesia. 2018;73(8):1008-1018. doi: https://doi.org/10.1111/anae.14251
46. Handelsman Y, Henry RR, Bloomgarden ZT, et al. American Association of Clinical Endocrinologists and American College of Endocrinology Position Statement on the Association of SGLT-2 Inhibitors and Diabetic Ketoacidosis. Endocr Pract. 2016;22(6):753-762. doi: https://doi.org/10.4158/EP161292.PS
47. Mazer CD, Arnaout A, Connelly KA, et al. Sodium-glucose cotransporter 2 inhibitors and type 2 diabetes: clinical pearls for in-hospital initiation, in-hospital management, and postdischarge. Curr Opin Cardiol. 2020;35(2):178-186. doi: https://doi.org/10.1097/HCO.0000000000000704
48. Ким Д.А., Анищенко В.В. Бариатрическая хирургия в управлении сахарным диабетом 2 типа. Сахарный диабет-2021: от мониторинга к управлению. Новосибирск, 2021. С. 56-59.
49. Thiruvenkatarajan V, Meyer EJ, Nanjappa N, et al. Perioperative diabetic ketoacidosis associated with sodium-glucose cotransporter-2 inhibitors: a systematic review. Br J Anaesth. 2019;123(1):27-36. doi: https://doi.org/10.1016/j.bja.2019.03.028
50. Andreadou I, Bell RM, Bøtker HE, Zuurbier CJ. SGLT2 inhibitors reduce infarct size in reperfused ischemic heart and improve cardiac function during ischemic episodes in preclinical models. Biochim Biophys Acta - Mol Basis Dis. 2020;1866(7):165770. doi: https://doi.org/10.1016/j.bbadis.2020.165770
51. Von Lewinski D, Benedikt M, Tripolt N, et al. Can sodium glucose cotransporter 2 (SGLT-2) inhibitors be beneficial in patients with acute myocardial infarction? Kardiol Pol. 2021;1866(7):165770. doi: https://doi.org/10.33963/KP.15969
52. Levine JA, Karam SL, Aleppo G. SGLT2-I in the Hospital Setting: Diabetic Ketoacidosis and Other Benefits and Concerns. Curr Diab Rep. 2017;17(7):54. doi: https://doi.org/10.1007/s11892-017-0874-3
Об авторах
В. В. СалуховРоссия
Салухов Владимир Владимирович, доктор медицинских наук
194044, г. Санкт-Петербург, ул. Академика Лебедева, д. 6
eLibrary SPIN: 4531-6011
Г. Р. Галстян
Россия
Галстян Гагик Радикович, доктор медицинских наук, профессор
Москва
eLibrary SPIN: 9815-7509
Т. С. Ильинская
Россия
Ильинская Татьяна Александровна, кандидат медицинских наук
Санкт-Петербург
eLibrary SPIN: 5734-7868
Дополнительные файлы
|
|
1. Рисунок 1. Механизмы, лежащие в основе диабетического эугликемического кетоацидоза на фоне приема ингибиторов натрий-глюкозного котранспортера 2 типа. Адаптировано из [29]. Примечание. СЖК - свободные жирные кислоты. иSGLT2 - ингибиторы натрий-глюкозного котранспортера 2 типа | |
| Тема | ||
| Тип | Исследовательские инструменты | |
Посмотреть
(290KB)
|
Метаданные ▾ | |
|
|
2. Рисунок 2. Алгоритм коррекции сахароснижающей терапии при назначении ингибитора натрий-глюкозного котранспортера 2 типа. Адаптировано из [43]. | |
| Тема | ||
| Тип | Исследовательские инструменты | |
Посмотреть
(346KB)
|
Метаданные ▾ | |
|
|
3. Рисунок 3. Общие рекомендации по старту терапии ингибиторами натрий-глюкозного котранспортера 2 типа у пациентов с сахарным диабетом 2 типа и атеросклеротическими сердечно-сосудистыми заболеваниями в стационаре. Адаптировано из [47]. Примечание. ЭуДКА — диабетический эугликемический кетоацидоз. НПВП — нестереоидные противовоспалительные препараты. рСКФ —расчетная скорость клубочковой фильтрации. АД — артериальное давление. САД — систолическое артериальное давление. ДАД — диастолическое артериальное давление. иSGLT2 — ингибиторы натрий-глюкозного котранспортера 2 типа. | |
| Тема | ||
| Тип | Исследовательские инструменты | |
Посмотреть
(367KB)
|
Метаданные ▾ | |
Рецензия
Для цитирования:
Салухов В.В., Галстян Г.Р., Ильинская Т.С. Практические аспекты инициации и применения ингибиторов SGLT2 в стационаре и на амбулаторном этапе. Сахарный диабет. 2022;25(3):275-287. https://doi.org/10.14341/DM12855
For citation:
Salukhov V.V., Galstyan G.R., Ilyinskay T.A. Practical aspects of initiation and use of SGLT2 inhibitors: inpatient and outpatient perspectives. Diabetes mellitus. 2022;25(3):275-287. (In Russ.) https://doi.org/10.14341/DM12855
JATS XML

Контент доступен под лицензией Creative Commons Attribution-NonCommercial-NoDerivatives 4.0 International License (CC BY-NC-ND 4.0).















































