Перейти к:
Перспективы комбинированного применения современных препаратов для кардионефропротекции у пациентов с сахарным диабетом 2 типа и хронической болезнью почек
https://doi.org/10.14341/DM13113
Аннотация
Хроническая болезнь почек (ХБП) — частое осложнение сахарного диабета (СД), которое значительно увеличивает сердечно-сосудистый риск, приводит к снижению качества жизни пациентов и, безусловно, требует лечения. В последние годы парадигма лечения СД 2 типа (СД2) сместилась с глюкозоцентрического подхода в сторону болезнь-модифицирующей терапии; все большее внимание уделяется кардионефропротекции пациентов. В терапии ХБП у пациентов с СД2 широко применяются препараты, влияющие на ренин-ангиотензин-альдостероновую систему, а также ингибиторы натрий-глюкозных котранспортеров 2 типа (иНГЛТ2). Несмотря на доказанное положительное влияние данных препаратов в отношении сохранности почечных функций, в патогенезе ХБП присутствуют еще не охваченные терапией звенья. В частности, потенциальной мишенью для нефропротективных препаратов могут быть процессы фиброзирования в паренхиме почек, активность которых у пациентов с ХБП выше в связи с увеличением экспрессии минеракортикоидных рецепторов. Таким образом, на резидуальный риск прогрессирования ХБП могут влиять антагонисты минеракортикоидных рецепторов (АМКР). В частности, эффективность нестероидного селективного АМКР финеренон была определена рядом крупных клинических исследований, что подтвердило его нефропротективный потенциал. В связи с этим особую актуальность приобретают исследования, направленные на изучение совместного действия известных нефропротективных препаратов, а также их сочетанное влияние на сердечно-сосудистый риск.
В данном обзоре приведены основные механизмы сочетанного действия иНГЛТ2 и финеренона, а также обсуждаются результаты исследований, посвященных комбинированному применению стандартной нефропротективной терапии, иНГЛТ2 и финеренона, с точки зрения дополнительных преимуществ кардионефропротекции.
Ключевые слова
Для цитирования:
Халимов Ю.Ш., Семикова Г.В., Шутова Ю.А. Перспективы комбинированного применения современных препаратов для кардионефропротекции у пациентов с сахарным диабетом 2 типа и хронической болезнью почек. Сахарный диабет. 2024;27(1):93-103. https://doi.org/10.14341/DM13113
For citation:
Khalimov Yu.Sh., Semikova G.V., Shutova Yu.A. Novel cardioprotective and nephroprotective combination in patients with type 2 diabetes and chronic kidney disease: perspectives of use. Diabetes mellitus. 2024;27(1):93-103. (In Russ.) https://doi.org/10.14341/DM13113
ВВЕДЕНИЕ
С момента первого описания клинической картины (СД) (согласно историческим документам, в 1552 г. до н.э.) прошло более трех тысяч лет до осознания пагубного воздействия хронической глюкозурии на функцию почек и описания осложнений «сахарного мочеизнурения». На сегодняшний день не вызывает сомнения, что СД неизбежно приводит к прогрессирующему повреждению почечной паренхимы и развитию хронической болезни почек (ХБП), а диабетическая нефропатия является ведущей причиной развития терминальной почечной недостаточности (ТПН) [1][2]. Данные проспективных наблюдательных исследований позволяют предположить, что развитие хронического повреждения почек в условиях гипергликемии начинается существенно раньше, чем пациенту диагностируется СД 2 типа (СД2) с неуклонным прогрессированием патологического процесса. Так, в момент постановки диагноза СД2 у 20% пациентов уже имеются признаки ХБП, через 15 лет наблюдения альбуминурия диагностируется уже у половины (52%) пациентов, а расчетная скорость клубочковой фильтрации (рСКФ) менее 60 мл/мин/1,73 м² выявляется почти у трети пациентов (28%) [3]. Распространенность ХБП при СД2 зависит от уровня диагностики и может превышать 56% [4][5]. Согласно отечественным данным, в ходе активного скрининга ХБП выявляется у 40% пациентов с СД2 [6][7]. Поскольку ХБП при СД2 ассоциирована с повышением кардиоренальных рисков и высоким уровнем смертности, не вызывает сомнений необходимость ежегодного рутинного скрининга ХБП (оценка альбуминурии и рСКФ) [8]. ХБП, особенно ее терминальная стадия, представляет собой социально-экономическое бремя для пациентов и системы здравоохранения. В связи с этим меры, направленные на профилактику, своевременное выявление и предотвращение прогрессирования этого заболевания, приобретают особую актуальность [9].
Лечение ХБП у пациентов с СД2 основано на модификации образа жизни (в частности снижении массы тела до оптимальных значений), достижении целевых значений липидного спектра и глюкозы плазмы, а также поддержании целевого артериального давления (АД). В качестве фармакологических агентов традиционно используются ингибиторы ангиотензин-превращающего фермента (иАПФ) или блокаторы рецепторов к ангиотензину II (БРА). Кроме того, в последние годы стали известны благоприятные эффекты ингибиторов натрий-глюкозных ко-транспортеров 2 типа (иНГЛТ-2), что также способствует снижению кардиоренального риска у пациентов с СД2 [10][11]. Тем не менее, остаточный риск прогрессирования ХБП и неблагоприятных сердечно-сосудистых исходов у лиц с СД2 остается достаточно высоким, что делает необходимым поиск новых терапевтических подходов, направленных на коррекцию не задействованных ранее патофизиологических путей прогрессирования ХБП [11]. Так, известно, что у пациентов с СД2 процессы воспаления и фиброзирования в почках и сердце во многом обусловлены гиперактивацией минералкортикоидных рецепторов (МКР), что послужило основой для разработки нового класса препаратов — нестероидных антагонистов МКР (нсАМКР) [12]. В настоящее время финеренон является основным препаратом данной группы, достоверно способствующим замедлению темпов прогрессирования ХБП и снижению сердечно-сосудистого риска у пациентов с СД2 за счет своего противовоспалительного и антифибротического действия. Благоприятные профили эффективности и безопасности в рандомизированных клинических исследованиях (РКИ) FIDELIO, FIGARO и объединенном анализе FIDELITY стали основанием для одобрения его применения с целью кардионефропротекции у пациентов с ХБП и СД2 в странах Европы, Америке, Индии, Китае, Японии и Российской Федерации [13].
Благоприятные эффекты финеренона были отмечены в последних обновлениях клинических рекомендаций эндокринологов, нефрологов и кардиологов с наивысшим уровнем доказательств, наравне с иНГЛТ-2. В отношении терапии ХБП это стало основанием для перехода от традиционного «последовательного» назначения препаратов к новой парадигме многофакторной терапии, согласно которой финеренон является обязательным компонентом кардионефропротективной терапии ХБП при СД2. Важным представляется определить потенциал и целесообразность совместного назначения финеренона с другими компонентами базовой кардионефропротективной терапии, включая иНГЛТ-2 [11–14].
ПАТОФИЗИОЛОГИЧЕСКИЕ АСПЕКТЫ НЕФРОПРОТЕКТИВНОГО ДЕЙСТВИЯ ИНГИБИТОРОВ НАТРИЙ-ГЛЮКОЗНОГО КОТРАНСПОРТЕРА-2 И НЕСТЕРОИДНЫХ АГОНИСТОВ МИНЕРАЛОКОРТИКОИДНЫХ РЕЦЕПТОРОВ
В основе многофакторной терапии лежит патогенетически обоснованное воздействие на прогноз заболевания. В частности, развитию и прогрессированию ХБП у пациентов с СД2 способствуют метаболические и гемодинамические нарушения, на которые прицельно влияют иАПФ/БРА и иНГЛТ-2. Несмотря на изученные положительные свойства, препараты данных классов лишь в малой степени влияют на компоненты воспаления и фиброз, которые играют важную роль в поражении органов-мишеней при СД2 [15].
ХБП при СД2 характеризуется процессами повреждения практически во всех элементах паренхимы почек: клубочках, канальцах, интерстиции, а также в сосудистом русле. Микроскопически это проявляется нарастающей экспансией внеклеточного матрикса, гломерулосклерозом, гиалинозом сосудов, усилением интерстициального фиброза и атрофией почечных канальцев, что приводит к снижению и утрате почечных функций с развитием прогрессирующей ХБП вплоть до ТПН [16]. Реабсорбция глюкозы в почечных канальцах является важным физиологическим механизмом, препятствующим потере важнейшего энергетического субстрата. Известно, что НГЛТ-2, расположенные преимущественно на мембране клеток в проксимальном отделе почечных канальцев, отвечают за реабсорбцию до 80–90% глюкозы из первичной мочи. У пациентов с СД2 из-за повышения концентрации глюкозы в моче увеличивается активность НГЛТ-2, что приводит к усилению реабсорбции глюкозы совместно с натрием. При этом концентрация натрия в области macula densa (плотного пятна) снижается, что влечет за собой вазодилатацию приносящих артериол и, как следствие, клубочковую гиперфильтрацию. Влияние на данный компонент патогенеза лежит в основе действия иНГЛТ-2: за счет своего специфического действия они снижают реабсорбцию натрия и глюкозы в проксимальных канальцах. В свою очередь это приводит к снижению внутриклубочковой гипертензии и уменьшению альбуминурии [17]. Доказано, что иНГЛТ2 обладают кардиопротективным и нефропротективным эффектом; кроме того, у пациентов с рСКФ >45 мл/мин/1,73 м² назначение иНГЛТ-2 способствует кетогенезу, снижению массы тела и АД и повышению чувствительности тканей к инсулину [18][19].
В отличие от НГЛТ-2, МКР экспрессируются во многих органах и тканях, включая мезангиальные клетки почек, подоциты, эндотелиальные клетки сосудов, миелоидные клетки, кардиомиоциты и гладкомышечные клетки. Широкое рецепторное поле определяет многообразие эффектов минералкортикоидов: от регуляции водно-электролитного баланса до модулирования системного воспаления, оксидативного стресса и фиброза [20]. У пациентов с ХБП и СД2 гиперактивация МКР приводит к увеличению продукции медиаторов воспаления и фиброза — ингибитора активатора плазминогена-1, трансформирующего фактора роста-β, фибронектина, тканевых ингибиторов матриксных металлопротеиназ и др. В почках результатом повышения активности МКР могут стать фиброз, гломерулосклероз, снижение рСКФ, протеинурия, тубулоинтерстициальные повреждения; в сердце — гипертрофия миокарда, фиброз, воспаление и оксидативный стресс; а в сосудах — эндотелиальная дисфункция, ремоделирование и повышение сосудистой жесткости. Финеренон, являясь селективным нсАМКР, способен существенно снизить выраженность данных нарушений [20]. Эффекты нсАМКР в отношении ХБП у пациентов с СД2 можно условно разделить на «ранние» и «отсроченные». «Ранние» эффекты, наблюдаемые в первые дни и недели после инициации терапии нсАМКР, обусловлены снижением экспрессии Na-каналов и Na/K-АТФазы в дистальных канальцах нефрона, в результате чего уменьшается реабсорбция Na и внутриклубочковое давление. Клинически это проявляется снижением альбуминурии и некоторым гипотензивным эффектом. Данный механизм может дополнять схожий эффект иНГЛТ-2, реализуемый в проксимальных канальцах. «Отсроченные» эффекты включают в себя снижение выраженности окислительного стресса и воспаления, а также улучшение функции эндотелия [21][22].
Кардионефропротективные эффекты терапии иНГЛТ-2 неоднократно доказаны; для финеренона также достоверно установлены положительные эффекты на течение ХБП. С учетом того, что иНГЛТ2 и нсАМКР имеют различные точки приложения в патогенезе ХБП и взаимно дополняют друг друга по своему механизму действия, их комбинированное применение может позволить получить ряд дополнительных клинических преимуществ (рис. 1) [22].
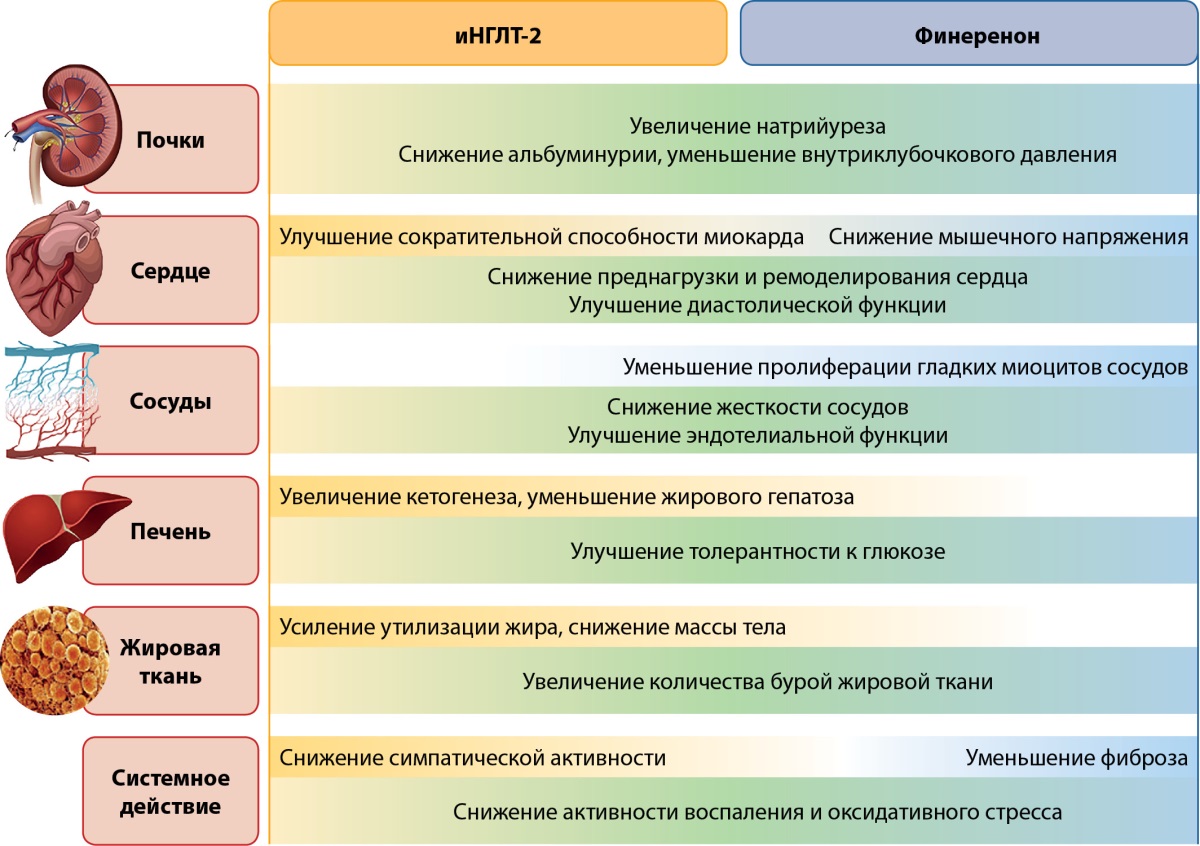
Рисунок 1. Комплементарные механизмы действия
ингибиторов натрий-глюкозных ко-транспортеров 2 типа и финеренона.
Примечание. иНГЛТ2 — ингибиторы натрий-глюкозных котранспортеров 2 типа.
Протективный эффект применения иНГЛТ-2 и финеренона представлен в ряде клинических исследований. В частности, применение иНГЛТ-2 (канаглифлозина) в исследовании CREDENCE способствовало снижению риска комбинированной конечной точки (почечные и сердечно-сосудистые неблагоприятные события) на 30% [23]. В исследовании FIDELIO было выявлено протективное действие нсАМКР (финеренон) в отношении неблагоприятных почечных и сердечно-сосудистых исходов — применение финеренона способствовало снижению риска на 18% прогрессирования ХБП и снижению на 14% риска развития сердечно-сосудистых событий [21]. Поскольку сердечно-сосудистые исходы у пациентов с СД2 наблюдаются чаще, чем почечные, прямое сравнение результатов данных исследований не позволяет сделать вывод о более выраженном протективном эффекте иНГЛТ-2 или финеренона — для этого необходимо оценивать препараты в исследовании с одинаковым дизайном и конечными точками. Agarwal R. с соавт. выполнили данную работу и произвели поэтапную корректировку основных отличий в дизайнах FIDELIO и CREDENCE, что позволило оценить сравнительную эффективность терапии финереноном и канаглифлозином. Исследователи выделили подгруппу пациентов FIDELIO, которые соответствовали критериям включения CREDENCE и в данной подгруппе оценили достижение кардиоренальных конечных точек (время до развития ТПН, устойчивого снижения рСКФ на ≥57%, смерти от почечных причин, смерти от сердечно-сосудистых причин). По результатам проведенного анализа, финеренон значимо снижал риск описанных конечных точек на 26% по сравнению с плацебо. Кроме того, при поправке на различия в доле пациентов с сердечной недостаточностью (7,6% в FIDELIO, 14,8% в CREDENCE) эффект финеренона в отношении снижения риска событий комбинированной кардиоренальной конечной точки составил 28%, что сопоставимо с эффектом канаглифлозина в исследовании CREDENCE — 30% по сравнению с плацебо (рис. 2) [24]. Учитывая вышесказанное, назначение комбинированной терапии равнозначными по выраженности эффектов препаратами потенциально способно значимо снизить кардиоренальные риски у пациентов с СД2 и ХБП, благодаря их влиянию на разные звенья патогенеза хронических осложнений СД2.
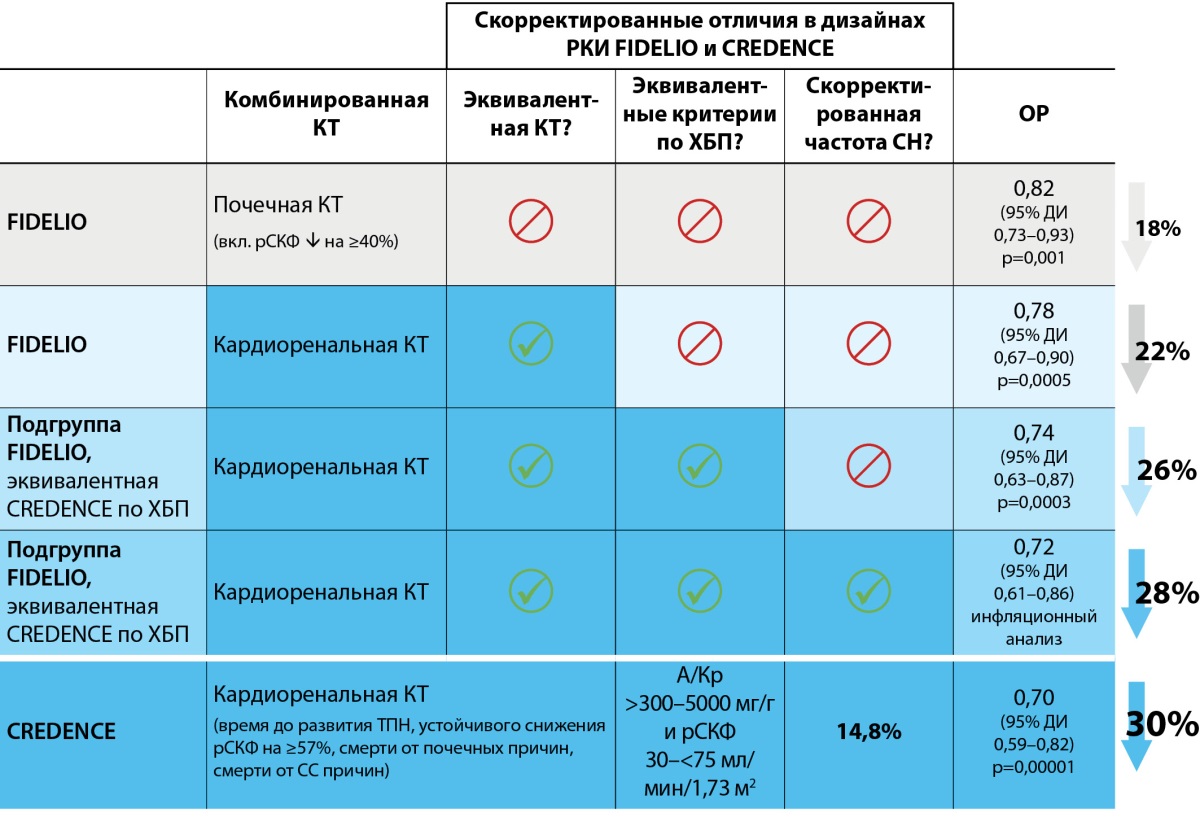
Рисунок 2. Сравнительный анализ результатов FIDELIO и CREDENCE
после корректировки основных различий. Адаптировано из [24].
Примечание. КТ — конечная точка, ХБП — хроническая болезнь почек,
рСКФ — расчетная скорость клубочковой фильтрации,
А/Кр — соотношение альбумина и креатинина мочи,
ДИ — доверительный интервал.
ДОКЛИНИЧЕСКИЕ И КЛИНИЧЕСКИЕ ИССЛЕДОВАНИЯ СОВМЕСТНОГО ПРИМЕНЕНИЯ ИНГЛТ2 И ФИНЕРЕНОНА
Впервые преимущество совместного применения финеренона и иНГЛТ-2 по сравнению с монотерапией было продемонстрировано в доклинических исследованиях. В экспериментальной работе Kolkhof P. на крысах была смоделирована типичная картина развития и прогрессирования артериальной гипертензии и эндотелиальной дисфункции с последующим повреждением органов-мишеней (включая гипертрофию левого желудочка сердца и гломерулосклероз). Все животные получали иАПФ (каптоприл). Далее крыс разделили на группы: плацебо, получавших эмпаглифлозин (3 и 10 мг/кг), финеренон (1 и 3 мг/кг) и комбинированную терапию (эмпаглифлозин 3 мг/кг + финеренон 1 мг/кг). Помимо смертности, у животных оценивали АД, выраженность протеинурии, уровень креатинина и мочевой кислоты плазмы, выраженность фибротических процессов в сердечно-сосудистой системе и почках. Согласно результатам, дозозависимый кардио- и нефропротективный эффект был выявлен и у финеренона, и у эмпаглифлозина, однако у их комбинации по сравнению с монотерапией был более выраженный эффект (рис. 3) [25]. Несмотря на то, что данные результаты были получены в доклинических условиях и еще не были подтверждены в крупных многоцентровых исследованиях на людях, они стали первым доказательством синергического действия финеренона и эмпаглифлозина.
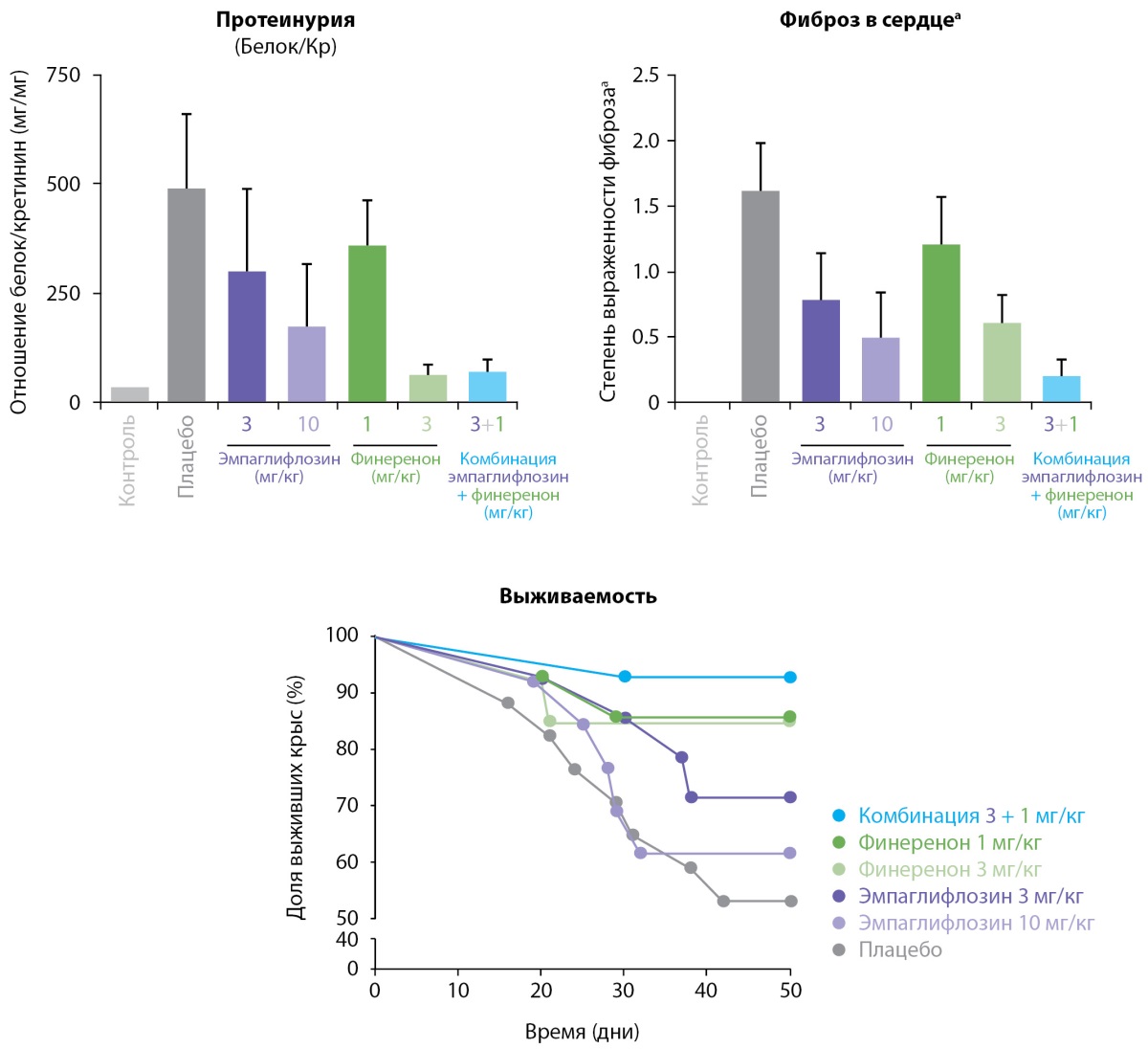
Рисунок 3. Эффекты терапии финереноном
и ингибиторами натрий-глюкозных ко-транспортеров 2 типа
в доклинических испытаниях. Адаптировано из [25].
Примечание. а — полуколичественная оценка;
1 степень соответствует минимальной/низкой степени выраженности;
2 степень — небольшая выраженность;
3 степень — умеренная;
4 степень — явные/выраженные изменения.
Первым клиническим подтверждением потенциала эффективной и безопасной терапии при совместном применении финеренона и иНГЛТ-2 стали результаты III фазы исследования FIDELITY, представляющего собой объединенный анализ двух комплементарных по дизайну и методологии РКИ: FIGARO и FIDELIO [13]. В рамках данных РКИ были получены убедительные доказательства кардионефропротективных эффектов финеренона и его благоприятного профиля безопасности в широкой популяции пациентов с ХБП С1-4 и СД2 [13]. Важно отметить, что по дизайну данных РКИ все пациенты получали максимально переносимые дозы иАПФ/БРА, что позволило оценить независимые эффекты финеренона в дополнение к стандартной терапии. В свою очередь исследование FIDELITY (n=13 026) основано на том, что по протоколу FIGARO и FIDELIO назначение иНГЛТ-2 не ограничивалось: еще до рандомизации 877 пациентов (6,7%) получали иНГЛТ-2, а у 1113 (8,5%) терапия иНГЛТ-2 была инициирована в ходе исследования. Единовременную терапию иНГЛТ-2 и финеренон получали 958 пациентов (14,7%). В ходе анализа данной подгруппы оценивалась выраженность эффектов финеренона в зависимости от исходной терапии иНГЛТ-2 в отношении сердечно-сосудистых и почечных конечных точек. Период наблюдения эффектов терапии в отношении конечных точек составил 3 года. В полученных результатах прослеживался тренд к более выраженному снижению риска событий на фоне комбинированной терапии финереноном и иНГЛТ2, однако различия были статистически не значимыми, что требует дальнейшего изучения на более многочисленной группе пациентов и при более длительном наблюдении (рис. 4) [26]. Вместе с тем финеренон продемонстрировал выраженное снижение частоты сердечно-сосудистых и почечных событий независимо от исходной терапии иНГЛТ-2, что подтверждает его независимый вклад в снижение сердечно-сосудистых и почечных рисков у пациентов с ХБП и СД2. Полученные результаты позволили включить финеренон в класс болезнь-модифицирующих препаратов наряду с иНГЛТ2.
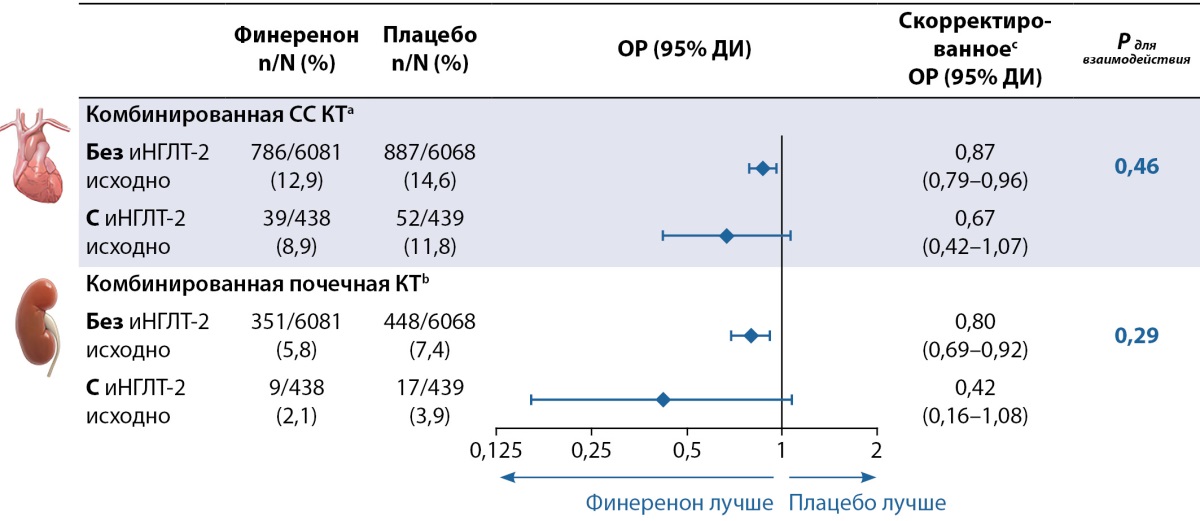
Рисунок 4. Кардионефропротективный эффект финеренона
в зависимости от исходной терапии
ингибиторами натрий-глюкозных ко-транспортеров 2 типа.
Адаптировано из [26].
Примечание. а — комбинированная сердечно-сосудистая конечная точка:
время до смерти от сердечно-сосудистых причин, нефатального инфаркта миокарда,
нефатального инсульта или госпитализации по причине сердечной недостаточности;
b — комбинированная почечная конечная точка:
время до развития терминальной почечной недостаточности,
устойчивого снижения рСКФ на ≥57% от исходного уровня, смерти от почечных причин;
c — скорректированное по уровню гликированного гемоглобина,
систолическому артериальному давлению, исходному А/Кр, исходной рСКФ;
ОР — отношение рисков; ДИ — доверительный интервал;
иНГЛТ-2 — ингибиторы натрий-глюкозных ко-транспортеров 2 типа.
Особое значение имеют результаты, касающиеся профиля безопасности, поскольку пациенты с нарушенной функцией почек находятся в зоне высокого риска развития гиперкалиемии. В исследовании FIDELITY гиперкалиемия более 6 ммоль/л реже развивалась у пациентов, получавших комбинированную терапию финереноном и иНГЛТ-2 по сравнению с пациентами, не получавшими иНГЛТ-2. Полученные результаты позволяют сделать предположение, что комбинация иНГЛТ-2 и финеренона может способствовать минимизации рисков нежелательных явлений в ходе лечения ХБП у пациентов с СД2 [26]. В пользу безопасного совместного применения двух разных классов лекарственных препаратов говорят также результаты подгруппового анализа РКИ DAPA-CKD, согласно которому меньшая частота случаев гиперкалиемии наблюдалась у пациентов, единовременно получавших иНГЛТ-2 и стероидные АМКР [27].
Целью комбинированной болезнь-модифицирующей терапии у пациентов с СД2 и ХБП является продление качественной жизни пациента без развития сердечно-сосудистых или почечных событий. Heerspink HJL с соавт. оценивали благоприятные эффекты комбинированной терапии финереноном и иНГЛТ-2 в дополнение к стандартной терапии (иАПФ/БРА) в отношении больших почечных событий (удвоение сывороточного креатинина, ТПН, смерть от почечных причин) в популяции пациентов с ХБП и СД2. Исследователями был проведен анализ трех крупных РКИ: CREDENCE, DAPA-CKD, FIDELIO-DKD [28]. Согласно результатам анализа, комбинированная болезнь-модифицирующая терапия (финеренон+иНГЛТ-2) в дополнение к иАПФ/БРА характеризовалась дополнительным снижением риска почечных событий на 50%, ТПН на 41% (ОР=0,59; 95% ДИ 0,51–0,69), госпитализации по поводу сердечной недостаточности (ГСН) на 48% (ОР=0,52; 95% ДИ 0,44–0,63), смерти от всех причин на 25% (ОР=0,75; 95% ДИ 0,65–0,86) по сравнению со стандартной терапией иАПФ/БРА (рис. 5). Авторы подчеркивают необходимость как можно более раннего назначения комбинации финеренона и иНГЛТ-2 в связи с ее влиянием на продолжительность жизни: у пациентов в возрасте 50 лет назначение комбинированной терапии сопровождалось пролонгацией жизни на 6,7 года без больших почечных событий (95% ДИ 5,5–7,9), на 4,8 года без ТПН (95% ДИ 3,5–6,0) и на 3,1 года без ГСН (95% ДИ 2,3–3,7). Схожие преимущества при назначении комбинированной болезнь-модифицирующей терапии могут получить пациенты в условиях реальной клинической практики: назначение комбинации иНГЛТ-2+финеренон в дополнение к иАПФ/БРА у пациентов с СД2 и ХБП с рСКФ 25–75 мл/мин/1,73 м²) сопровождалось увеличением продолжительности жизни без почечных событий на 6,3 года (95% ДИ 5,2–7,3). Преимущества комбинированной терапии перед иАПФ/БРА сохранялись даже в условиях худшей приверженности [28].
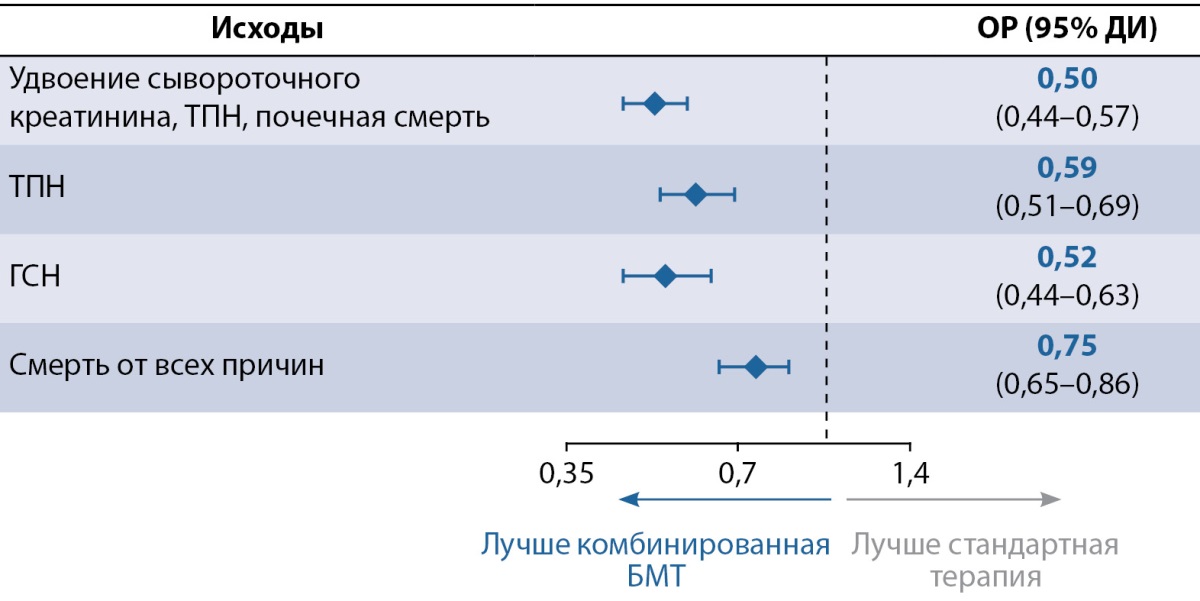
Рисунок 5. Эффекты комбинированной болезнь-модифицирующей терапии
хронической болезни почек (ингибиторы натрий-глюкозных ко-транспортеров 2 типа
+финеренон+ингибиторы ангиотензин-превращающего фермента (иАПФ)
или блокаторы рецепторов к ангиотензину II)
по сравнению со стандартной терапией
ингибиторами ангиотензин-превращающего фермента (иАПФ)
или блокаторами рецепторов к ангиотензину II по ключевым конечным точкам.
Адаптировано из [28].
Примечание. ТПН — терминальная почечная недостаточность,
ГСН — госпитализация по поводу сердечной недостаточности,
ОР — отношение рисков, ДИ — доверительный интервал.
Еще больший кардионефропротективный потенциал может иметь комбинация четырех классов болезнь-модифицирующей терапии (иНГЛТ-2, агонисты рецепторов глюкагоноподобного пептида 1 (арГПП-1) и финеренон в дополнение к иАПФ/БРА), поскольку данные группы препаратов воздействуют на разные патофизиологические звенья прогрессирования ХБП: метаболические нарушения, гемодинамические отклонения, воспаление и фиброз. Так, первичным механизмом, определяющим клинические эффекты препаратов класса иНГЛТ-2, считается их влияние на метаболические и гемодинамические нарушения, в отношении арГПП-1 на первый план выходят их метаболические эффекты, при этом в основе действия нсАМКР, помимо прочих эффектов, лежит способность подавлять не охваченные другими препаратами процессы воспаления и фиброза [29][30]. Neuen B.L. с соавт. провели анализ, который объединяет результаты 14 крупных РКИ III фазы по применению иНГЛТ-2, нсАМКР, арГПП-1 с участием более 87 тысяч пациентов с ХБП и СД2 в отношении NNT (Number Needed to Treat — число пациентов, которых необходимо лечить в течение определенного периода, чтобы избежать любого события конечной точки). В частности, в рамках данного анализа оценивали выживаемость без больших неблагоприятных сердечно-сосудистых событий (MACE: нефатальный инфаркт, нефатальный инсульт, смерть от сердечно-сосудистых причин), без прогрессирования ХБП (удвоение сывороточного креатинина, ТПН, смерть от почечных причин), без ГСН, смерти от сердечно-сосудистых причин, смерти по любой причине. Согласно полученным результатам, комбинированная терапия (иНГЛТ-2, финеренон, арГПП-1) сопровождалась снижением риска по всем конечным точкам, включая снижение риска MACE на 35%, а также повышением выживаемости пациентов без указанных событий по любой конечной точке. Полученные результаты подтверждают значимость многофакторного подхода в лечении ХБП у пациентов с СД2, основанного на синергии эффектов разных классов лекарственных препаратов [30]. Схожий многофакторный подход (квадротерапия как базовая терапия) уже давно применяется в лечении сердечной недостаточности с низкой фракцией выброса и может иметь большой потенциал в лечении ХБП при СД2 [31].
Несмотря на то, что финеренон является относительно новым препаратом в лечении пациентов с СД2 и ХБП, он был одобрен к применению FDA (Food and Drug Administration) в июле 2021 г. и EMA (European Medicines Agency) в феврале 2022 г. и уже активно применяется. Понимание целесообразности раннего назначения финеренона позволяет оценивать результаты многофакторной болезнь-модифицирующей терапии у пациентов с СД2 и ХБП в реальной клинической практике, а также подтвердить их в долгосрочной перспективе [32][33][34]. Как правило, врачи назначают финеренон пациентам с ХБП и СД2 в дополнение к иАПФ/БРА, что отражает положение финеренона в актуальных клинических рекомендациях: его применение рекомендовано в дополнение к иАПФ/БРА независимо от назначения иНГЛТ2 с целью снижения сердечно-сосудистых и почечных рисков у пациентов с СД2 и ХБП с альбуминурией [34]. На конгрессе ASN 2023 (American Society of Nephrology) были представлены промежуточные результаты FINE-REAL — первого проспективного наблюдательного исследования, нацеленного на изучение эффектов применения финеренона в рутинной практике. Согласно результатам промежуточного анализа (n=504), 47% пациентов в исследовании FINE-REAL одновременно получали финеренон и иНГЛТ-2. Частота случаев гиперкалиемии в условиях реальной клинической практики была невысокой: у 21 (4,2%) пациента уровень калия был более 5,5 ммоль/л, лишь у 2 (0,4%) пациентов — более 6 ммоль/л. При этом за 7 месяцев наблюдения не отмечено ни одного случая гиперкалиемии, потребовавшего госпитализации или проведения гемодиализа. Полученные результаты соответствуют профилю безопасности, который финеренон продемонстрировал в исследовании FIDELITY [13][34].
МЕСТО ФИНЕРЕНОНА В КЛИНИЧЕСКИХ РЕКОМЕНДАЦИЯХ
Лекарственная терапия СД2 традиционно представляет собой поэтапное назначение последующих классов в зависимости от эффективности лечения и качества жизни пациентов. Подобный подход подразумевает наличие определенного «периода ожидания», что не всегда является оптимальным для пациентов с хроническим прогрессирующим заболеванием. В связи с этим в обновленных клинических рекомендациях подчеркивается, что многофакторная кардионефропротективная терапия, нацеленная на минимизацию рисков у пациентов с ХБП и СД2, заключается в необходимости назначения полного перечня препаратов, воздействующих на основные факторы риска и патофизиологические механизмы развития и прогрессирования осложнений СД: контроль гликемии, АД и липидного обмена, а также органы-мишени: сердце, почки и головной мозг. Таким образом, после регистрации в Европе и США финеренон последовательно был включен в обновленные клинические рекомендации с наивысшим уровнем доказательств (А) для применения с целью кардионефропротекции у пациентов с ХБП и СД2 (табл. 1). Основным принципом нефропротекции у пациентов с СД2 и ХБП в настоящее время является совокупное назначение трех классов «болезнь-модифицирующих» препаратов (иАПФ/БРА, иНГЛТ-2, финеренон) [35–41].
Таблица 1. Место финеренона в актуальных клинических рекомендациях
|
Название руководства |
Дата обновления |
Позиция финеренона в КР |
|
Научное заявление AHA [35] |
март 2022 г. |
Наряду с иНГЛТ-2 и арГПП-1 отмечена важность результатов FIDELIO и ценность финеренона для замедления темпов прогрессирования ХБП на фоне СД2 |
|
Рекомендации AACE [36] |
27 сентября 2022 г. |
«Нестероидный АМКР (финеренон) с доказанными благоприятными почечными и СС-эффектами рекомендован пациентам с СД2, рСКФ≥25 мл/мин/1,73 м², нормальной [K+] крови и альбуминурией (≥30 мг/г [ ≥3 мг/ммоль]), несмотря на максимально переносимую дозу ингибиторов РААС» (А1) |
|
Консенсус |
3 октября 2022 г. |
«нсАМКР с доказанными благоприятными почечными и сердечно-сосудистыми эффектами рекомендован пациентам с СД2, рСКФ≥25 мл/мин/1,73 м², нормальной [K+] и альбуминурией (А/Кр≥30 мг/г), несмотря на максимально переносимую дозу ингибиторов РААС» |
|
Рекомендации KDIGO [37] |
19 октября 2022 г. |
«Пациентам с СД2, рСКФ≥ 25 мл/мин/1,73 м², нормальной [K+] крови и альбуминурией (≥ 30 мг/г), несмотря на максимально переносимую дозу блокаторов РААС, рекомендуется рассмотреть назначение нестероидного АМКР с доказанными кардио- и нефропротективными эффектами» (2А) |
|
Рекомендации ADA-2023 г. [38] |
12 декабря 2022 г. |
Раздел №10 по контролю СС рисков: 10.43. «Пациентам с СД2 и ХБП с альбуминурией, получающим иАПФ или БРА в максимально переносимых дозировках, рекомендуется назначить финеренон с целью улучшения сердечно-сосудистых исходов и замедления темпов прогрессирования ХБП» (А) |
|
Раздел №11 по контролю почечных рисков: 11.5c. «Пациентам с СД2 и ДБП рассмотреть назначение иНГЛТ-2 (при рСКФ ≥20 мл/мин/1,73 м²), арГПП-1 или нестероидного АМКР (при рСКФ≥25 мл/мин/1,73 м²) дополнительно с целью снижения сердечно-сосудистых рисков» (А) |
||
|
11. Раздел по контролю почечных рисков: 11.5d. «Пациентам с ХБП и альбуминурией с повышенным риском сердечно-сосудистых событий и прогрессирования ХБП рекомендован нестероидный АМКР (с доказанным в клинических исследованиях профилем эффективности) для замедления темпов прогрессирования ХБП и снижения риска СС событий» (А) |
||
|
Алгоритмы медицинской помощи больным СД (2023 г.) [8] |
май 2023 г. |
«Нестероидный антагонист минералокортикоидных рецепторов финеренон, показавший снижение риска прогрессирования ХБП и развития кардиоваскулярных событий, рекомендуется пациентам с СД2, рСКФ≥25 мл/мин/1,73 м², нормальной концентрацией калия в сыворотке и альбуминурией (А/Кр≥30 мг/г), несмотря на максимально переносимую дозу ингибиторов РААС» |
|
Рекомендации по АГ European Society of Hypertension [39] |
21 июня 2023 г. |
Раздел 18. СД и АГ: «нсАМКР финеренон может быть назначен благодаря своим кардионефропротективным эффектам пациентам с ХБП на фоне сахарного диабета с умеренной или тяжелой альбуминурией. Финеренон также обладает гипотензивным эффектом» (1А) |
|
Раздел 19. ХБП и АГ: «нсАМКР финеренон рекомендован пациентам с ХБП и альбуминурией на фоне СД2 при рСКФ≥25 мл/мин/1,73 м² и при концентрации калия в сыворотке крови <5,0 ммоль/л» (1А) |
||
|
Практическое руководство European Renal Best Practice ERA 2023 г. [40] |
24 июня 2023 г. |
«Финеренон должен быть назначен с целью кардионефропротекции в дополнение к иАПФ/БРА в максимально переносимых дозах и независимо от применения иНГЛТ2 у пациентов с ХБП и СД2 при рСКФ>25 мл/мин/1,73 м², умеренной или выраженной альбуминурии и концентрации К<4,8 ммоль/л» |
|
Рекомендации ESC-2023 г. по диагностике и лечению СН [41] |
25 августа 2023 г. |
У пациентов с СД2 и ХБП финеренон рекомендован для снижения риска ГСН (1А) |
|
Рекомендации ESC-2023 г. по лечению ССЗ при СД [14] |
25 августа 2023 г. |
Финеренон рекомендуется в дополнение к иАПФ или БРА пациентам с СД2 и рСКФ >60 мл/мин/1,73 м² при А/Кр≥300 мг/г или рСКФ 25–60 мл/мин/1,73 м² и А/Кр≥30 мг/г для снижения риска сердечно-сосудистых событий и ТПН (1А) |
Примечание. СД — сахарный диабет;
СД2 — сахарный диабет 2 типа;
ХБП — хроническая болезнь почек;
ТПН — терминальная почечная недостаточность;
АГ — артериальная гипертензия;
ГСН — госпитализация по поводу сердечной недостаточности;
иНГЛТ-2 — ингибиторы натрий-глюкозных котранспортеров 2 типа;
арГПП-1 — агонисты рецепторов глюкагоноподобного пептида-1;
нсАМКР — нестероидные антагонисты минералкортикоидных рецепторов;
иАПФ — ингибиторы ангиотензинпревращающего фермента;
БРА — блокаторы рецепторов ангиотензина II;
рСКФ — расчетная скорость клубочковой фильтрации;
А/Кр — соотношение альбумина и креатинина мочи;
AACE — Американская ассоциация клинической эндокринологии;
ADA — Американская ассоциация диабета;
AHA — Американская кардиологическая ассоциация;
European Renal Best Practice ERA — Инициатива по лучшим практикам
в лечении заболеваний почек Европейской ассоциации нефрологов;
ESC — Европейское Общество Кардиологов;
European Society of Hypertension (ESH) —
Европейское общество по артериальной гипертензии;
KDIGO – Инициатива по улучшению глобальных исходов заболеваний почек
ПРАКТИЧЕСКИЕ РЕКОМЕНДАЦИИ
На основании данных клинических исследований и реальной клинической практики можно выделить ряд практических советов по инициации кардионефропротективной терапии финереноном и иНГЛТ-2 у пациентов с ХБП и СД2, получающих иАПФ/БРА. В целях минимизации рисков инициального снижения рСКФ и повышения уровня сывороточного креатинина рекомендовано [42][43]:
- Каждый класс препаратов назначить с интервалом не менее 1 недели для оптимизации их гемодинамического эффекта в отношении почечной функции.
- Перед инициацией терапии финереноном и иНГЛТ-2 следует временно приостановить диуретическую терапию и возобновить спустя 1 неделю при необходимости.
- Перед инициацией терапии пациентам рекомендовано пить не менее 1,5–2 л жидкости в день.
- В случае гиперкалиемии терапию ингибиторами РААС прекращать не следует, поскольку это может привести к увеличению риска неблагоприятных почечных и сердечно-сосудистых исходов. В этом случае рекомендовано рассмотреть совместное назначение диуретиков (не калийсберегающих), калий-связывающих агентов и использование других методов контроля гиперкалиемии.
ЗАКЛЮЧЕНИЕ
В данном обзоре представлены основные исследования, позволяющие оценить потенциальные преимущества комбинированной терапии двумя классами препаратов (нсАМКР (финеренон) и иНГЛТ-2) в дополнение к стандартной терапии иАПФ/БРА. ИНГЛТ-2 и финеренон имеют разные точки приложения в лечении ХБП при СД2, что может приводить к дополнительному кардионефропротективному эффекту. Результаты доклинических исследований, РКИ и данных реальной клинической практики стали основанием для смены парадигмы в лечении ХБП у пациентов с СД2. В настоящее время пациенты с СД2 и ХБП с целью кардионефропротекции должны получать комбинированную трехкомпонентную терапию, включающую иАПФ/БРА, иНГЛТ-2 и финеренон.
ДОПОЛНИТЕЛЬНАЯ ИНФОРМАЦИЯ
Конфликт интересов. Публикация подготовлена при поддержке АО «Байер». Компания «Байер» поддерживала техническую редакцию статьи. Ю.А. Шутова является сотрудником АО «Байер».
Участие авторов. Халимов Ю.Ш. — разработка концепции и дизайна, проверка критически важного интеллектуального содержания, анализ и интерпретация данных, написание текста, окончательное утверждение для публикации рукописи; Семикова Г.В. — сбор, анализ и интерпретация данных, написание текста; Шутова Ю.А. — сбор, анализ и интерпретация данных, коррекция текста.
Все авторы одобрили финальную версию статьи перед публикацией, выразили согласие нести ответственность за все аспекты публикации, подразумевающей надлежащее изучение и решение вопросов, связанных с точностью или добросовестностью любой части работы.
Список литературы
1. Cameron JS. The discovery of diabetic nephropathy: From small print to centre stage. J Nephrol. 2006:19 Suppl 10:S75-87.2006
2. Saran R, Li Y, Robinson B et al. US Renal Data System 2015 Annual Data Report: Epidemiology of Kidney Disease in the United States. Am J Kidney Dis. 2016;67(3 Suppl 1):Svii, S1-305. https://doi.org/10.1053/j.ajkd.2015.12.014
3. Bonora E, Trombetta M, Dauriz M, et al. Chronic complications in patients with newly diagnosed type 2 diabetes: prevalence and related metabolic and clinical features: the Verona Newly Diagnosed Type 2 Diabetes Study (VNDS) 9. BMJ Open Diabetes Res Care, 2020;8(1):e001549. https://doi.org/10.1136/bmjdrc-2020-001549
4. Thomas MC, Cooper ME, Zimmet P. Changing epidemiology of type 2 diabetes mellitus and associated chronic kidney disease. Nat. Rev. Nephrol. 2016;12(2):73-81. https://doi.org/10.1038/nrneph.2015.173
5. Wu B, Bell K, Stanford A, et al. Understanding CKD among patients with T2DM: prevalence, temporal trends, and treatment patterns—NHANES 2007–2012. BMJ Open Diab. Res. Care. 2016;4(1):e000154. https://doi.org/10.1136/bmjdrc-2015-000154
6. Добронравов В.А. Эпидемиология диабетической нефропатии: общие и региональные проблемы // Нефрология. — 2002. — Т. 6. — №1. — С. 16–22. https://doi.org/10.24884/1561-6274-2002-6-1-16-22
7. Дедов И.И., Шестакова М.В., Сунцов Ю.И. и др. Результаты реализации подпрограммы «Сахарный диабет» Федеральной целевой программы «Предупреждение и борьба с социально значимыми заболеваниями 2007–2012 годы» // Сахарный диабет. — 2013. — Т. 16. — №S2.— C.1–48. https://doi.org/10.14341/2072-0351-3879
8. Дедов И.И., Шестакова М.В., Майоров А.Ю. и др. Алгоритмы специализированной медицинской помощи больным сахарным диабетом (11-й выпуск) // Сахарный диабет. — 2023. — Т. 26. — №S2. — С. 1–231. https://doi.org/10.14341/DM13042
9. Шестакова М.В., Шамхалова М.Ш., Ярек-Мартынова И.Я. и др. Сахарный диабет и хроническая болезнь почек: достижения, нерешенные проблемы и перспективы лечения // Сахарный диабет. — 2011. — Т. 14. —№1. — С.81–88. https://doi.org/10.14341/2072-0351-6254
10. Wheeler DC, James J, Patel D, et al. SGLT2 inhibitors: slowing of chronic kidney disease progression in Type 2 diabetes. Diabetes Ther. 2020;11(12):2757-2774. https://doi.org/10.1007/s13300-020-00930-x
11. de Boer IH, Khunti K, Sadusky T, et al. Diabetes Management in Chronic Kidney Disease: A Consensus Report by the American Diabetes Association (ADA) and Kidney Disease: Improving Global Outcomes (KDIGO). Kidney Int. 2022;102(5):974–989, https://doi.org/10.1016/j.kint.2022.08.012
12. Шестакова М.В., Добронравов В.А., Аметов А.С. и др. Перспективы применения финеренона в российской популяции пациентов с хронической болезнью почек и сахарным диабетом 2 типа. Резолюция междисциплинарного совета экспертов // Сахарный диабет. — 2023. — Т. 26. — №5. — С. 492–499 https://doi.org/10.14341/DM13020
13. Agarwal R, Filippatos G, Pitt B, et al. Cardiovascular and kidney outcomes with finerenone in patients with type 2 diabetes and chronic kidney disease: the FIDELITY pooled analysis. Eur Heart J. 2022;43(6):474-484, https://doi.org/10.1093/eurheartj/ehab777
14. Marx N, Federici M, Schütt K, et al. 2023 ESC Guidelines for the management of cardiovascular disease in patients with diabetes. Eur Heart J. 2023;44(39):4043-4140. https://doi.org/10.1093/eurheartj/ehad192
15. Alicic RZ, Rooney MT, Tuttle KR. Diabetic kidney disease: challenges, progress, and possibilities. Clin J Am Soc Nephrol. 2017;12:2032–2045. https://doi.org/10.2215/CJN.11491116
16. Agarwal R. Pathogenesis of Diabetic Nephropathy. Chronic Kidney Disease and Type 2 Diabetes. 2021;1:2–7. https://doi.org/10.2337/db20211-2
17. Hou YC, Zheng CM, Yen TH, et al. Molecular Mechanisms of SGLT2 Inhibitor on Cardiorenal Protection. Int J Mol Sci. 2020;21(21):7833. https://doi.org/10.3390/ijms21217833
18. Lopaschuk GD, Verma S. Mechanisms of Cardiovascular Benefits of Sodium Glucose Co-Transporter 2 (SGLT2) Inhibitors. JACC Basic Transl Sci. 2020;5(6):632-644. https://doi.org/10.1016/j.jacbts.2020.02.004
19. Chertow GM, Vart P, Jongs N, et al. Effects of Dapagliflozin in Stage 4 Chronic Kidney Disease. J Am Soc Nephrol. 2021;32(9):2352-2361. https://doi.org/10.1681/ASN.2021020167
20. Epstein M. Aldosterone and mineralocorticoid receptor signaling as determinants of cardiovascular and renal injury: an extraordinary paradigm shift. Kidney Int Suppl (2011). 2022; 12(1): 1–6. https://doi.org/10.1016/j.kisu.2021.11.007
21. Салухов В.В., Шамхалова М.Ш., Дуганова А.В. Кардиоренальные эффекты финеренона и его место в терапии хронической болезни почек у пациентов с сахарным диабетом 2-го типа. Терапевтический архив. 2023;95(3):261–273. https://doi.org/10.26442/00403660.2023.03.202152
22. Kolkhof P, Lawatscheck R, Filippatos G, et al. Nonsteroidal Mineralocorticoid Receptor Antagonism by Finerenone-Translational Aspects and Clinical Perspectives across Multiple Organ Systems. Int J Mol Sci. 2022;23(16):9243, https://doi.org/10.3390/ijms23169243
23. Perkovic V, Jardine MJ, Neal B, et al. Canagliflozin and Renal Outcomes in Type 2 Diabetes and Nephropathy. 2019;380(24):2295-2306. https://doi.org/10.1056/NEJMoa1811744
24. Agarwal R, Anker SD, Filippatos G, et al. Effects of canagliflozin versus finerenone on cardiorenal outcomes: exploratory post hoc analyses from FIDELIO-DKD compared to reported CREDENCE results. Nephrol Dial Transplant. 2021, https://doi.org/10.1093/ndt/gfab336
25. Kolkhof P, Hartmann E, Freyberger A, et al. Effects of Finerenone Combined with Empagliflozin in a Model of Hypertension-Induced End-Organ Damage. Am J Nephrol. 2021;52(8):642-652. https://doi.org/10.1159/000516213
26. Rossing P, Anker SD, Filippatos G, et al. Finerenone in Patients With Chronic Kidney Disease and Type 2 Diabetes by Sodium-Glucose Cotransporter 2 Inhibitor Treatment: The FIDELITY Analysis. Diabetes Care. 2022;45(12):2991-2998, https://doi.org/10.2337/dc22-0294
27. Provenzano M, Jongs N, Vart P, et al. The kidney protective effects of the sodium-glucose cotransporter-2 inhibitor, dapagliflozin, are present in patients with CKD treated with mineralocorticoid receptor antagonists. Kidney Int Rep. 2021;7(3):436–443, https://doi.org/10.1016/j.ekir.2021.12.013
28. Heerspink HJL, Vart P, Jongs N, et al. Estimated lifetime benefit of novel pharmacological therapies in patients with type 2 diabetes and chronic kidney disease: A joint analysis of randomized controlled clinical trials. Diabetes Obesity and Metabolism, 2023;25(11):3327-3336. https://doi.org/10.1111/dom.15232
29. Naaman SC, Bakris GL. Diabetic Nephropathy: Update on Pillars of Therapy Slowing Progression. Diabetes Care. 2023; 46(9):1574-1586. https://doi.org/10.2337/dci23-0030
30. Neuen BL, Heeerspink HJL, Vart P, et al. Estimated Lifetime Cardiovascular, Kidney and Mortality Benefits of Combination Treatment With SGLT2 Inhibitors, GLP-1 Receptor Agonists, and Non-steroidal MRA Compared With Conventional Care in Patients With Type 2 Diabetes and Albuminuria. Circulation. 2023. Ahead of print. https://doi.org/10.1161/CIRCULATIONAHA.123.067584
31. Heidenreich PA, Bozkurt B, Aguilar D, et al. 2022 AHA/ACC/HFSA Guideline for the Management of Heart Failure: A Report of the American College of Cardiology/American Heart Association Joint Committee on Clinical Practice Guidelines. Circulation, 2022;145(18):e895-e1032. https://doi.org/10.1161/CIR.0000000000001063
32. Desai NR, Navaneethan SD, Nicholas SB, et al. Design and rationale of FINE-REAL: A prospective study of finerenone in clinical practice. J Diabetes Complications. 2023;37(4):108411. https://doi.org/10.1016/j.jdiacomp.2023.108411
33. Vizcaya D, Kovesdy CP, Reyes A, et al. Characteristics of patients with chronic kidney disease and Type 2 diabetes initiating finerenone in the USA: a multi-database, cross-sectional study. J Comp Eff Res. 2023;12(8):e230076, https://doi.org/10.57264/cer-2023-0076
34. Nicholas SB, Correa-Rotter R, Desai N, et al. Interim Results from FINE-REAL: A Prospective Study Providing Insights into the Use of Finerenonein Routine Clinical Settings. Presented on November 2023 ASN Congress. Poster number SA-PO481
35. Joseph JJ, Deedwania P, Acharya T, et al. Comprehensive Management of Cardiovascular Risk Factors for Adults With Type 2 Diabetes: A Scientific Statement From the American Heart Association. Circulation. 2022;145(9):e722-e759, https://doi.org/10.1161/CIR.0000000000001040
36. Blonde L, Umpierrez GE, Reddy SS, et al. American Association of Clinical Endocrinology Clinical Practice Guideline: Developing a Diabetes Mellitus Comprehensive Care Pland2022 Update. Endocr Pract. 2022;28(10):923-1049, https://doi.org/10.1016/j.eprac.2022.08.002
37. Kidney Disease: Improving Global Outcomes (KDIGO) Diabetes Work Group. KDIGO 2022 Clinical Practice Guideline for Diabetes Management in Chronic Kidney Disease. Kidney Int. 2022;102(5S): S1-S127. https://doi.org/10.1016/j.kint.2022.06.008
38. ElSayed NA, Aleppo G, Aroda VR, et al. Summary of Revisions: Standards of Care in Diabetes-2023. Diabetes Care. 2023;46 (Suppl 1):S5-S9. https://doi.org/10.2337/dc23-Srev
39. Mancia G, Kreutz R, Brunstrom M, et al. 2023 ESH Guidelines for the management of arterial hypertension. J Hypertens. 2023;41(12):1874-2071. https://doi.org/10.1097/HJH.0000000000003480
40. Sarafidis PA, Iatridi F, Ferro C, et al. Mineralocorticoid receptor antagonist use in chronic kidney disease with type 2 diabetes: a clinical practice document by the European Renal Best Practice (ERBP) board of the European Renal Association (ERA), Clinical Kidney Journal. 2023; 16(11): 1885–1907. https://doi.org/10.1093/ckj/sfad139
41. McDonagh TA, Metra M, Adamo M, et al. 2023 Focused Update of the 2021 ESC Guidelines for the diagnosis and treatment of acute and chronic heart failure. Eur Heart J. 2023;44(37):3627-3639. https://doi.org/10.1093/eurheartj/ehad195
42. Blazek O, Bakris GL. The evolution of “pillars of therapy” to reduce heart failure risk and slow diabetic kidney disease progression. American Heart Journal Plus. 2022;19. https://doi.org/10.1016/j.ahjo.2022.100187.
43. Wanner C, Fioretto P, Kovesdy CP, et al. Endocrinol Diabetes Metab. 2022;5(6):e360. https://doi.org/10.1002/edm2.360
Об авторах
Ю. Ш. ХалимовРоссия
Халимов Юрий Шавкатович - д.м.н., профессор.
197022, Санкт-Петербург, ул. Льва Толстого, д. 6-8
Конфликт интересов:
Публикация подготовлена при поддержке АО «Байер». Компания «Байер» поддерживала техническую редакцию статьи
Г. В. Семикова
Россия
Семикова Галина Владимировна - к.м.н., ассистент.
197022, Санкт-Петербург, ул. Льва Толстого, д. 6–8
Конфликт интересов:
Публикация подготовлена при поддержке АО «Байер». Компания «Байер» поддерживала техническую редакцию статьи
Ю. А. Шутова
Россия
Шутова Юлия Александровна
Конфликт интересов:
Публикация подготовлена при поддержке АО «Байер». Компания «Байер» поддерживала техническую редакцию статьи. Ю.А. Шутова является сотрудником АО «Байер»
Дополнительные файлы
|
|
1. Рисунок 1. Комплементарные механизмы действия ингибиторов натрий-глюкозных ко-транспортеров 2 типа и финеренона. | |
| Тема | ||
| Тип | Исследовательские инструменты | |
Посмотреть
(536KB)
|
Метаданные ▾ | |
|
|
2. Рисунок 2. Сравнительный анализ результатов FIDELIO и CREDENCE после корректировки основных различий. Адаптировано из [24]. | |
| Тема | ||
| Тип | Исследовательские инструменты | |
Посмотреть
(489KB)
|
Метаданные ▾ | |
|
|
3. Рисунок 3. Эффекты терапии финереноном и ингибиторами натрий-глюкозных ко-транспортеров 2 типа в доклинических испытаниях. Адаптировано из [25]. | |
| Тема | ||
| Тип | Исследовательские инструменты | |
Посмотреть
(360KB)
|
Метаданные ▾ | |
|
|
4. Рисунок 4. Кардионефропротективный эффект финеренона в зависимости от исходной терапии ингибиторами натрий-глюкозных ко-транспортеров 2 типа. Адаптировано из [26]. | |
| Тема | ||
| Тип | Исследовательские инструменты | |
Посмотреть
(241KB)
|
Метаданные ▾ | |
|
|
5. Рисунок 5. Эффекты комбинированной болезнь-модифицирующей терапии хронической болезни почек (ингибиторы натрий-глюкозных ко-транспортеров 2 типа+финеренон+ингибиторы ангиотензин-превращающего фермента (иАПФ) или блокаторы рецепторов к ангиотензину II) по сравнению со стандартной терапией ингибиторами ангиотензин-превращающего фермента (иАПФ) или блокаторами рецепторов к ангиотензину II по ключевым конечным точкам. Адаптировано из [28]. | |
| Тема | ||
| Тип | Исследовательские инструменты | |
Посмотреть
(145KB)
|
Метаданные ▾ | |
Рецензия
Для цитирования:
Халимов Ю.Ш., Семикова Г.В., Шутова Ю.А. Перспективы комбинированного применения современных препаратов для кардионефропротекции у пациентов с сахарным диабетом 2 типа и хронической болезнью почек. Сахарный диабет. 2024;27(1):93-103. https://doi.org/10.14341/DM13113
For citation:
Khalimov Yu.Sh., Semikova G.V., Shutova Yu.A. Novel cardioprotective and nephroprotective combination in patients with type 2 diabetes and chronic kidney disease: perspectives of use. Diabetes mellitus. 2024;27(1):93-103. (In Russ.) https://doi.org/10.14341/DM13113
JATS XML

Контент доступен под лицензией Creative Commons Attribution-NonCommercial-NoDerivatives 4.0 International License (CC BY-NC-ND 4.0).















































