Перейти к:
Влияние ингибиторов натрий-глюкозного котранспортера 2 типа дапаглифлозина на показатели общей смертности больных сахарным диабетом 2 типа (исследование CARDIA-MOS, Москва)
https://doi.org/10.14341/DM12929
Аннотация
ОБОСНОВАНИЕ. Широкое применение в клинической практике препаратов с кардио- и нефропротективными свойствами, в частности ингибиторов натрий-глюкозного котранспортера 2 типа (иНГЛТ-2), базируется на результатах крупномасштабных международных рандомизированных исследований. Между тем отсутствуют данные, демонстрирующие возможности влияния данных препаратов на показатели смертности в реальной клинической практике у российских пациентов. Для изучения данного вопроса было проведено исследование CARDIA-MOS на популяции больных сахарным диабетом 2 типа (СД2) г. Москвы.
ЦЕЛЬ. Изучить влияние иНГЛТ-2 на показатели общей смертности больных СД2 Москвы.
МАТЕРИАЛЫ И МЕТОДЫ. Для оценки частоты различных исходов были сформированы две выборки пациентов по заранее определенным критериям: 1) пациенты, начавшие терапию иНГЛТ-2 (дапаглифлозином) в 2017 г. и получавшие его в течение 48 мес; 2) контрольная группа пациентов (не получавших иНГЛТ-2), соответствующая основной группе по ключевым показателям: возраст, длительность СД, наличие сердечно-сосудистых заболеваний, использование инсулинотерапии, уровень гликированного гемоглобина (НbА1с).
РЕЗУЛЬТАТЫ. На 1-м этапе работы был проведен анализ данных 499 пациентов, начавших лечение дапаглифлозином в 2017 г., а также 499 пациентов контрольной группы (n=998). Исходные характеристики пациентов в основном были сопоставимыми. Показатели систолического артериального давления и уровня НbА1с до исследования были хуже в группе дапаглифлозина. Применение дапаглифлозина ассоциировалось со снижением относительного риска (ОР) смерти от всех причин на 39% (ОР 0,614; 95% ДИ 0,417–0,903; р=0,013), приводило к снижению уровня НbА1с на 0,8% (с 8,5 до 7,7%, p<0,001) на протяжении 48 мес наблюдения.
ЗАКЛЮЧЕНИЕ. Использование дапаглифлозина в терапии больных СД2 позволяет снизить показатели общей смертности и улучшить показатели гликемического контроля.
Ключевые слова
Для цитирования:
Анциферов М.Б., Демидов Н.А., Балберова М.А., Лобанова О.В., Мудрикова И.Г., Гусенбекова Д.Г. Влияние ингибиторов натрий-глюкозного котранспортера 2 типа дапаглифлозина на показатели общей смертности больных сахарным диабетом 2 типа (исследование CARDIA-MOS, Москва). Сахарный диабет. 2022;25(5):439-448. https://doi.org/10.14341/DM12929
For citation:
Antsiferov M.B., Demidov N.A., Balberova M.A., Lobanova O.V., Mudrikova I.G., Gusenbekova D.G. Influence of type 2 sodium-glucose co-transporter inhibitors (dapagliflozin) on the indicators of total mortality in patients with type 2 diabetes (CARDIA-MOS study, Moscow). Diabetes mellitus. 2022;25(5):439-448. https://doi.org/10.14341/DM12929
ОБОСНОВАНИЕ
Согласно оценке Международной федерации диабета (International Diabetes Federation, IDF), глобальная распространенность сахарного диабета (СД) к 2045 г. увеличится в 1,5 раза [1]. При этом большую часть случаев составляет СД типа (СД2). Несмотря на широкий спектр используемых в настоящее время сахароснижающих препаратов, СД2 по-прежнему ассоциирован с высоким риском развития отдаленных осложнений и смертностью от сердечно-сосудистых заболеваний [2].
Терапия СД2 включает изменения образа жизни и фармакотерапию с целью предотвращения развития осложнений, а также постоянный мониторинг показателей гликемического контроля, в первую очередь гликированного гемоглобина (HbA1c). Американская диабетическая ассоциация (ADA) и Европейская ассоциация по изучению диабета (EASD) рекомендуют устанавливать индивидуальные целевые уровни HbA1c с учетом состояния пациентов, рисков, связанных с терапией и наличием сопутствующих заболеваний. В соответствии с консенсусным заявлением ADA/EASD [3][4] целевой показатель HbA1c для большинства взрослых пациентов составляет ≤7,0%. В российских рекомендациях 2021 г. также отмечается необходимость указания индивидуального целевого уровня HbA1c в структуре диагноза. При этом для большинства взрослых пациентов уровень HbA1c≤7,0% также считается целевым [5].
Однако достижение и удержание целевых значений HbA1c у больных СД2 не дают им полной гарантии с точки зрения развития и прогрессирования сердечно-сосудистых заболеваний, хронической сердечной недостаточности (ХСН) и хронической болезни почек (ХБП) [6–10]. По данным Федерального регистра пациентов с СД, ХСН является причиной смерти примерно 30% больных СД2 [6]. Около трети всех пациентов с СД2 имеют ХБП, что приводит к увеличению частоты госпитализаций и смертности, а также увеличению потребности в диализе и избыточной нагрузке на систему здравоохранения [7].
Современные подходы к назначению противодиабетической терапии предполагают необходимость учета коморбидных состояний. Особое внимание уделяется использованию препаратов, обладающих, помимо сахароснижающего эффекта, кардио-и ренопротективными свойствами. К настоящему моменту разработаны и успешно применяются новые классы антидиабетических препаратов, одним из которых являются ингибиторы натрий-глюкозного котранспортера-2 (иНГЛТ-2). Они стали первой группой препаратов, продемонстрировавшей снижение рисков сердечно-сосудистых событий и госпитализаций по поводу ХСН, в связи с чем заняли особое место в терапии СД2 [8–10]. Ключевой особенностью применения иНГЛТ-2 стала возможность снижения частоты крупных сердечно-сосудистых исходов (сердечно-сосудистой смертности, нефатального инфаркта миокарда (ИМ) и острого нарушения мозгового кровообращения), а также госпитализации по поводу ХСН [11]. Применение данных препаратов снижает необходимость в диализе, частоту трансплантаций или смерти из-за болезни почек, а также частоту иных неблагоприятных ренальных исходов [12]. Несмотря на обширную доказательную базу, убедительно демонстрирующую кардио- и нефропротективные эффекты иНГЛТ-2, возникает вопрос воспроизводимости данных эффектов в реальной клинической практике в российской популяции пациентов и влияния применения данных препаратов на выживаемость больных СД2, что и стало предметом изучения в исследовании CARDIA-MOS. На первом этапе работы было изучено влияние препарата дапаглифлозин на показатели общей смертности при добавлении к проводимой терапии больных СД2.
Дапаглифлозин — селективный и обратимый иНГЛТ-2 [13], продемонстрировавший высокий уровень эффективности и безопасности в рандомизированных контролируемых исследованиях, в том числе в отношении кардиоренальных исходов [14–17].
ЦЕЛЬ ИССЛЕДОВАНИЯ
Анализ влияния дапаглифлозина на показатели общей смертности пациентов с СД2 г. Москвы.
МАТЕРИАЛЫ И МЕТОДЫ
Место и время проведения исследования
Место проведения. ГБУЗ «Эндокринологический диспансер Департамента здравоохранения г. Москвы», Москва.
Время исследования. В анализ включались ретроспективные данные первичной медицинской документации больных СД2 за период с 01.01.2017 по 31.12.2020.
Изучаемые популяции (одна или несколько)
Для оценки частоты различных исходов терапии больных СД2 были сформированы две выборки пациентов: основная и контрольная группы.
Основная группа (группа дапаглифлозина) формировалась по следующим критериям.
Критерии включения:
- СД2;
- возраст 50–75 лет;
- наличие в анамнезе сердечно-сосудистых заболеваний (ССЗ) или 1 и более факторов риска ССЗ (артериальная гипертензия, дислипидемия);
- отсутствие до момента включения в исследование приема препаратов из группы агонистов рецепторов глюкагоноподобного пептида-1 (арГПП-1) либо иНГЛТ-2;
- начало терапии иНГЛТ-2 (дапаглифлозин) в 2017 г.
Критерии исключения:
- отсутствие в медицинской документации информации о состоянии здоровья на протяжении всего периода наблюдения (48 мес), за исключением подтвержденных случаев смерти в течение данного периода;
- указание в медицинской документации об отмене терапии дапаглифлозином на срок более 3 мес в течение периода наблюдения;
- наличие терапии арГПП-1 в течение периода исследования (48 мес со дня старта терапии иНГЛТ-2).
Контрольная группа пациентов формировалась по следующим критериям:
Критерии включения:
- СД2;
- возраст 50–75 лет;
- наличие в анамнезе ССЗ или 1 и более факторов риска ССЗ (артериальная гипертензия, дислипидемия);
- отсутствие до момента включения в исследование и в течение всего периода наблюдения (48 мес) приема препаратов из группы арГПП-1 либо иНГЛТ-2.
Критерии исключения:
- отсутствие в медицинской документации информации о состоянии здоровья на протяжении всего периода наблюдения (48 мес), за исключением подтвержденных случаев смерти в течение периода наблюдения.
Способ формирования выборки из изучаемой популяции (или нескольких выборок из нескольких изучаемых популяций)
Основная группа пациентов (группа дапаглифлозина) была сформирована путем выборки из базы данных Московского сегмента ФРСД больных СД2, которые начали получать терапию дапаглифлозином в период с 01.01.2017 по 31.12.2017 с учетом критериев включения и исключения (n=703). Так как первичная медицинская документация содержит гораздо больше информации, чем база данных ФРСД, была проведена повторная проверка соответствия критериям включения и исключения сформированной когорты пациентов (n=703) с помощью анализа данных, содержащихся в электронной амбулаторной карте ЕМИАС. Пациенты, соответствовавшие критериям включения и не соответствовавшие критериям исключения по данным первичной медицинской документации (n=499), составили основную группу.
Для формирования контрольной группы пациенты основной группы были разделены на 36 подгрупп в зависимости от пола, возрастной категории (<60 лет, 60–70 лет, >70 лет), наличия в анамнезе ССЗ, применения инсулинотерапии.
Контрольная группа пациентов была сформирована случайным образом при выборке из московского сегмента ФРСД больных СД2, соответствовавших критериям включения и не соответствовавших критериям исключения (n=4317). Далее из данной выборки было сформировано 36 подгрупп пациентов, сопоставимых по основным характеристикам (пол, возрастная группа, длительность СД, ИМТ, уровень НbА1с, наличие ССЗ в анамнезе, использование инсулинотерапии) с подгруппами пациентов из основной группы (группы дапаглифлозина) в количестве 2736 чел. С помощью генератора случайных чисел из данной выборки были отобраны 449 пациентов, которые составили контрольную группу.
Дизайн исследования
Ретроспективное двухвыборочное сравнительное исследование, срок наблюдения 48 мес.
Статистический анализ
В рамках статистической обработки для количественных переменных представлены средние значения и стандартные отклонения, а для категориальных переменных — частоты и доли (%). Анализ выживаемости проводился с использованием модели регрессионного анализа пропорциональных рисков Кокса. В качестве результатов регрессионного анализа приводятся отношения рисков (ОР) с 95% доверительным интервалом (ДИ). В качестве основного показателя эффективности использовался критерий смертности от всех причин; для оценки дополнительных показателей — смертность от ХСН, ССЗ, COVID-19, сочетания COVID-19 и ССЗ, а также подгрупповые анализы в зависимости от исходных характеристик.
Этическая экспертиза
Исследование было одобрено локальным этическим комитетом ГБУЗ "Эндокринологический диспансер Департамента здравоохранения г. Москвы" (номер протокола отсутствует, заключение от 28.06.2022).
РЕЗУЛЬТАТЫ
Исходные характеристики пациентов двух групп были сопоставимыми по основным показателям (табл. 1). По ряду характеристик между группами были выявлены статистически значимые различия (уровень НbА1с, уровень систолического АД, частота использования метформина). При этом показатели уровней АД и НbА1с в группе дапаглифлозина были хуже, чем в группе контроля. Метформин в группе дапаглифлозина использовался реже (табл. 1).
Таблица 1. Исходные характеристики пациентов
|
Контроль |
Дапаглифлозин |
p* |
|
|
Количество, n |
499 |
499 |
|
|
Возраст, лет (SD) |
62,7 (6,0) |
62,5 (5,8) |
p>0,05 |
|
Пол, муж., n (%) |
205 (41,1) |
205 (41,1) |
1,000 |
|
Длительность СД, лет (SD) |
8,7 (4,5) |
8,8 (5,6) |
p>0,05 |
|
ИМТ, кг/м² (SD) |
34,04 |
33,91 |
p>0,05 |
|
САД, мм рт. ст. |
133,27 |
134,87 |
p=0,013 |
|
HbA1c, % |
8,27 |
8,53 |
p<0,001 |
|
ОХС, ммоль/л, среднее |
5,84 |
5,99 |
p>0,05 |
|
ЛПНП, ммоль/л, среднее |
2,75 |
2,72 |
p>0,05 |
|
Подтвержденное ССЗ, n (%) |
217 (43,5) |
211 (42,3) |
p>0,05 |
|
Терапия: |
|||
|
Метформин, n (%) |
468 (93,8) |
429 (86,0) |
p<0,001 |
|
ПСМ, n (%) |
289 (57,9) |
284 (56,9) |
p>0,05 |
|
иДПП-4, n (%) |
63 (12,6) |
56 (11,2) |
p>0,05 |
|
Инсулин, n (%) |
193 (38,7) |
193 (38,7) |
p>0,05 |
*р — для сравнений контрольной группы с группой дапаглифлозина.
Примечание. ПСМ — препараты сульфонилмочевины; иДПП-4 — ингибиторы дипептидилпептидазы-4; ИМТ — индекс массы тела; ОХС — общий холестерин; ЛПНП — липопротеины низкой плотности; СД — сахарный диабет; САД — систолическое артериальное давление; ССЗ — сердечно-сосудистое заболевание.
Показатели смертности
Результаты анализа свидетельствуют о статистически значимом снижении ОР смерти от всех причин в группе пациентов, получавших дапаглифлозин, на 39% (рис. 1): ОР 0,614; 95% ДИ 0,417–0,903; р=0,013. При этом частота достижения данной конечной точки за 4 года наблюдения в группе дапаглифлозина составила 8,4%, тогда как в контрольной группе — 13,4%, показатель NNT (Number Needed to Treat, число больных, которых необходимо лечить) при этом составило 20 (рис. 1).

Рисунок 1. Смертность от всех причин в группах.
Figure 1. Mortality from all causes in groups.
Дапа — дапаглифлозин.
При анализе показателя смертности от ХСН результаты были еще более значительными: в группе пациентов, получавших дапаглифлозин, снижение ОР смерти от ХСН за период наблюдения составило 77% (рис. 2): ОР 0,230; 95% ДИ 0,077–0,683; р=0,008. Так, смертность от ХСН в группе дапаглифлозина составила 0,7%, а в контрольной группе — 3,4% за аналогичный период наблюдения (рис. 2).

Рисунок 2. Смертность от хронической сердечной недостаточности в группах.
Figure 2. Mortality from chronic heart failure in groups.
Дапа — дапаглифлозин.
Кроме того, наблюдалась тенденция к снижению риска смерти от ССЗ и от COVID-19 в группе пациентов, получавших дапаглифлозин: для ССЗ ОР составил 0,431; 95% ДИ 0,177–1,048; р=0,063, для COVID-19 — 0,667; 95% ДИ 0,329–1,351; р=0,261. При этом при оценке частоты комбинированной конечной точки «смерть от ССЗ + COVID-19» было зарегистрировано статистически значимое снижение риска на 44%: ОР 0,56; 95% ДИ 0,323–0,969; р=0,038, а смертность от ССЗ + COVID-19 составила 2,6% в группе дапаглифлозина и 3,8% в контрольной группе.
При проведении субанализов в зависимости от исходных характеристик пациентов было продемонстрировано, что у пациентов, находившихся на инсулинотерапии до включения в исследование, отмечалась тенденция к снижению смертности отвсех причин в группе дапаглифлозина: ОР 0,62; 95% ДИ 0,37–1,10; р=0,064. Кроме того, было показано снижение риска смерти от всех причин среди женщин, получавших дапаглифлозин, на 46%: ОР 0,54; 95% ДИ 0,30–0,98; р=0,042 по сравнению с женщинами контрольной группы.
Наличие или отсутствие подтвержденного ССЗ в анамнезе на момент включения в анализ является значимым фактором, влияющим на выживаемость пациентов. У пациентов без подтвержденного ССЗ на момент включения в анализ риск смерти был на 39% ниже (ОР 0,616; 95% ДИ 0,419–0,905; р=0,014), чем у больных СД2 с ССЗ в анамнезе (рис. 3).

Рисунок 3. Смертность от всех причин в зависимости от наличия сердечно-сосудистого заболевания на момент включения в анализ данных.
Figure 3. All-cause mortality by presence of cardiovascular disease at the time of inclusion in the data analysis
ССЗ — сердечно-сосудистое заболевание.
Терапия дапаглифлозином в подгруппе пациентов с подтвержденным ССЗ приводила к снижению ОР смерти от всех причин на 47%, тогда как в когорте пациентов без зарегистрированного ССЗ наблюдалась только тенденция к снижению ОР смерти от всех причин на 23% (рис. 4).

Рисунок 4. Смертность от всех причин в когортах, распределенных по наличию подтвержденного сердечно-сосудистого заболевания.
Figure 4. All-cause mortality in cohorts categorized by confirmed CVD.
Дапа — дапаглифлозин, ССЗ — сердечно-сосудистое заболевание.
Динамика клинических и лабораторных показателей
Помимо показателей смертности, была оценена динамика ряда клинических и лабораторных показателей. Начиная с 3-го месяца наблюдения в группе дапаглифлозина было показано статистически значимое снижение уровня НbА1с, несмотря на более высокие исходные показатели (рис. 5).

Рисунок 5. Динамика уровня гликированного гемоглобина в группах за 48 месяцев наблюдения.
Figure 5. Dynamics of glycated hemoglobin levels in groups over 48 months of observation
Аналогичная положительная динамика была зарегистрирована для показателей массы тела и ИМТ. Так, спустя 48 мес наблюдения масса тела в группе дапаглифлозина составила 92,8 кг, тогда как в контрольной группе — 95,3 кг (р=0,022). При этом важно отметить, что исходное значение данного показателя в группе дапаглифлозина значимо превышало таковое в контрольной группе (исходная масса тела в группе дапаглифлозина — 95,9 кг, в группе контроля — 94,2 кг). ИМТ в группе дапаглифлозина через 48 мес наблюдения составил 29,4 кг/м² (снижение с начала исследования на 4,5 кг/м²), в контрольной группе — 34,3 кг/м² (увеличение с начала исследования на 0,4 кг/м²), p<0,001. При этом на старте исследования статистически значимых различий между группами по ИМТ не было выявлено.
За 48 мес наблюдения отмечалось значимое снижение как систолического, так и диастолического АД в обеих группах (рис. 6). За время наблюдения отмечалась лишь тенденция к снижению частоты основных сердечно-сосудистых исходов при применении дапаглифлозина. Различия между группами по отдельным показателям (инфаркт миокарда (ИМ)), реваскуляризация, острое нарушение мозгового кровообращения) не достигли статистической значимости.

Рисунок 6. Динамика показателей артериального давления в группах за 48 месяцев наблюдения.
Figure 6. Dynamics of blood pressure indicators in groups for 48 months of observation.
За период наблюдения была продемонстрирована положительная динамика расчетной скорости клубочковой фильтрации (рСКФ) при применении дапаглифлозина: через 48 мес после старта терапии было показано улучшение рСКФ на 2,1% исходного значения (рис. 7). Доля пациентов с нормальными значениями рСКФ через 48 мес наблюдения в контрольной группе составила 12,6%, в группе дапаглифлозина — 22,1%.

Рисунок 7. Динамика расчетной скорости клубочковой фильтрации в группах за 48 месяцев наблюдения.
Figure 7. Dynamics of the calculated glomerular filtration rate in groups for 48 months of observation.
Профиль безопасности в группе дапаглифлозина был сравним с таковым в группе контроля и не противоречил результатам ранее проведенных клинических исследований (табл. 2). В группе дапаглифлозина не было зарегистрировано случаев диализа в отличие от контрольной группы.
Таблица 2. Показатели безопасности в группах на 48-м месяце наблюдения
|
Контроль |
Дапаглифлозин |
P |
|||
|
случаев, n |
доля, % |
Случаев, n |
доля, % |
||
|
Ампутации |
3 |
0,6 |
5 |
1,0 |
0,48 |
|
Переломы |
13 |
2,6 |
11 |
2,2 |
0,68 |
|
Острое повреждение почек |
1 |
0,2 |
1 |
0,2 |
1,00 |
|
Диализ |
3 |
0,6 |
0 |
- |
0,08 |
ОБСУЖДЕНИЕ
Целью лечения СД2 является предотвращение развития осложнений путем достижения и длительного поддержания целевых показателей гликемического контроля. На данный момент в терапии СД2 используется несколько классов антигипергликемических препаратов с различными механизмами действия.
В качестве первой линии терапии в большинстве случаев рекомендовано изменение образа жизни, включающее снижение массы тела (для пациентов с избыточной массой тела или ожирением) и повышение физической активности, а также использование метформина (при отсутствии противопоказаний и хорошей переносимости) [4][5]. Выбор других видов терапии должен быть индивидуализирован в соответствии с анамнезом, массой тела, рисками гипогликемии, наличием ССЗ и/или ХБП, стоимостью препаратов и предпочтениями пациента. Также следует учитывать, что ССЗ являются основной причиной смертности при СД2. Большая часть смертей таких пациентов приходится на ХСН, ИМ и инсульт. Таким образом, особое значение приобретает использование классов препаратов, снижающих сердечно-сосудистую заболеваемость и смертность [18].
иНГЛТ-2 представляют собой относительно новый класс противодиабетических препаратов, снижающих уровень глюкозы в крови за счет увеличения экскреции глюкозы с мочой. Благодаря независимому от инсулина механизму действия иНГЛТ-2 возможно комбинировать с другими антигипергликемическими препаратами, включая инсулин, с минимальными рисками гипогликемии [19]. Дапаглифлозин — высокоселективный иНГЛТ-2 с доказанной эффективностью и безопасностью у пациентов сСД2 [19]. В клинических исследованиях препарат, принимавшийся в виде моно- и комбинированной терапии с другими препаратами, обеспечивал эффективный контроль гликемии, снижение массы тела и АД у пациентов с СД2, включая пациентов с артериальной гипертензией и/или иными ССЗ [14–17]. Данные реальной клинической практики подтверждают эффективность дапаглифлозина у пациентов с СД2 [20–23].
Нельзя не отметить, что популяции пациентов в исследованиях иНГЛТ-2 отличались по исходным характеристикам. Так, в исследовании EMPA-REG OUTCOME [8] участвовали пациенты с СД2 и установленным ССЗ, при этом у каждого четвертого пациента в исследовании наблюдался высокий пятилетний риск ХСН, еще у 5,1% пациентов — очень высокий. В исследовании DECLARE [15] значительную часть пациентов составляла когорта первичной профилактики, тогда как в исследовании CANVAS [10] у двух третей пациентов наблюдалось ССЗ в анамнезе.
В метаанализе трех рандомизированных плацебо-контролируемых исследований иНГЛТ-2 [24], оценивающем сердечно-сосудистые исходы у пациентов с СД2, было показано, что иНГЛТ-2 уменьшали риск крупного сердечно-сосудистого события на11%, риск сердечно-сосудистой смерти или госпитализации по причине ХСН у пациентов с ССЗ на 23%. Кроме того, иНГЛТ-2 снижали частоту ухудшения функции почек, терминальной стадии почечной недостаточности или смерти по причине почечной дисфункции как у пациентов с атеросклеротическими ССЗ, так и без них.
Результаты данного исследования в целом согласуются с результатами крупных рандомизированных клинических исследований иНГЛТ-2. Так, согласно результатам EMPA-REG OUTCOME [24], снижение риска смерти от всех причин в группе эмпаглифлозина составило 32% (ОР 0,68; 95% ДИ 0,57–0,82; p<0,001). Согласно данным нашего исследования, применение дапаглифлозина ассоциировалось со снижением риска смерти от всех причин на 39%.
Эффективность дапаглифлозина в предотвращении сердечно-сосудистых событий подтверждается результатами исследования DECLARE-TIMI 58 [15], а также исследованием CVD-REAL Nordic [25]. Дапаглифлозин значимо снижал риск МАСЕ на22% (ОР 0,78; 95% ДИ 0,67–0,94), госпитализации по поводу ХСН на 38% (ОР 0,62; 95% ДИ 0,50–0,77) и смертности от всех причин на 41% (ОР 0,59; 95% ДИ 0,49–0,72) по сравнению с ингибиторами дипептидилпептидазы 4-го типа.
Наличие или отсутствие подтвержденного ССЗ в анамнезе на момент включения пациента в анамнез являлось значимым фактором, оказывавшим влияние на выживаемость пациентов. В нашем исследовании пациенты с подтвержденным ССЗ также получали наибольшую пользу от терапии дапаглифлозином: риск смерти от всех причин снижался на 47% (рис. 8).
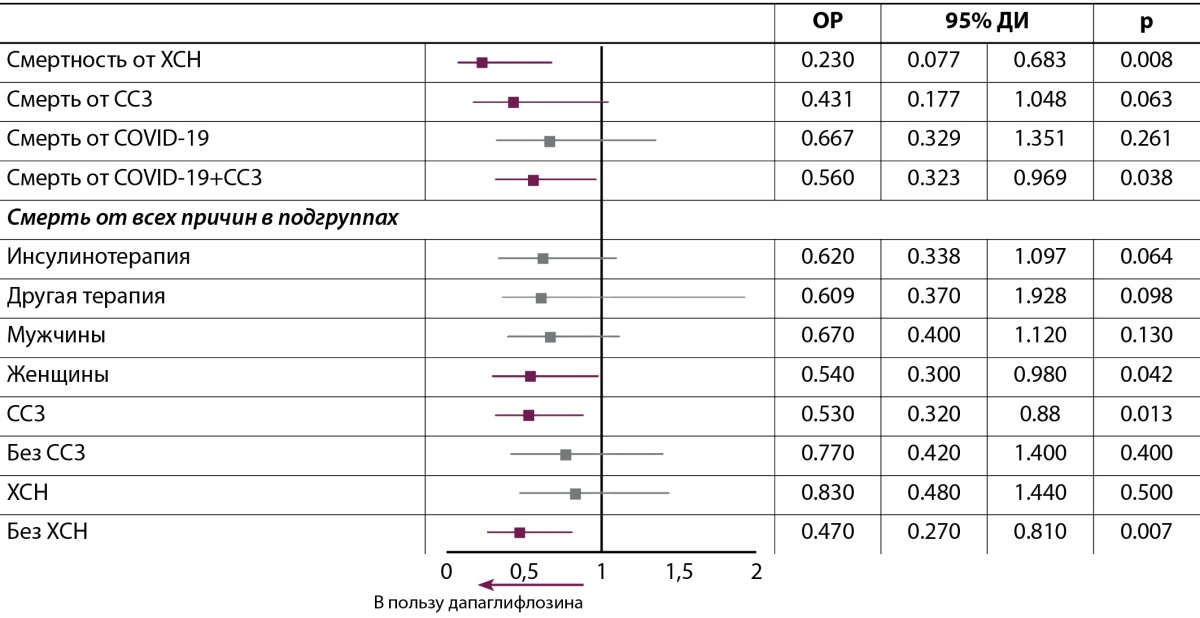
Рисунок 8. Риски различных исходов в целом и в подгруппах пациентов.
Figure 8. Risks of various outcomes in general and in subgroups of patients
Кроме того, применение дапаглифлозина ассоциировалось с отсутствием снижения рСКФ при наблюдении в течение 48 мес по сравнению с контрольной группой. Влияние дапаглифлозина на почечные исходы ранее также оценивали в исследовании DECLARE-TIMI 58 [26]. Было продемонстрировано, что дапаглифлозин снижал вероятность прогрессирования почечной недостаточности, о чем свидетельствовала более низкая частота почечных комбинированных и дополнительных почечных конечных точек в группе дапаглифлозина по сравнению с плацебо. В то же время среднее снижение рСКФ по сравнению с исходным уровнем было значимо больше в группе дапаглифлозина, чем в группе плацебо, через 6 мес (p<0,0001), однако эти показатели в группах сравнялись через 2 года наблюдения, а через 3 и 4 года после рандомизации снижение рСКФ в группе плацебо превысило таковое в группе дапаглифлозина [27].
Все это в совокупности свидетельствует о возможности применения препаратов класса иНГЛТ-2 и дапаглифлозина, в частности, для вторичной профилактики осложнений СД2 в реальной клинической практике. Препарат обладает выраженными кардио- и ренопротекторными свойствами, что подтверждается результатами предыдущих исследований и данной работы. В будущем исследователям предстоит ответить на вопросы о том, какие еще группы пациентов смогут получить пользу от терапии дапаглифлозином.
Возможные ограничения исследования
Необходимо отметить, что значимый отрезок периода наблюдения (часть 2019 г. и 2020 г.) пришелся на период широкого распространения COVID-19, что могло существенно повлиять на показатели смертности больных СД2, а также на структуру причин смерти.
Кроме того, несколько пациентов обеих групп не имели в медицинской документации информации о причине смерти, что также затрудняет понимание истинной структуры причин смерти и выделение категории «сердечно-сосудистая смертность».
ЗАКЛЮЧЕНИЕ
Использование в терапии больных СД2 препаратов из класса иНГЛТ-2, в частности дапаглифлозина, позволяет рассчитывать не только на улучшение показателей гликемического контроля, снижение массы тела и показателей АД, но и на снижение показателей общей смертности. Препарат демонстрирует кардио- и ренопротекторные свойства не только в рандомизированных клинических исследованиях, но и в исследовании реальной клинической практики на популяции российских пациентов. Одновременно с этим дапаглифлозин демонстрирует высокий уровень безопасности. Результаты данной работы позволяют рекомендовать дапаглифлозин для лечения широкой популяции больных СД2 с ССЗ и факторами риска их развития.
ДОПОЛНИТЕЛЬНАЯ ИНФОРМАЦИЯ
Источники финансирования. Исследование выполнено на базе Эндокринологического диспансера ДЗМ с использованием ресурсов данного учреждения.
Конфликт интересов. Авторы декларируют отсутствие явных и потенциальных конфликтов интересов, связанных с содержанием настоящей статьи.
Участие авторов. Все авторы внесли равный вклад в концептуализацию исследования, анализ и интерпретацию результатов, написание статьи и ее редактирование. Все авторы одобрили финальную версию рукописи и согласны нести ответственность за все аспекты работы.
Список литературы
1. Saeedi P, Petersohn I, Salpea P, et al. Global and regional diabetes prevalence estimates for 2019 and projections for 2030 and 2045: Results from the International Diabetes Federation Diabetes Atlas, 9th edition. Diabetes Res Clin Pract. 2019;157(4):107843. doi: https://doi.org/10.1016/j.diabres.2019.107843
2. Zheng Y, Ley SH, Hu FB. Global aetiology and epidemiology of type 2 diabetes mellitus and its complications. Nat Rev Endocrinol. 2018;14(2):88-98. doi: https://doi.org/10.1038/nrendo.2017.151
3. Davies MJ, D’Alessio DA, Fradkin J, et al. Management of hyperglycemia in type 2 diabetes, 2018. a consensus report by the American Diabetes Association (ADA) and the European Association for the Study of Diabetes (EASD). Diabetes Care. 2018;41(12):2669-2701. doi: https://doi.org/10.2337/dci18-0033
4. Buse JB, Wexler DJ, Tsapas A, et al. 2019 Update to: Management of Hyperglycemia in type 2 diabetes, 2018. a consensus report by the American Diabetes Association (ADA) and the European Association for the Study of Diabetes (EASD). Diabetes Care. 2020;43(2):487-493. doi: https://doi.org/10.2337/dci19-0066
5. Российская ассоциация эндокринологов. Клинические рекомендации. Сахарный диабет 2 типа у взрослых. М.: Минздрав РФ; 2021.
6. Калашников В.Ю., Викулова О.К., Железнякова А.В., и др. Эпидемиология сердечно-сосудистых заболеваний у больных сахарным диабетом, по данным федерального регистра Российской Федерации (2013–2016 гг.). // Сахарный диабет. — 2019. — Т. 22. №2. — С. 105-114. doi: https://doi.org/10.14341/DM10167
7. Pecoits-Filho R, Abensur H, Betônico CCR, et al. Interactions between kidney disease and diabetes: dangerous liaisons. Diabetol Metab Syndr. 2016;8(1):50. doi: https://doi.org/10.1186/s13098-016-0159-z
8. Fitchett D, Butler J, van de Borne P, et al. Effects of empagliflozin on risk for cardiovascular death and heart failure hospitalization across the spectrum of heart failure risk in the EMPA-REG OUTCOME® trial. Eur Heart J. 2018;39(5):363-370. doi: https://doi.org/10.1093/eurheartj/ehx511
9. Home P. Cardiovascular outcome trials of glucose-lowering medications: an update. Diabetologia. 2019;62(3):357-369. doi: https://doi.org/10.1007/s00125-018-4801-1
10. Neal B, Perkovic V, Mahaffey KW, et al. Canagliflozin and Cardiovascular and renal events in type 2 diabetes. N Engl J Med. 2017;377(7):644-657. doi: https://doi.org/10.1056/NEJMoa1611925
11. Usman MS, Siddiqi TJ, Memon MM, et al. Sodium-glucose co-transporter 2 inhibitors and cardiovascular outcomes: A systematic review and meta-analysis. Eur J Prev Cardiol. 2018;25(5):495-502. doi: https://doi.org/10.1177/2047487318755531
12. Zelniker TA, Wiviott SD, Raz I, et al. SGLT2 inhibitors for primary and secondary prevention of cardiovascular and renal outcomes in type 2 diabetes: a systematic review and meta-analysis of cardiovascular outcome trials. Lancet. 2019;393(10166):31-39. doi: https://doi.org/10.1016/S0140-6736(18)32590-X
13. Forxiga 10 mg film-coated tablets — Summary of Product Characteristics (SmPC) [Internet]. Available from: https://www.medicines.org.uk/emc/product/7607/smpc [cited April 18, 2022].
14. Rosenstock J, Vico M, Wei L, et al. Effects of dapagliflozin, an sglt2 inhibitor, on hba1c, body weight, and hypoglycemia risk in patients with type 2 diabetes inadequately controlled on pioglitazone monotherapy. Diabetes Care. 2012;35(7):1473-1478. doi: https://doi.org/10.2337/dc11-1693
15. Wiviott SD, Raz I, Bonaca MP, et al. Dapagliflozin and cardiovascular outcomes in type 2 diabetes. N Engl J Med. 2019;380(4):347-357. doi: https://doi.org/10.1056/NEJMoa1812389
16. Bailey CJ, Gross JL, Hennicken D, et al. Dapagliflozin add-on to metformin in type 2 diabetes inadequately controlled with metformin: a randomized, double-blind, placebo-controlled 102-week trial. BMC Med. 2013;11(1):43. doi: https://doi.org/10.1186/1741-7015-11-43
17. Strojek K, Yoon KH, Hruba V, et al. Effect of dapagliflozin in patients with type 2 diabetes who have inadequate glycaemic control with glimepiride: a randomized, 24-week, double-blind, placebo-controlled trial. Diabetes, Obes Metab. 2011;13(10):928-938. doi: https://doi.org/10.1111/j.1463-1326.2011.01434.x
18. Ferrannini E, DeFronzo RA. Impact of glucose-lowering drugs on cardiovascular disease in type 2 diabetes. Eur Heart J. 2015;36(34):2288-2296. doi: https://doi.org/10.1093/eurheartj/ehv239
19. Lupsa BC, Inzucchi SE. Use of SGLT2 inhibitors in type 2 diabetes: weighing the risks and benefits. Diabetologia. 2018;61(10):2118-2125. doi: https://doi.org/10.1007/s00125-018-4663-6
20. Wilding J, Bailey C, Rigney U, et al. Dapagliflozin therapy for type 2 diabetes in primary care: Changes in HbA1c, weight and blood pressure over 2 years follow-up. Prim Care Diabetes. 2017;11(5):437-444. doi: https://doi.org/10.1016/j.pcd.2017.04.004
21. Brown RE, Gupta N, Aronson R. Effect of dapagliflozin on glycemic control, weight, and blood pressure in patients with type 2 diabetes attending a specialist endocrinology practice in Canada: A retrospective cohort analysis. Diabetes Technol Ther. 2017;19(11):685-691. doi: https://doi.org/10.1089/dia.2017.0134
22. Han E, Kim A, Lee SJ, et al. Characteristics of dapagliflozin responders: A longitudinal, prospective, nationwide dapagliflozin surveillance study in Korea. Diabetes Ther. 2018;9(4):1689-1701. doi: https://doi.org/10.1007/s13300-018-0470-9
23. Fadini GP, Zatti G, Baldi I, et al. Use and effectiveness of dapagliflozin in routine clinical practice: An Italian multicentre retrospective study. Diabetes, Obes Metab. 2018;20(7):1781-1786. doi: https://doi.org/10.1111/dom.13280
24. Zinman B, Wanner C, Lachin JM, et al. Empagliflozin, cardiovascular outcomes, and mortality in type 2 diabetes. N Engl J Med. 2015;373(22):2117-2128. doi: https://doi.org/10.1056/NEJMoa1504720
25. Persson F, Nyström T, Jørgensen ME, et al. Dapagliflozin is associated with lower risk of cardiovascular events and all‐cause mortality in people with type 2 diabetes (CVD‐REAL Nordic) when compared with dipeptidyl peptidase‐4 inhibitor therapy: A multinational observationa. Diabetes, Obes Metab. 2018;20(2):344-351. doi: https://doi.org/10.1111/dom.13077
26. Bajaj HS, Raz I, Mosenzon O, et al. Cardiovascular and renal benefits of dapagliflozin in patients with short and long‐standing type 2 diabetes: Analysis from the DECLARE‐TIMI 58 trial. Diabetes, Obes Metab. 2020;22(7):1122-1131. doi: https://doi.org/10.1111/dom.14011
27. Mosenzon O, Wiviott SD, Cahn A, et al. Effects of dapagliflozin on development and progression of kidney disease in patients with type 2 diabetes: an analysis from the DECLARE–TIMI 58 randomised trial. Lancet Diabetes Endocrinol. 2019;7(8):606-617. doi: https://doi.org/10.1016/S2213-8587(19)30180-9
Об авторах
М. Б. АнциферовРоссия
Михаил Борисович Анциферов - доктор медицинских наук, профессор; eLibrary SPIN: 1035–4773.
Москва
Конфликт интересов:
отсутствие явных и потенциальных конфликтов интересов, связанных с содержанием настоящей статьи
Н. А. Демидов
Россия
Николай Александрович Демидов - кандидат медицинских наук, врач-эндокринолог; eLibrary SPIN: 7715-4508.
Москва, г. Московский, мкр. 3, стр. 7, 108111
Конфликт интересов:
отсутствие явных и потенциальных конфликтов интересов, связанных с содержанием настоящей статьи
М. А. Балберова
Россия
Мария Александровна Балберова - врач-эндокринолог; eLibrary SPIN: 7263-5503.
Москва
Конфликт интересов:
отсутствие явных и потенциальных конфликтов интересов, связанных с содержанием настоящей статьи
О. В. Лобанова
Россия
Ольга Владимировна Лобанова - врач-эндокринолог.
Москва
Конфликт интересов:
отсутствие явных и потенциальных конфликтов интересов, связанных с содержанием настоящей статьи
И. Г. Мудрикова
Россия
Ирина Геннадьевна Мудрикова - врач-эндокринолог; eLibrary SPIN: 8965-5850.
Москва
Конфликт интересов:
отсутствие явных и потенциальных конфликтов интересов, связанных с содержанием настоящей статьи
Д. Г. Гусенбекова
Россия
Динара Гаджимагомедовна Гусенбекова - кандидат медицинских наук, врач-эндокринолог; eLibrary SPIN: 5332-2890.
Москва
Конфликт интересов:
отсутствие явных и потенциальных конфликтов интересов, связанных с содержанием настоящей статьи
Дополнительные файлы
|
|
1. Рисунок 1. Смертность от всех причин в группах. | |
| Тема | ||
| Тип | Исследовательские инструменты | |
Посмотреть
(163KB)
|
Метаданные ▾ | |
|
|
2. Рисунок 2. Смертность от хронической сердечной недостаточности в группах. | |
| Тема | ||
| Тип | Исследовательские инструменты | |
Посмотреть
(162KB)
|
Метаданные ▾ | |
|
|
3. Рисунок 3. Смертность от всех причин в зависимости от наличия сердечно-сосудистого заболевания на момент включения в анализ данных | |
| Тема | ||
| Тип | Исследовательские инструменты | |
Посмотреть
(132KB)
|
Метаданные ▾ | |
|
|
4. Рисунок 4. Смертность от всех причин в когортах, распределенных по наличию подтвержденного сердечно-сосудистого заболевания. | |
| Тема | ||
| Тип | Исследовательские инструменты | |
Посмотреть
(232KB)
|
Метаданные ▾ | |
|
|
5. Рисунок 5. Динамика уровня гликированного гемоглобина в группах за 48 месяцев наблюдения | |
| Тема | ||
| Тип | Исследовательские инструменты | |
Посмотреть
(154KB)
|
Метаданные ▾ | |
|
|
6. Рисунок 6. Динамика показателей артериального давления в группах за 48 месяцев наблюдения. | |
| Тема | ||
| Тип | Исследовательские инструменты | |
Посмотреть
(181KB)
|
Метаданные ▾ | |
|
|
7. Рисунок 7. Динамика расчетной скорости клубочковой фильтрации в группах за 48 месяцев наблюдения. | |
| Тема | ||
| Тип | Исследовательские инструменты | |
Посмотреть
(149KB)
|
Метаданные ▾ | |
|
|
8. Рисунок 8. Риски различных исходов в целом и в подгруппах пациентов | |
| Тема | ||
| Тип | Исследовательские инструменты | |
Посмотреть
(318KB)
|
Метаданные ▾ | |
Рецензия
Для цитирования:
Анциферов М.Б., Демидов Н.А., Балберова М.А., Лобанова О.В., Мудрикова И.Г., Гусенбекова Д.Г. Влияние ингибиторов натрий-глюкозного котранспортера 2 типа дапаглифлозина на показатели общей смертности больных сахарным диабетом 2 типа (исследование CARDIA-MOS, Москва). Сахарный диабет. 2022;25(5):439-448. https://doi.org/10.14341/DM12929
For citation:
Antsiferov M.B., Demidov N.A., Balberova M.A., Lobanova O.V., Mudrikova I.G., Gusenbekova D.G. Influence of type 2 sodium-glucose co-transporter inhibitors (dapagliflozin) on the indicators of total mortality in patients with type 2 diabetes (CARDIA-MOS study, Moscow). Diabetes mellitus. 2022;25(5):439-448. https://doi.org/10.14341/DM12929
JATS XML

Контент доступен под лицензией Creative Commons Attribution-NonCommercial-NoDerivatives 4.0 International License (CC BY-NC-ND 4.0).















































