Перейти к:
Кардиодиабетология: эволюция или революция?
https://doi.org/10.14341/DM13295
Аннотация
Статья посвящена современным проблемам эндокринной кардиологии. Основное содержание работы составляет анализ истории лекарственных препаратов, применяемых в диабетологии, начиная от первых инсулинов животного происхождения до современных ингибиторов натрий-глюкозного котранспортера ٢ типа (НГЛТ-2) и агонистов рецепторов глюкагоноподобного пептида-1 (арГПП-1), обладающих выраженной кардиопротективной активностью. Проанализированы исследования, в которых доказана эффективность их влияния на сердечно-сосудистую систему у пациентов с сахарным диабетом ٢ типа (СД٢). Особое внимание уделяется многоцентровым клиническим исследованиям, которые изучали влияние гипогликемии на сердечно-сосудистые исходы у пациентов с СД2. Также в статье обобщается научный и практический опыт применения ингибиторов НГЛТ-2 у пациентов с различными нарушениями сердечного ритма, в том числе представляющими угрозу жизни для пациентов с СД٢.
Ключевые слова
Для цитирования:
Бондаренко И.З., Калашников В.Ю. Кардиодиабетология: эволюция или революция? Сахарный диабет. 2025;28(1):38-45. https://doi.org/10.14341/DM13295
For citation:
Bondarenko I.Z., Kalashnikov V.Y. Cardiodiabetology: Evolution or Revolution? Diabetes mellitus. 2025;28(1):38-45. (In Russ.) https://doi.org/10.14341/DM13295
«С тех пор, как эра до инсулина и связанные с ней осложнения (ацидоз, кома) закончилась, заболевания сердца и сосудов стали главной проблемой инвалидизации и смертности у больных сахарным диабетом…»
Coronary disease in 100 autopsied diabetics.
Nathanson MH. Am J Med. 1932 (183) 495-502
Вторая половина ХХ века — золотой век кардиологии: многочисленные многоцентровые, плацебо-контролируемые исследования демонстрируют феноменальные успехи статинов, бета-адреноблокаторов, блокаторов ренин-ангиотензин-альдостероновой системы (РААС) в улучшении сердечно-сосудистого прогноза и увеличении продолжительности жизни, в том числе в популяции диабета. В это же время появились технологии в лечении ишемической болезни сердца (ИБС) — интервенционная кардиология. Усовершенствовалось антитромботическое сопровождение чрескожных вмешательств на артериях сердца, что позволило существенно снизить осложнения хирургического лечения у больных сахарным диабетом (СД). А в эндокринологии было относительное затишье: хотя влияние СД на утяжеление сердечно-сосудистого прогноза активно изучалось со времен Фремингемского исследования, эффективность сахароснижающей терапии в большей степени оценивалась по ее способности осуществлять метаболический контроль и не вызывать тяжелую гипогликемию, негативные последствия которой уже были хорошо известны.
В 20-е годы прошлого столетия был выпущен первый инсулин животного происхождения, а позже налажено его массовое производство. Это позволило существенно снизить смертельные исходы от кетоацидоза и кетоацидотической комы. Данное событие было поистине революционным.
До появления инсулина связь диабета с атеросклерозом была практически не известна. Фремингемское исследование, начатое в 1948 г. и продолжающееся в настоящее время, было первым крупным эпидемиологическим исследованием, показавшим высокий риск развития атеросклероза и хронической сердечной недостаточности (ХСН) в популяции СД [1].
Ряд клинических исследований продемонстрировал достоверно более высокий риск развития СД у пациентов с ХСН, что, по-видимому, связано с нарушением чувствительности к инсулину: чем более выражена инсулинорезистентность, тем агрессивнее клинические проявления сердечной недостаточности. В масштабном исследовании CHARM почти у 8% пациентов с ХСН за 3 года наблюдения развился СД 2 типа (СД2). Тяжесть ХСН прямо коррелировала с вероятностью заболеть диабетом [2]. В свою очередь у пациентов с СД2 в сравнении с пациентами без диабета более тяжело протекают клинические проявления ХСН даже при сходных показателях ремоделированного миокарда. В исследовании PARADIGM-HF у пациентов с ХСН СД2 не был диагностирован в 13% случаев, преддиабет — в 25% случаев [3]. В исследовании CHARM СД не распознан с одинаковой частотой как у пациентов с сохраненной, так и сниженной фракцией выброса левого желудочка (ЛЖ) [4].
По данным исследования DIABHYCAR [5], смертность больных СД2 при наличии ХСН оказалась в 12 раз выше, чем в отсутствие ХСН. Наиболее частые побочные эффекты в виде развития гипогликемии наблюдались у пациентов, получавших инсулин и/или производные сульфонилмочевины. У них же чаще развивались неблагоприятные сердечно-сосудистые исходы. Именно гипогликемия расценивалась как пусковой механизм для развития ишемии миокарда или нарушения мозгового кровообращения.
Помимо инсулина, в арсенале эндокринолога оставались метформин, тиазолидиндионы, препараты сульфонилмочевины [6].
Метформин длительное время занимал позицию первой линии в лечении пациентов с СД как эффективный и безопасный в плане развития гипогликемии. Метформин безопасен у пациентов с ХСН, участвует в снижении уровня триглицеридов, тканевого активатора плазминогена и фибриногена, С-реактивного белка. В проспективном исследовании UKPDS у пациентов с СД2 и избыточным весом, рандомизированных на прием метформина и плацебо, в группе его применения снижался относительный риск смертности от всех причин на 36%, от инфаркта миокарда (ИМ) — на 39% [7].
Тиазолидиндионы активируют ядерные рецепторы и стимулируют пролиферацию пероксисом (PPARs). Среди тиазолидиндионов пиоглитазон оказывает антиатеросклеротическое действие в сосудистой стенке: в проспективном клиническом исследовании применения пиоглитазона — PROactive, в котором участвовали 5238 пациентов с СД2 и сердечно-сосудистыми заболеваниями (ССЗ), в группе пациентов с ранее перенесшими ИМ, отмечалось достоверное снижение риска фатального ИМ на 28%, острого коронарного синдрома — на 37% [8]. Пиоглитазон также оказывает прямое протективное действие на уровне мозгового кровообращения: у пациентов с инсулинорезистентностью без диабета с недавно перенесенным острым нарушением мозгового кровообращения (ОНМК) на фоне его применения снижался показатель конечной точки (фатальный или нефатальный инсульт, ИМ) на 26% [9]. Важен и тот факт, что данная группа препаратов существенно не влияет на развитие гипогликемии. Однако способность тиазолидиндионов ухудшать прогноз ХСН за счет гиперволемии, что приводит к повышению веса и появлению отеков, существенно ограничивает их применение у пациентов с ССЗ в популяции СД2.
Производные сульфонилмочевины способны снизить уровень гликемии до опасного значения у пациентов с СД2, имеющих ССЗ. Они стимулируют секрецию инсулина, а значит, могут вызывать гипогликемию. Инсулинотропный механизм опосредуется через блокирование АТФ-чувствительных калиевых каналов в β-клетках поджелудочной железы. Однако такие каналы находятся и в миоцитах. Открытые АТФ-зависимые калиевые каналы в миокарде приводят к повышению устойчивости сердечной мышцы к повторяющимся эпизодам ишемии, а их закрытие — к ухудшению кровоснабжения сердца [10]. Глибенкламид блокирует все виды K+АТФ-каналов, в том числе в миокарде. В свою очередь гликлазид и глимеперид не повреждают этот механизм, т.е. не закрывают АТФ-зависимые каналы в миокарде. Этот факт надо учитывать при выборе препаратов сульфонилмочевины у пациентов с СД и ССЗ.
Инсулин остается самым главным «виновником» развития гипогликемии, а значит, потенциально опасен при компенсации углеводного обмена у пациентов с СД и ССЗ. В исследовании DIGAMI, результаты которого были опубликованы в 1997 г., было показано, что интенсивное лечение инсулином пациентов с СД2 и острым ИМ снизило смертность в течение года на 30% [11]. Но результаты исследования DIGAMI 2, опубликованные в 2005 г., не подтвердили факт, что длительное лечение инсулином, начатое в кардиореанимации, улучшает выживаемость пациентов с СД2 после ИМ.
Помимо DIGAMI и DIGAMI 2, несколько эпохальных исследований в диабетологии начала ХХI века проанализировали влияние гипогликемии на сердечно-сосудистые исходы на фоне ужесточения метаболического контроля (табл. 1 и 2). Обращает на себя внимание, что исследования не были стандартизированы по параметрам гипогликемии: уровень гипогликемии был разный, а в исследовании ACCORD вообще не определен. Именно исследование ACCORD было досрочно прекращено по этическим соображениям, так как значимо выросли сердечно-сосудистая и общая смертность.
Таблица 1. Сердечно-сосудистые исходы вследствие развития гипогликемий у пациентов с сахарным диабетом 2 типа в исследованиях ACCORD, ADVANCE, VADT
|
Название исследования |
Популяция пациентов |
Определение гипогликемии |
Группа интенсивного контроля (%) |
Группа контроля (%) |
Заболевание и смертность |
|
ACCORD |
10 251 амбулаторный пациент с СД2 и ССЗ или факторами риска ССЗ |
Уровень гипогликемии, требующий посторонней помощи |
3,1% за год |
1% за год |
Исследование ДОСРОЧНО ОСТАНОВЛЕНО через 3,5 года наблюдения в связи с увеличением общей смертности на 22% и сердечно-сосудистой смертности на 35% в группе интенсивного контроля |
|
ADVANCE |
11 140 амбулаторных пациентов с СД2 |
≤2,8 ммоль/л ИЛИ типичные симптомы гипогликемии |
2,7% (как минимум с одним тяжелым эпизодом гипо) |
1,5% |
По сравнению с исследованием ACCORD длительность, уровень НbА1с меньше, а также значительно меньше пациентов на инсулине |
|
VADT |
1791 амбулаторный пациент с СД2 |
Не определена |
24,1% |
17,6% |
Через 5,6 года наблюдения не было значимых различий по уровню общей и сердечно-сосудистой смертности в обеих группах |
Примечание. HbA1c — гликированный гемоглобин; СД2 — сахарный диабет 2 типа; ССЗ — сердечно-сосудистые заболевания.
Таблица 2. Сердечно-сосудистые исходы вследствие развития гипогликемий у пациентов с сахарным диабетом 2 типа в условиях кардиореанимации в исследованиях NICE-SUGAR, VISEP, GLUCONTROL
|
Название исследования |
Популяция пациентов |
Определение гипогликемии |
Группа интенсивного контроля (%) |
Группа контроля (%) |
Заболевание и смертность |
|
NICE-SUGAR |
6104 пациента с СД2, которым потребовалась госпитализация в ОРИТ от 3 и более суток |
≤2,2 ммоль/л |
6,8% за год |
0,5% за год |
Нет различий по длительности госпитализации ВЫШЕ смертность в группе интенсивного лечения |
|
VISEP |
537 пациентов с тяжелым сепсисом |
≤2,2 ммоль/л |
17% |
4,1% |
Тенденция к увеличению длительности пребывания в ОРИТ Нет различий в смертности |
|
GLUCOCONTROL |
1101 пациент с СД2, находящийся в ОРИТ |
≤2,2 ммоль/л |
8,7% |
2,7% |
Уровни смертности одинаковые в обеих группах |
Примечание. СД2 — сахарный диабет 2 типа; ОРИТ — отделение реанимации и интенсивной терапии.
В большинстве приведенных исследований гипогликемии преобладали в группах интенсивного лечения, где чаще развивались сердечно-сосудистые осложнения.
До начала XXI века в диабетологии в основном применялись инсулины и ранее перечисленные группы сахароснижающих препаратов. В рамках своих «одноклассников» они эволюционировали, усовершенствовались в плане метаболического контроля, и предпочтение в лечении отдавалось более безопасным. В первом десятилетии XXI века практически одновременно стартовали многоцентровые рандомизированные контролируемые исследования (РКИ) с принципиально другими механизмами снижения гликемии. Именно безопасность новых сахароснижающих препаратов становится ключевым параметром по требованию FDA, согласно которому фармакологическая компания-производитель должна продемонстрировать, что новое лекарственное вещество не приводит к повышению сердечно-сосудистых событий в клинических исследованиях 2–3 фазы. Более того, обязательным условием было включение пациентов высокого риска (с ИБС, хронической болезнью почек (ХБП), пожилые). Продолжительность исследования должна была быть не менее 2 лет. В целом, революционными были два факта: включение коморбидных пациентов, а также использование критериев безопасности, характерных для сердечно-сосудистых РКИ, что было принципиально новым в истории многоцентровых исследований.
ЭРА ИНГИБИТОРОВ ДПП-4, АГОНИСТОВ РЕЦЕПТОРОВ ГПП-1, ИНГИБИТОРОВ НГЛТ-2
Чуть более 10 лет назад были опубликованы первые итоги трех мультицентровых рандомизированных, двойных слепых, плацебо-контролируемых исследований по эффективности метаболического контроля в популяции пациентов с СД2, принимающих ингибиторы дипептидилпептидазы-4 (ДПП-4) в сравнении с плацебо: EXAMINE [12] включило в свое исследование 5380 пациентов, SAVOR-TIMI [13] — 5380 пациентов, TECOS [14] — 14 724 пациента. Длительность РКИ составила от 7,5 до 10 лет. По требованию FDA в РКИ были включены и пациенты высокого сердечно-сосудистого риска. Первичные конечные точки (сердечно-сосудистая смерть, нефатальный ИМ или нефатальный инсульт) были стандартными для РКИ, оценивающих эффективность кардиологических препаратов, поэтому представляли большой интерес для кардиологов. Вторичные конечные точки оценивали по количеству госпитализаций по причине декомпенсации ХСН. Стадия ХСН определялась по уровню натрийуретического пептида (proBNP). Только в исследовании SAVOR-TIMI наблюдалось небольшое, но статистически значимое увеличение количества госпитализаций, связанных с прогрессированием ХСН (1,27 95% доверительный интервал (ДИ) 1,07–1,51, р=0,007). При этом класс-эффект по отсутствию гипогликемий был продемонстрирован во всех исследованиях. Исследования EXAMINE и TECOS показали не только эффективность в контроле гликемии, но и сердечно-сосудистую безопасность у пациентов высокого сердечно-сосудистого риска. Различное влияние ингибиторов ДПП-4 на кардиальные исходы, наиболее вероятно, было связано с особенностями дизайна, несопоставимостью пациентов по тяжести ССЗ, а также фармакокинетическими и фармакодинамическими особенностями молекул ингибиторов ДПП-4.
В эндокринной кардиологии эта группа препаратов была принята спокойно, как еще один класс сахароснижающих препаратов, безопасных, но не дающих какого-либо преимущества в лечении пациентов с СД2 и ССЗ.
В это же время появились результаты РКИ по изучению агонистов рецепторов глюкагоноподобного пептида-1 (арГПП-1). Во всех трех исследованиях по изучению ликсисенатида [15], лираглутида [16] и семаглутида [17] была подтверждена безопасность для пациентов с СД2 и ХСН, но впервые были выявлены преимущества для пациентов с ССЗ: в исследовании LEADER [16] наблюдалось уменьшение первичной конечной комбинированной точки на 13%, смертности от сердечно-сосудистых заболеваний на 22%, в исследовании SUSTAIN-6 [17] — семаглутид позволил уменьшить время до нефатального ИМ, нефатального инсульта и сердечно-сосудистой смерти, а также снизить время до реваскуляризации миокарда, и это снижение не зависело от исходного сердечно-сосудистого статуса.
В исследовании SUSTAIN-6, первые результаты которого были опубликованы чуть менее 10 лет назад, подтверждена основная гипотеза, что у пациентов, принимавших семаглутид, риск основного комбинированного исхода, включающего смерть от ССЗ, нефатальный ИМ или нефатальный инсульт, был значимо ниже, чем у пациентов, принимавших плацебо. Частота смертей от ССЗ заболеваний при этом не изменилась. Таким образом, арГПП-1 являются ключевыми сахароснижающими препаратами, которые должны входить в схему лечения коморбидных пациентов с СД2 и ССЗ.
Одновременно с LEADER первое исследование ингибитора натрийзависимого переносчика глюкозы 2-го типа (НГЛТ-2) (EMPA-REG Outcome) доказало преимущество по безопасности влияния на сердечно-сосудистую систему препарата эмпаглифлозина (табл. 3).
Таблица 3. Основные результаты исследований EMPA-REG OUTCOME (препарат эмпаглифлозин) и LEADER (препарат лираглутид)
|
EMPA REG OUTCOME |
LEADER |
|
|
Первичная конечная точка: 3 основных нежелательных сердечно-сосудистых события — сердечно-сосудистая смерть, нефатальный ИМ, нефатальный инсульт |
-14% (р=0,0382) |
-13% (р≤0,01) |
|
Инфаркт миокарда |
-13% (p=NS) |
-12% (p=NS) |
|
Инсульт |
-24% (p=NS) |
-11% (p=NS) |
|
Сердечно-сосудистая смерть |
-38% (p<0,0001) |
-22% (p=0,007) |
|
Общая смертность |
-32% (p<0,0001) |
-15% (p=0,02) |
|
Госпитализация по поводу ХСН |
-35% (p<0,002) |
-13% (p=0,02) |
|
Новые случаи или прогрессирование нефропатии |
-39% (p=0,001) |
Нет данных |
|
Прогрессирование макроальбуминурии |
-38% (p<0,001) |
-26% (p<0,05) |
|
Удвоение уровня креатинина в крови |
-44% (p=0,001) |
-14% (p=NS) |
|
Показания к трансплантации почек |
-55% (p=0,001) |
-13% (p=NS) |
|
Удвоение уровня креатинина, показание к трансплантации почек или смерть по почечным причинам |
-46% (p=0,001) |
Нет данных |
Примечание. NS — статистически не значимые различия ("not significant"); ИМ — инфаркт миокарда; ХСН — хроническая сердечная недостаточность.
В сентябре 2015 г. в Стокгольме на конгрессе Европейской ассоциации по изучению диабета (EASD) были представлены результаты исследования EMPA-REG Outcome [18]. Исследование исходно было спланировано как изучение сахароснижающего эффекта эмпаглифлозина, но по критериям FDA последний превратился в лекарственный препарат с выраженной кардиопротективной активностью. На фоне эмпаглифлозина наблюдалось достоверное снижение первичной конечной точки, смертности от сердечно-сосудистых причин, общей смертности, а также почечных исходов. Огромным достижением всех ингибиторов НГЛТ-2 является «класс-эффект» по снижению случаев госпитализации с декомпенсацией ХСН, самой тяжелой и прогностически неблагоприятной популяции пациентов. Другие представители этого класса — канаглифлозин и дапаглифлозин также эффективны в снижении случаев госпитализации по причине декомпенсации ХСН (табл. 4).
Таблица 4. Ингибиторы натрий-глюкозного котранспортера-2 — снижение сердечно-сосудистых рисков
|
Конечные точки |
|||||
|
3 МАСЕ |
СС смертность |
Общая смертность |
Госпитализация по причине ХСН |
||
|
Снижение АР |
Снижение ОР |
||||
|
Эмпаглифлозин |
1,6%* |
14%* |
38%* |
32%* |
35%* |
|
Канаглифлозин |
1,5%* |
14%* |
13% |
13% |
33%* |
|
Дапаглифлозин |
0,6% |
7% |
2% |
7% |
27%* |
|
Эртуглифлозин |
0% |
0% |
0% |
8% |
30%* |
Примечание. * — «достоверно». МАСЕ —серьезные сердечно-сосудистые события; АР — абсолютный риск; ОР — относительный риск; СС смертность — сердечно-сосудистая смертность; ХСН — хроническая сердечная недостаточность.
ХСН не только ухудшает качество жизни, но и является прогрессирующим заболеванием, которое требует последующих госпитализаций и сопровождается снижением функции почек.
Дапаглифлозин и эмпаглифлозин продолжают доказывать свое преимущество в улучшении сердечно-сосудистого прогноза как у пациентов с СД2, так и без СД, у пациентов со сниженной и сохраненной фракцией выброса левого желудочка (ЛЖ), с нарушением функции почек. Этому вопросу посвящены масштабные программы DAPA и EMPOWER, включающие в себя по несколько клинических исследований, в том числе в условиях реальной клинической практики. Результаты исследований с участием ингибиторов НГЛТ-2 [19] совершили революционные изменения как в диабетологии, так и в кардиологии. Благодаря результатам этих программ оба препарата вошли во все российские, американские и европейские рекомендации как приоритетные у пациентов с ССЗ, особенно с ХСН [20].
ИНГИБИТОРЫ НГЛТ-2 И НАРУШЕНИЯ РИТМА СЕРДЦА
Появились данные о положительном влиянии ингибиторов НГЛТ-2 на нарушения ритма сердца. У пациентов с СД2 риск развития фибрилляции предсердий (ФП) на 49% выше, а риск внезапной сердечной смерти — более чем в 2 раза выше по сравнению с пациентами без СД [21]. Распространенность ФП у пациентов с ХСН увеличивается параллельно с тяжестью недостаточности кровообращения: от 10 до 26% у пациентов с ХСН с сохраненной или умеренно сниженной фракцией выброса ЛЖ (ФВЛЖ), и до 50% — у пациентов с ХСН и низкой ФВЛЖ. Внезапная сердечная смерть в последней популяции развивается у 1/3 пациентов [22].
Ранее проведенные исследования показали, что ингибиторы НГЛТ-2 могут улучшать энергетический обмен в миокарде [23], подавлять воспаление, снижать окислительный стресс, а также предотвращать патологическое ремоделирование миокарда [24], что лежит в основе его беспрецедентного влияния на снижение числа госпитализаций по причине декомпенсации ХСН. Можно предположить, что эти же механизмы принимают участие в предотвращении жизнеугрожающих аритмий.
Для подтверждения этой гипотезы в 2024 г. был проведен крупный метаанализ с включением 33 плацебо-контролируемых РКИ и с участием 88 098 пациентов (48 585 в группе, получающей ингибиторы НГЛТ-2, и 39 513 в группе плацебо). Средний возраст составил 64,9±9,4 года. Среднее время наблюдения составило 1,4±1,1 года [25].
Объединенные результаты показали, что лечение ингибиторами НГЛТ-2 коррелировало со значительно более низким риском развития ФП [ коэффициент риска (RR): 0,88, 95% доверительный интервал (CI): 0,78–1,00, P=0,04], в том числе у пациентов, имеющих как ФП, так и трепетание предсердий (ТП): RR: 0,86, 95% CI: 0,77–0,96, P=0,01. Этот благоприятный эффект был наиболее выражен у пациентов с ХСН и сохраненной ФВЛЖ (СНсФВ), у лиц мужского пола, а также у принимающих дапаглифлозин более 1 года. Только у пациентов с ХСН прием ингибиторов НГЛТ-2 коррелировал с незначительным снижением риска внезапной смерти (ОР: 0,67, P=0,05). Существенного влияния на другие виды аритмии выявлено не было [22].
ПРЕДПОЛАГАЕМЫЕ МЕХАНИЗМЫ ЗАЩИТНЫХ ЭФФЕКТОВ ИНГИБИТОРОВ НГЛТ-2 ПРИ ПРЕДСЕРДНЫХ АРИТМИЯХ
Эмпаглифлозин уменьшает структурное ремоделирование предсердий, снижает митохондриальную дисфункцию, что потенциально может быть использовано для профилактики ФП у пациентов с СД2 [26]. Чрезмерная активация Ca2+/кальмодулин-зависимой киназы II (CaMKII) является ключевым клеточным механизмом развития ХСН, приводящим к дисфункции сократительной способности миокарда и, как следствие, к аритмиям. Ингибиторы НГЛТ-2 способны блокировать активность CaMKII и CaMKII-зависимую эвакуацию Ca2+ из саркоплазматического ретикулума, что может стать основой протективного действия ингибиторов НГЛТ-2 на сократительную функцию сердца. Кроме того, ингибиторы НГЛТ-2 подавляют активность симпатической нервной системы и уменьшают воспалительные процессы в перивисцеральной жировой ткани, что также приводит к антиаритмическому эффекту [27].
Снижение риска развития ФП является важной целью для пациентов с ХСН. Наиболее вероятно, что на фоне лечения ингибиторами НГЛТ-2 уменьшается вероятность развития предсердных аритмий вне зависимости от компенсации ХСН.
ИНГИБИТОРЫ НГЛТ-2 И ЖЕЛУДОЧКОВЫЕ АРИТМИИ
Было доказано, что ингибиторы НГЛТ-2 снижают смертность от всех причин и сердечно-сосудистую смертность у пациентов независимо от наличия СД2, ХСН и ХБП, однако связь между ингибиторами НГЛТ-2 и желудочковыми аритмиями изучена мало. Согласно приведенному метаанализу [25], не обнаружено существенных различий в частоте желудочковых тахиаритмий, в том числе в возникновении фибрилляции желудочков и внезапной сердечной смерти между группами принимавших и не принимавших ингибиторы НГЛТ-2. В то же время только у пациентов с ХСН прием ингибиторов НГЛТ-2 был связан с незначительным снижением риска внезапной сердечной смерти.
В исследовании DAPA-HF применение ингибитора НГЛТ-2 дапаглифлозина привело к снижению частоты жизнеугрожающих желудочковых аритмий (желудочковая тахикардия, фибрилляция желудочков, пируэтная тахикардия) и уменьшению числа реанимационных мероприятий и случаев внезапной сердечной смерти (5,9% против 7,4%, ОР: 0,79, P=0,037) [28]. Следует отметить, что в исследовании DAPA-HF у всех пациентов была ХСН со сниженной ФВЛЖ (31±7%), а у 55% диагностирована ишемическая кардиомиопатия, т.е. включались больные с неблагоприятным прогнозом.
Клинически значимым является тот факт, что ингибиторы НГЛТ-2 снижают риск внезапной сердечной смерти только у пациентов с ХСН. Можно предположить, что влияние ингибиторов НГЛТ-2 на снижение риска внезапной сердечной смерти (или злокачественных желудочковых аритмий) может быть более выраженным у пациентов с высоким риском сердечно-сосудистых осложнений. В то же время статистическая мощность исследований в отношении ФП, внезапной сердечной смерти и внезапной сердечной смерти с успешной реанимацией пока недостаточна для оценки связи между ингибиторами НГЛТ-2, желудочковыми аритмиями и/или внезапной сердечной смертью. Необходимы дальнейшие исследования.
ЗАКЛЮЧЕНИЕ
Нет сомнения, что новые классы сахароснижающих препаратов, такие как арГПП-1 и ингибиторы НГЛТ-2, появившиеся в течение последнего десятилетия, перевернули страницу не только в диабетологии и кардиологии, но и в самих подходах к лечению пациентов с СД2 и ССЗ. Эти изменения нашли свое отражение в Алгоритмах медицинской специализированной помощи больным СД [29]: гликемический контроль у пациентов с заболеваниями, ассоциированными с атеросклерозом, осуществляется с помощью дополнительного назначения именно этих лекарственных групп как снижающих риск развития неблагоприятных сердечно-сосудистых событий. У пациентов с СД и ХСН с низкой ФВЛЖ предпочтение отдается ингибиторам НГЛТ-2. В последних рекомендациях Американской диабетологической ассоциации [30] также подчеркнута важность выбора терапии диабета, которая обеспечивает не только гипогликемическую эффективность, но и достигает нескольких целей лечения, включая улучшение сердечно-сосудистых и почечных исходов, исключения риска гипогликемии, снижение веса (класс рекомендаций А). У пациентов с ожирением с атеросклеротическими ССЗ предпочтение отдается арГПП-1 (А), а при наличии ХСН — вне зависимости от величины ФВ — ингибиторам НГЛТ-2 (А). У пациентов с ХБП (расчетная скорость клубочковой фильтрации (рСКФ) 20–60 мл/мин/1,73 м² и/или с альбуминурией наиболее эффективны ингибиторы НГЛТ-2 (класс доказательности А). Находясь на верхней ступеньке иерархии лекарственных средств (рис. 1), данные группы препаратов, успешно применяемые в диабетологии и кардиологии, остаются пока недостаточно изученными по своим резервам влиять на прогноз при других заболеваниях сердца, например, при заболеваниях проводящей системы в миокарде. Возможный потенциал такого действия продолжает изучаться.
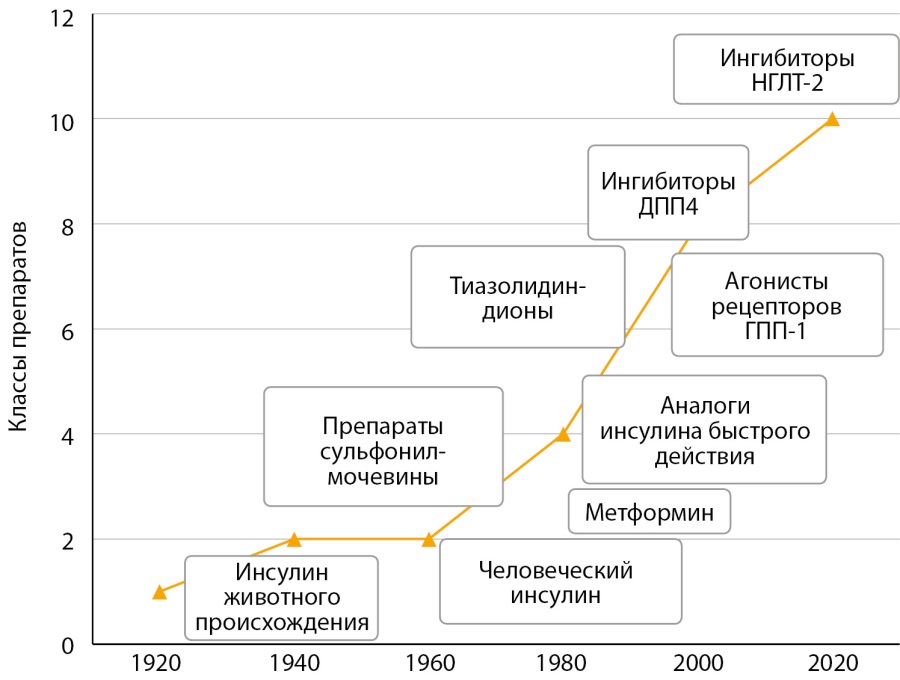
Рисунок 1. Эволюция сахароснижающей терапии за последние 100 лет.
ДОПОЛНИТЕЛЬНАЯ ИНФОРМАЦИЯ
Источник финансирования. Работа выполнена без привлечения финансирования.
Конфликт интересов. Авторы декларируют отсутствие явных и потенциальных конфликтов интересов, связанных с содержанием настоящей статьи.
Вклад авторов. Бондаренко И.З. — сбор и анализ материала, написание текста статьи; Калашников В.Ю. — сбор и анализ материала, внесение существенных правок в текст статьи. Все авторы одобрили финальную версию статьи перед публикацией, выразили согласие нести ответственность за все аспекты работы, подразумевающую надлежащее изучение и решение вопросов, связанных с точностью или добросовестностью любой части работы.
Список литературы
1. McKee PA, Castelli WP, McNamara PM, Kannel WB. The natural history of congestive heart failure: the Framingham study. N Engl J Med. 1971;285(26):1441-1446. doi: https://doi.org/10.1056/NEJM197112232852601
2. Preiss D, Zetterstrand S, McMurray JJ, et al. Predictors of development of diabetes in patients with chronic heart failure in the Candesartan in Heart Failure Assessment of Reduction in Mortality and Morbidity (CHARM) program. Diabetes Care. 2009;32(5):915-920. doi: https://doi.org/10.2337/dc08-1709
3. Kristensen SL, Preiss D, Jhund PS, et al. Risk Related to Pre-Diabetes Mellitus and Diabetes Mellitus in Heart Failure With Reduced Ejection Fraction: Insights From Prospective Comparison of ARNI With ACEI to Determine Impact on Global Mortality and Morbidity in Heart Failure Trial. Circ Heart Fail. 2016;9(1):e002560. doi: https://doi.org/10.1161/CIRCHEARTFAILURE.115.002560
4. Kristensen SL, Jhund PS, Lee MMY, et al. Prevalence of Prediabetes and Undiagnosed Diabetes in Patients with HFpEF and HFrEF and Associated Clinical Outcomes. Cardiovasc Drugs Ther. 2017;31(5-6):545-549. doi: https://doi.org/10.1007/s10557-017-6754-x
5. Marre M, Lievre M, Chatellier G, et al. Effects of low dose ramipril on cardiovascular and renal outcomes in patients with type 2 diabetes and raised excretion of urinary albumin: randomised, double blind, placebo controlled trial (the DIABHYCAR study) [published correction appears in BMJ. 2004 Mar 20;328(7441):686]. BMJ. 2004;328(7438):495. doi: https://doi.org/10.1136/bmj.37970.629537.0D
6. Nissen SE, Wolski K. Effect of rosiglitazone on the risk of myocardial infarction and death from cardiovascular causes [published correction appears in N Engl J Med. 2007 Jul 5;357(1):100.]. N Engl J Med. 2007;356(24):2457-2471. doi: https://doi.org/10.1056/NEJMoa072761
7. Effect of intensive blood-glucose control with metformin on complications in overweight patients with type 2 diabetes (UKPDS 34). UK Prospective Diabetes Study (UKPDS) Group [published correction appears in Lancet 1998 Nov 7;352(9139):1558]. Lancet. 1998;352(9131):854-865
8. Dormandy JA, Charbonnel B, Eckland DJ, et al. Secondary prevention of macrovascular events in patients with type 2 diabetes in the PROactive Study (PROspective pioglitAzone Clinical Trial In macroVascular Events): a randomised controlled trial. Lancet. 2005;366(9493):1279-1289. doi: https://doi.org/10.1016/S0140-6736(05)67528-9
9. Kernan WN, Viscoli CM, Furie KL, et al. Pioglitazone after Ischemic Stroke or Transient Ischemic Attack. N Engl J Med. 2016;374(14):1321-1331. doi: https://doi.org/10.1056/NEJMoa1506930
10. Schmidt MR, Smerup M, Konstantinov IE, et al. Intermittent peripheral tissue ischemia during coronary ischemia reduces myocardial infarction through a KATP-dependent mechanism: first demonstration of remote ischemic perconditioning. Am J Physiol Heart Circ Physiol. 2007;292(4):H1883-H1890. doi: https://doi.org/10.1152/ajpheart.00617.2006
11. Malmberg K, Rydén L, Hamsten A, Herlitz J, Waldenström A, Wedel H. Mortality prediction in diabetic patients with myocardial infarction: experiences from the DIGAMI study [published correction appears in Cariovasc Res 1997 Dec;36(3):460]. Cardiovasc Res. 1997;34(1):248-253. doi: https://doi.org/10.1016/s0008-6363(96)00263-5
12. Ponikowski P, Voors AA, Anker SD, et al. 2016 ESC Guidelines for the diagnosis and treatment of acute and chronic heart failure: The Task Force for the diagnosis and treatment of acute and chronic heart failure of the European Society of Cardiology (ESC). Developed with the special contribution of the Heart Failure Association (HFA) of the ESC. Eur J Heart Fail. 2016;18(8):891-975. doi: https://doi.org/10.1002/ejhf.592
13. Scirica BM, Bhatt DL, Braunwald E, et al. Saxagliptin and cardiovascular outcomes in patients with type 2 diabetes mellitus. N Engl J Med. 2013;369(14):1317-1326. doi: https://doi.org/10.1056/NEJMoa1307684
14. Standards of medical care in diabetes — 2015: summary of revisions. Diabetes Care. 2015;38Suppl:S4. doi: https://doi.org/10.2337/dc15-S003
15. Pfeffer MA, Claggett B, Diaz R, et al. Lixisenatide in Patients with Type 2 Diabetes and Acute Coronary Syndrome. N Engl J Med. 2015;373(23):2247-2257. doi: https://doi.org/10.1056/NEJMoa1509225
16. Buse JB; the LEADER Steering Committee. Liraglutide and Cardiovascular Outcomes in Type 2 Diabetes. N Engl J Med. 2016;375(18):1798-1799. doi: https://doi.org/10.1056/NEJMc1611289
17. Marso SP, Bain SC, Consoli A, et al. Semaglutide and Cardiovascular Outcomes in Patients with Type 2 Diabetes. N Engl J Med. 2016;375(19):1834-1844. doi: https://doi.org/10.1056/NEJMoa1607141
18. Zinman B, Wanner C, Lachin JM, et al. Empagliflozin, Cardiovascular Outcomes, and Mortality in Type 2 Diabetes. N Engl J Med. 2015;373(22):2117-2128. doi: https://doi.org/10.1056/NEJMoa1504720
19. Lytvyn Y, Bjornstad P, Udell JA, Lovshin JA, Cherney DZI. Sodium Glucose Cotransporter-2 Inhibition in Heart Failure: Potential Mechanisms, Clinical Applications, and Summary of Clinical Trials. Circulation. 2017;136(17):1643-1658. doi: https://doi.org/10.1161/CIRCULATIONAHA.117.030012
20. McDonagh TA, Metra M, Adamo M, et al. 2021 ESC Guidelines for the diagnosis and treatment of acute and chronic heart failure [published correction appears in Eur Heart J. 2021 Dec 21;42(48):4901. doi: 10.1093/eurheartj/ehab670]. Eur Heart J. 2021;42(36):3599-3726. doi: https://doi.org/10.1093/eurheartj/ehab368
21. Zeppenfeld K, Tfelt-Hansen J, de Riva M, et al. 2022 ESC Guidelines for the management of patients with ventricular arrhythmias and the prevention of sudden cardiac death. Eur Heart J. 2022;43(40):3997-4126. doi: https://doi.org/10.1093/eurheartj/ehac262
22. Packer M. What causes sudden death in patients with chronic heart failure and a reduced ejection fraction? Eur Heart J. 2020;41(18):1757-1763. doi: https://doi.org/10.1093/eurheartj/ehz553
23. Ferrannini E, Baldi S, Frascerra S, et al. Shift to Fatty Substrate Utilization in Response to Sodium-Glucose Cotransporter 2 Inhibition in Subjects Without Diabetes and Patients With Type 2 Diabetes. Diabetes. 2016;65(5):1190-1195. doi: https://doi.org/10.2337/db15-1356
24. Ferrannini E, Muscelli E, Frascerra S, et al. Metabolic response to sodium-glucose cotransporter 2 inhibition in type 2 diabetic patients [published correction appears in J Clin Invest. 2014 Apr 1;124(4):1868]. J Clin Invest. 2014;124(2):499-508. doi: https://doi.org/10.1172/JCI72227
25. Liao J, Ebrahimi R, Ling Z, et al. Effect of SGLT-2 inhibitors on arrhythmia events: insight from an updated secondary analysis of > 80,000 patients (the SGLT2i-Arrhythmias and Sudden Cardiac Death). Cardiovasc Diabetol. 2024;23(1):78. doi: https://doi.org/10.1186/s12933-024-02137-x
26. Habibi J, Aroor AR, Sowers JR, et al. Sodium glucose transporter 2 (SGLT2) inhibition with empagliflozin improves cardiac diastolic function in a female rodent model of diabetes. Cardiovasc Diabetol. 2017;16(1):9. doi: https://doi.org/10.1186/s12933-016-0489-z
27. Sato T, Aizawa Y, Yuasa S, et al. The effect of dapagliflozin treatment on epicardial adipose tissue volume. Cardiovasc Diabetol. 2018;17(1):6. doi: https://doi.org/10.1186/s12933-017-0658-8
28. Curtain JP, Docherty KF, Jhund PS, et al. Effect of dapagliflozin on ventricular arrhythmias, resuscitated cardiac arrest, or sudden death in DAPA-HF. Eur Heart J. 2021;42(36):3727-3738. doi: https://doi.org/10.1093/eurheartj/ehab560
29. Дедов И.И., Шестакова М.В., Майоров А.Ю., и др. Алгоритмы специализированной медицинской помощи больным сахарным диабетом / Под редакцией И.И. Дедова, М.В. Шестаковой, А.Ю. Майорова. 11-й выпуск // Сахарный диабет. — 2023. — Т.26. — №2S. — С.1-157. doi: https://doi.org/10.14341/DM13042
30. American Diabetes Association Professional Practice Committee; Introduction and Methodology: Standards of Care in Diabetes—2025. Diabetes Care. 2025;48(S1):S1–S5. doi: https://doi.org/10.2337/dc25-SINT
Об авторах
И. З. БондаренкоРоссия
Бондаренко Ирина Зиятовна, д.м.н.
117036, Москва, ул. Дм. Ульянова, д. 11
В. Ю. Калашников
Россия
Калашников Виктор Юрьевич, д.м.н., профессор, член-корреспондент РАН
117036, Москва, ул. Дм. Ульянова, д. 11
Дополнительные файлы
|
|
1. Рисунок 1. Эволюция сахароснижающей терапии за последние 100 лет. | |
| Тема | ||
| Тип | Исследовательские инструменты | |
Посмотреть
(191KB)
|
Метаданные ▾ | |
Рецензия
Для цитирования:
Бондаренко И.З., Калашников В.Ю. Кардиодиабетология: эволюция или революция? Сахарный диабет. 2025;28(1):38-45. https://doi.org/10.14341/DM13295
For citation:
Bondarenko I.Z., Kalashnikov V.Y. Cardiodiabetology: Evolution or Revolution? Diabetes mellitus. 2025;28(1):38-45. (In Russ.) https://doi.org/10.14341/DM13295
JATS XML

Контент доступен под лицензией Creative Commons Attribution-NonCommercial-NoDerivatives 4.0 International License (CC BY-NC-ND 4.0).















































