Перейти к:
Анализ эффективности лечения больных с синдромом диабетической стопы в амбулаторных условиях
https://doi.org/10.14341/DM13127
Аннотация
ОБОСНОВАНИЕ. Синдром диабетической стопы (СДС) является поздним осложнением сахарного диабета (СД) и основной причиной выполнения нетравматических ампутаций нижних конечностей у больных СД. В настоящее время для лечения и профилактики данного осложнения разработаны и внедрены стандарты оказания медицинской помощи. При этом есть определенный дефицит опубликованных данных об эффективности специализированной помощи, особенно на догоспитальном этапе.
ЦЕЛЬ. Проанализировать исходы язвенных дефектов у больных СД с СДС, получающих лечение в амбулаторном режиме специализированного отделения, и выявить факторы, влияющих на них.
МАТЕРИАЛЫ И МЕТОДЫ. Были проанализированы медицинские карты пациентов с язвенными дефектами при СДС, получающих специализированное лечение в амбулаторном режиме в отделении диабетической стопы. Всем пациентам при первичном осмотре проводилась оценка состояния периферической чувствительности и магистрального кровотока. Лечение назначалось в соответствии с наличием и степенью выраженности инфекции и ишемии пораженной конечности. Анализировалось количество ампутаций на разных уровнях, процент заживших и незаживших ран в течение года. Выявлялись предикторы выполнения высоких ампутаций и отсутствия заживления в течение года.
РЕЗУЛЬТАТЫ. Из 503 пациентов с СДС нейропатическая форма была диагностирована у 336 (67%) пациентов, нейро-ишемическая — у 167 (33%). Заживление без выполнения высоких и малых ампутаций в общей когорте пациентов отмечено в 407 случаях (81%). В 32 (7%) случаях потребовалось выполнение ампутаций, из них: 23 (5%) — в пределах стопы, 3 — на уровне голени (0,6%), 6 — на уровне бедра (1,2%). Смерть констатирована у 6 пациентов (1,2%), из них у 2 после выполнения ампутации на уровне бедра. 61 пациент (12%) продолжал лечиться на момент окончания исследования. Предикторами выполнения высоких ампутаций в общей когорте больных стали возраст, нарушение магистрального кровотока в артериях нижних конечностей, глубина язвенного дефекта по Вагнеру и уровень гликированного гемоглобина. Значимыми предикторами отсутствия заживления на фоне консервативных мероприятий в течение года стали: наличие нарушенного магистрального кровотока и несвоевременное обращение за специализированной медицинской помощью.
ЗАКЛЮЧЕНИЕ. Полученные данные продемонстрировали высокую эффективность специализированной помощи больным с язвенными дефектами при СДС на догоспитальном этапе.
Ключевые слова
Для цитирования:
Комелягина Е.Ю., Анциферов М.Б. Анализ эффективности лечения больных с синдромом диабетической стопы в амбулаторных условиях. Сахарный диабет. 2024;27(4):376-383. https://doi.org/10.14341/DM13127
For citation:
Komelyagina E.Y., Antsiferov M.B. Analysis of the effectiveness of outpatient treatment of patients with diabetic foot. Diabetes mellitus. 2024;27(4):376-383. https://doi.org/10.14341/DM13127
Обоснование
Синдром диабетической стопы (СДС) — позднее осложнение сахарного диабета (СД) — является основной причиной нетравматических ампутаций нижних конечностей у больных СД, их последующей инвалидизации, стойкой утраты трудоспособности и снижением качества жизни. Основными причинами выполнения высоких ампутаций нижних конечностей при СДС являются: критическая ишемия конечности, неконтролируемая инфекция, критическая ишемия в сочетании с инфекцией [1]. Ведение пациентов с риском выполнения высоких ампутаций требует междисциплинарного взаимодействия эндокринологов, гнойных хирургов, сосудистых хирургов, ортопедов. Для снижения количества ампутаций выше голеностопного сустава предложены предикторы их выполнения: систолическое давление на тибиальных артериях пораженной конечности <50 мм рт.ст., лодыжечно-плечевой индекс (ЛПИ)<0,5, давление в пальцевой артерии <30 мм рт.ст., транскутанная оксиметрия <25 мм рт.ст. Наличие перечисленных признаков у пациента указывает на высокую вероятность выполнения ампутации нижней конечности выше голеностопного сустава и может быть основанием для проведения реваскуляризации в максимально короткие сроки [2]. Следование этим рекомендациям в реальной клинической практике привело к снижению числа высоких ампутаций во многих странах мира. По данным рандомизированных исследований в разных странах, высокие ампутации снизились на 3–85% в период 1982–2011 гг. [3]. Согласно суммарным данным по 21 стране, доля высоких ампутаций в общей популяции снизилась с 10,8 до 7,5 на 100 тыс. населения (-30,6%). 11 стран опубликовали цифры по снижению высоких ампутаций среди больных СД с 1,83 до 1,28 в пересчете на 1000 больных СД (-29,8%) [4]. В Санкт-Петербурге количество высоких ампутаций на 1000 больных СД снизилось с 2,53 в 2010 г. до 1,03 в 2021 г. [5]. Чрезвычайно важно, что в подавляющем большинстве публикаций снижение высоких ампутаций было связано с внедрением междисциплинарного подхода к лечению пациентов в стационарных условиях. Между тем большинство пациентов с СДС получают помощь в амбулаторном режиме. Кроме того, во всех странах, независимо от местных особенностей организации медицинской помощи, пациент с СДС первоначально обращается в амбулаторное учреждение. Поэтому, от того, как организована помощь на догоспитальном этапе, будет зависеть и количество экстренных госпитализаций в запущенных случаях и, соответственно, количество ампутаций. Нельзя не учитывать тот факт, что контингент больных, получающих помощь в амбулаторных и стационарных условиях, различается. Поэтому задачи, стоящие перед амбулаторной и стационарной службами, также имеют отличия. Если для стационаров ведущим показателем эффективности оказания помощи больным данной категории является количество высоких ампутаций и его динамика, то при оценке эффективности амбулаторной службы, наряду с количеством ампутаций, анализируются сроки заживления язвенных дефектов и частота их рецидивов.
Цель
Проанализировать исходы язвенных дефектов у больных СД с СДС, получающих лечение в амбулаторном режиме специализированного отделения, и выявить факторы, влияющих на них.
МАТЕРИАЛЫ И МЕТОДЫ
Место проведения
Работа была выполнена в ГБУЗ «Эндокринологический диспансер Департамента здравоохранения города Москвы».
Время исследования
Январь 2014 — декабрь 2019 гг.
Изучаемые популяции (одна или несколько).
В исследовании приняли участие пациенты, обратившиеся за специализированной помощью в отделение диабетической стопы.
Способ формирования выборки из изучаемой популяции (или нескольких выборок из нескольких изучаемых популяций).
Проанализированы амбулаторные карты пациентов, которые проходили лечение в отделении диабетической стопы с 2014 по 2019 гг. с установленным диагнозом СДС. В окончательный анализ не включались данные пациентов, не посещавших отделение в течение трех и более месяцев. Если у пациента было несколько язвенных дефектов, то с целью исключения возможного искажения результатов в анализ включались данные по одному язвенному дефекту, зафиксированному последним (рис. 1).

Рисунок 1. Когорта пациентов с синдромом диабетической стопы, вошедших в окончательный анализ.
Примечание. СДС — синдром диабетической стопы.
Дизайн исследования
Ретроспективное наблюдательное одноцентровое исследование.
Методы
Всем пациентам при первичном обращении проводилась стандартная оценка состояния периферической чувствительности и магистрального кровотока [6]. В соответствии со стандартами оказания медицинской помощи при диагностировании нейропатических язвенных дефектов ведение пациентов базировалось на следующих принципах: разгрузка пораженной конечности, антибактериальная терапия (при необходимости), местное ведение ран с использованием современных перевязочных средств и с учетом стадии течения раны. Режим разгрузки обеспечивался в нескольких вариантах: 1) обувь с разгрузкой переднего или заднего отделов стопы; 2) жесткий иммобилизирующий ортез с фиксацией голеностопного сустава; 3) индивидуальная разгружающая повязка (ИРП) в съемном или несъемном вариантах. ИРП накладывалась непосредственно на приеме [6][7].
Антибактериальная терапия назначалась при наличии местных или системных признаков инфицирования раны. Первоначальный выбор препарата проводился эмпирически на основании клинических и эпидемиологических данных о преобладающих возбудителях, степени тяжести инфекционного процесса, наличия и степени выраженности нефропатии, нейропатии, аллергических реакций, предшествующих госпитализаций. Предпочтения отдавались антибактериальным средствам широкого спектра действия: защищенным пенициллинам (амоксициллин/клавуланат, амоксициллин/сульбактам, ампициллин/сульбактам), фторхинолонам (левофлоксацин, ципрофлоксацин) в таблетированном режиме приема. При отсутствии эффекта терапия корректировалась с учетом результатов бактериологического исследования [6][8][9].
Местное лечение ран состояло из их очищения, промывания, применения перевязочного средства. Очищение раны заключалось в удалении некроза, участков окружающего гиперкератоза. Объем вмешательства определялся состоянием раневого дефекта: некротизированные ткани удалялись скальпелем, ложкой Фолькмана за один прием или путем поэтапной обработки. С целью удаления инородных частиц, поверхностных нежизнеспособных наслоений, остатков предыдущих раневых покрытий, рана промывалась раствором антисептика (хлоргексидин 0,05%) либо физиологическим раствором. На завершающем этапе на рану накладывалось перевязочное средство. Выбор перевязочного средства основывался на стадии раневого процесса и уровне экссудации. Применялись многокомпонентные мази на водорастворимой основе, альгинатные перевязочные средства, гидроволокна [6].
Все больные с язвенными дефектами на фоне снижения/или отсутствия магистрального кровотока в пораженной конечности были проконсультированы сосудистым хирургом, который определял объем дообследования и необходимость госпитализации в отделение сосудистой хирургии. В рамках подготовки к госпитализации пациенты получали стандартную терапию язвенных дефектов с учетом имеющегося нарушения кровотока. Следует отметить, что в качестве местного лечения применялись только растворы жидких антисептиков. В качестве разгрузки использовалась в основном обувь с разгрузкой переднего или заднего отделов стопы, в ряде случаев — ортез.
Кратность визитов в клинику в среднем составляла 1 раз в 7 дней. При необходимости частота посещений увеличивалась до 1 раза в 3 дня.
В исследуемой когорте оценивались следующие варианты исходов: заживление язвенного дефекта, ампутация конечности, продолжение лечения на момент окончания периода исследования, смерть. Исследуемым периодом считались 12 месяцев наблюдения. Заживление определялось как полная эпителизация язвенного дефекта и отсутствие рецидива в течение четырех недель после заживления. В эту группу вошли пациенты, у которых заживление язвенных дефектов наступило в результате консервативных лечебных мероприятий, а также после хирургического вмешательства без удаления пальцев или части стопы. При выполнении ампутации нижней конечности анализировался ее уровень. К высоким ампутациям относятся ампутации выше голеностопного сустава: на уровне голени или бедра. Ампутации пальцев стоп или части стопы, выполняемые до уровня голеностопного сустава, относятся к невысоким или малым.
Статистический анализ
Данные описательной статистики представлены как среднее со стандартным отклонением (M±SD) в случае нормального распределения данных, как медиана и значения 25-го и 75-го перцентилей множества данных [Me (25; 75)] при отличном от нормального распределения данных. При частотном распределении переменных по категориям как абсолютное число и его процентное выражение (n, %). Сравнение двух групп проводилось при помощи таблиц сопряженности с вычислением критерия χ2 при номинальных переменных и сравнения средних значений с вычислением t-критерия Стьюдента при непрерывных переменных с нормальным распределением данных. В случае неравномерного распределения данных для сравнения двух независимых выборок применялся метод Манна-Уитни с вычислением U-критерия. Для сравнения нескольких независимых выборок при нормальном распределении данных применялся однофакторный дисперсионный анализ ANOVA. Для того, чтобы определить, между какими из исследуемого множества групп выявляются статистически значимые различия, выполнялось попарное сравнение данных методом Тьюки. При неравномерном распределении данных для сравнения нескольких независимых выборок применялся дисперсионный анализ Краскела-Уоллиса с вычислением Н-критерия. В такой ситуации попарное сравнение данных не выполнялось. Разница считалась значимой при уровне p<0,05.
Построение модели предсказания наступления события (например, выполнения высокой ампутации или заживления хронического язвенного дефекта) выполнялось в два этапа. На первом этапе для выявления ассоциативных связей каждого из потенциальных предикторов исхода вычислялось отношение шансов наступления и ненаступления события. На втором этапе с учетом того, что в реальной клинической практике на исход влияют не отдельно взятые параметры, а их совокупность, для построения многомерной модели одновременного воздействия множества независимых факторов был применен метод логистической регрессии, где в качестве зависимой переменной выступал исход течения язвенного дефекта: заживление или ампутация на любом уровне. Для выявления возможного значимого взаимного влияния параметров выполнялся корреляционный анализ. Применялись коэффициенты корреляции Пирсона и Спирмена. Статистический анализ проводился с использованием программы SPSS, версия 17.0.
Этическая экспертиза
С учетом того, что анализировались данные рутинной работы отделения диабетической стопы, этическая экспертиза исследования признана нецелесообразной (Протокол №5 от 13.10.2023 г.).
Результаты
В окончательный анализ вошли данные 503 пациентов с СДС. В 67% случаев язвенные дефекты протекали на фоне сохранного магистрального кровотока, в 33% — при его снижении. В течение исследуемого периода заживление без выполнения высоких и малых ампутаций в общей когорте пациентов с СДС отмечено в 407 случаях (80,9%). В 32 (6,3%) случаях потребовалось выполнение ампутаций, из них: 23 (4,6%) — в пределах стопы, 3 — на уровне голени (0,6%), 6 — на уровне бедра (1,2%). Смерть наступила у 6 пациентов (1,2%), из них у 2 после выполнения ампутации на уровне бедра. 61 пациент (12,1%) продолжал лечиться на момент окончания исследования (рис. 2).
Таким образом, в подавляющем большинстве случаев удалось достичь заживления язвенных дефектов при СДС в результате проведения консервативных терапевтических мероприятий без выполнения ампутаций на любом уровне.
Учитывая различия в патогенезе и прогнозе нейропатической и нейроишемической форм СДС, была проведена стратификация когорты по наличию или отсутствию ишемии пораженной конечности. Пациенты с нейроишемической формой поражения были значимо старше, имели хроническую болезнь почек (ХБП) 4 и 5 стадии в большем проценте случаев, у них чаще встречался некроз всех слоев кожи (4 и 5 степень по классификации Вагнера). У пациентов с нейропатической формой СДС была чаще диагностирована пролиферативная стадия диабетической ретинопатии. По таким параметрам, как пол, тип диабета, контроль углеводного обмена, скорость обращения за специализированной помощью, локализация, размер и инфицирование язвенного дефекта при первичном обращении, различий между формами СДС не выявлено.
В табл. 1 представлены исходы язвенных дефектов при различных формах СДС
У пациентов с нейропатической формой СДС заживление за год наступало значимо в большем проценте случаев, тогда как ампутации на всех уровнях, включая малые, выполнялись значимо реже, чем у пациентов с нейроишемической формой СДС. Следует отметить, что у пациентов с нейропатическими язвенными дефектами ни одной ампутации бедра выполнено не было. Кроме того, немаловажным является общее небольшое количество выполненных высоких ампутаций за 5-летний период.
Значимые предикторы выполнения высоких ампутаций были выявлены только в отношении пациентов с нейроишемической формой СДС. В этой группе риск выполнения высоких ампутаций возрастал в 3,2 раза при увеличении возраста на каждые 10 лет; в 1,69 раз — при увеличении уровня HbA1c на 1%; в 7,53 раза — при вовлечении в процесс костей, сухожилий и глубжележащих тканей. Анализ группы пациентов с сохранным магистральным кровотоком не выявил объективных предикторов выполнения у них высоких ампутаций (рис. 3).
Параметры, относящиеся к характеристикам пациента, такие как пол, тип СД, вид сахароснижающего лечения, наличие и степень выраженности осложнений СД, значимого влияния на частоту выполнения высоких ампутаций, по полученным нами данным, не оказывают.
На следующем этапе проводилось выявление факторов, влияющих на заживление и отсутствие заживления язвенных дефектов в результате проведения консервативных мероприятий в течение года.
Пациенты с зажившими и незажившими язвенными дефектами отличались продолжительностью этого процесса до обращения за специализированной помощью. Среди заживших ран было значимо больше тех, длительность существования которых не превышала 30 дней. Среди незаживших ран было больше тех, которые образовались вследствие хирургического вмешательства и с нарушенным магистральным кровотоком. По другим параметрам, относящимся как к пациенту, так и к язвенному дефекту, отличий между группами не было.
Для выявления параметров, одновременно воздействующих и оказывающих влияние на исход (заживление или незаживление в течение года), был применен метод бинарной логистической регрессии. Значимыми предикторами отсутствия заживления в результате консервативных мероприятий в течение года явились нарушение магистрального кровотока и несвоевременное обращение за специализированной медицинской помощью (табл. 2).
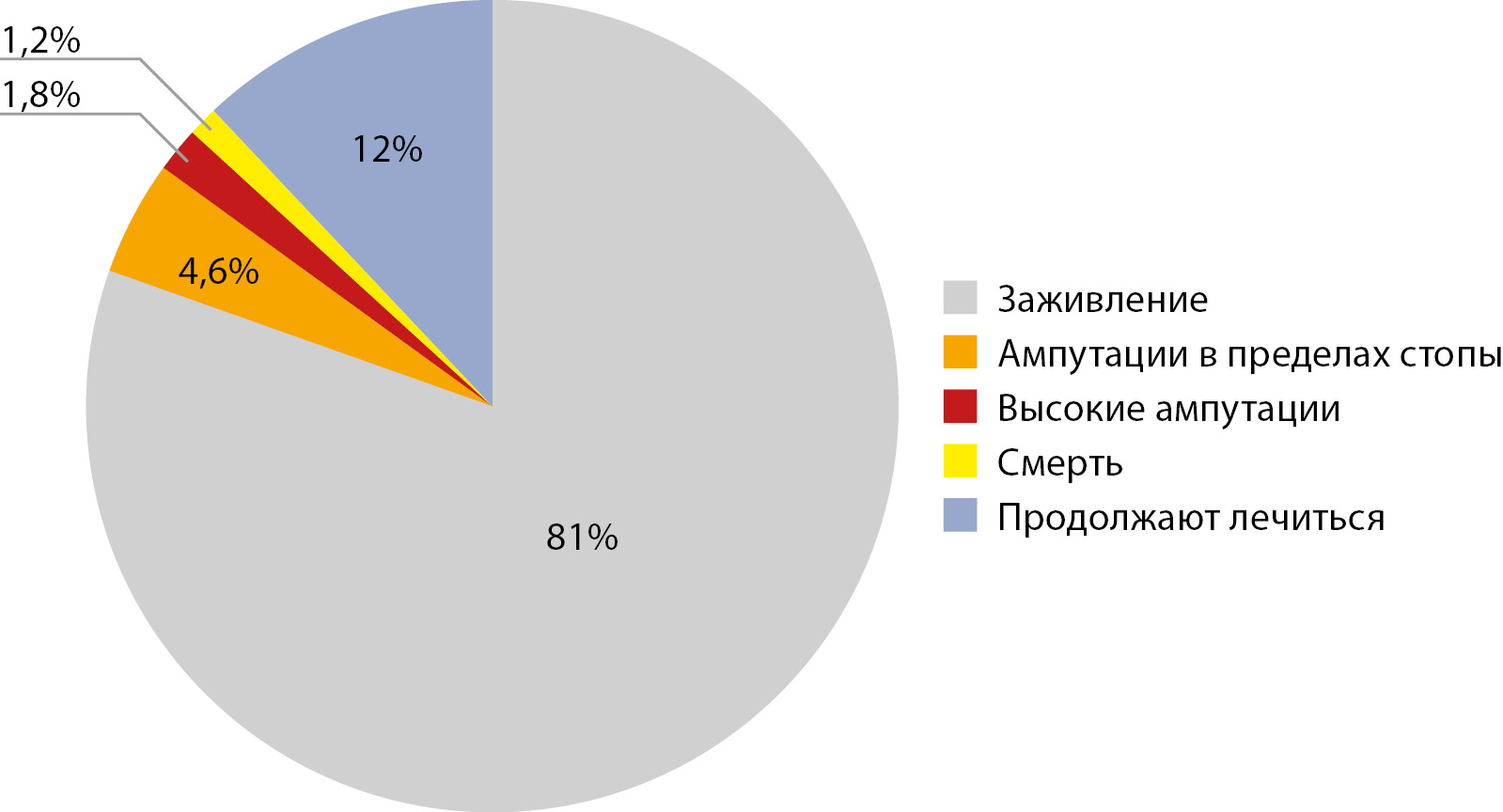
Рисунок 2. Исходы лечения язвенных дефектов при синдроме диабетической стопы в когорте пациентов, наблюдавшихся в отделении диабетической стопы с 2014 по 2019 гг.
Таблица 1. Исходы лечения язвенных дефектов при нейропатической и нейроишемической формах синдрома диабетической стопы
Исход | СДС нейропатическая (n=336) | СДС нейроишемическая (n=167) | p |
Заживление в течение 12 месяцев, n (%) | 294 (87,2) | 113 (67,7) | 0,0001 |
Продолжают лечиться, n (%) | 31 (9,2) | 30 (18) | 0,004 |
Смерть, n (%) | 2 (0,6) | 2 (1,2) | 0,405 |
Ампутации всего, n (%) | 10 (3) | 22 (13,2) | |
на уровне стопы, n (%) | 9 (2,6) | 14 (8,4) | 0,005 |
на уровне голени, n (%) | 1 (0,3) | 2 (1,2) | 0,538 |
на уровне бедра, n (%) | 0 | 6 (3,6) | 0,01 |
Примечание. Числовые данные представлены как абсолютное число и его процентное выражение (n, %). СДС — синдром диабетической стопы.
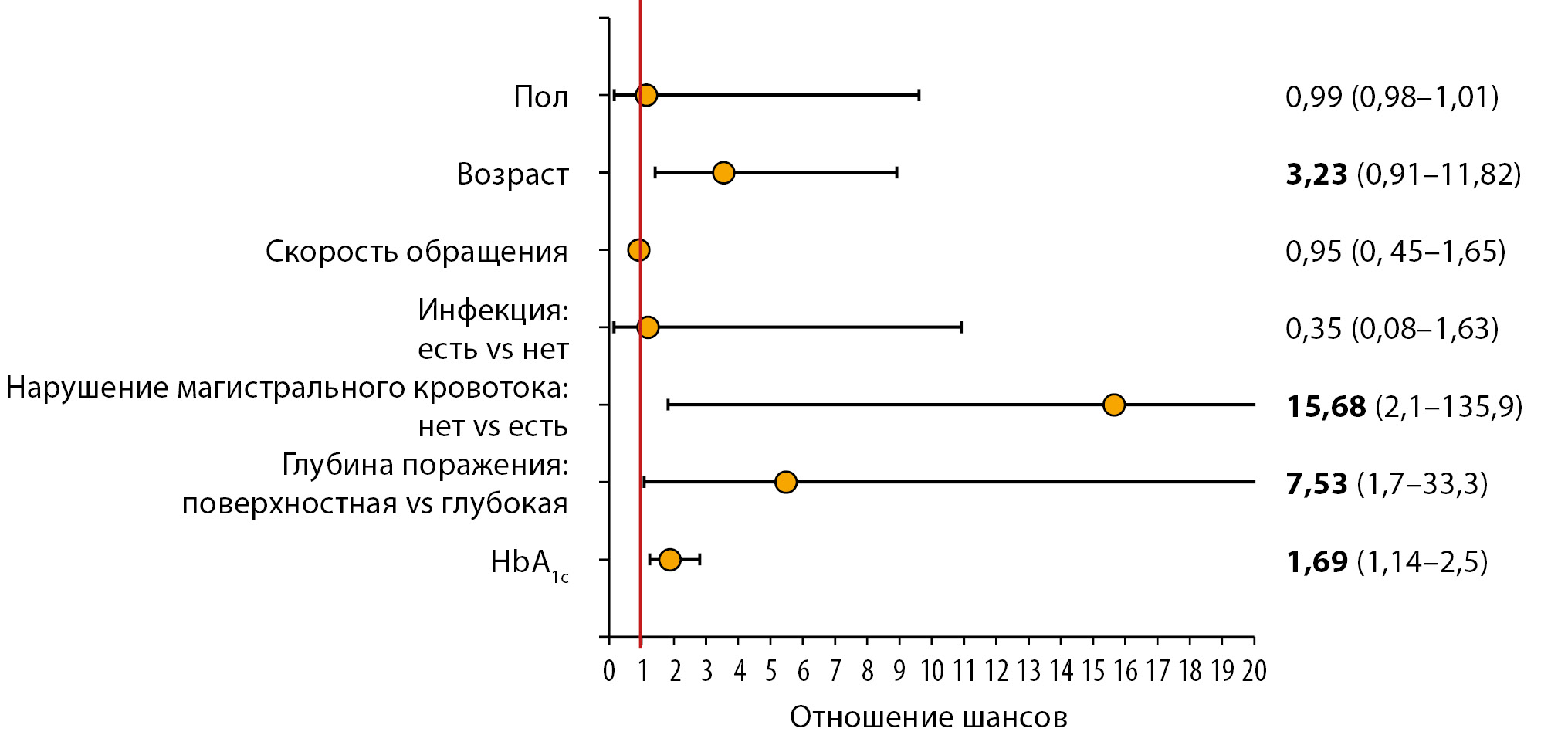
Рисунок 3. Предикторы выполнения высоких ампутаций у пациентов с нейроишемической формой синдрома диабетической стопы.
Примечание. Справа указаны цифровые значения отношения шансов, в скобках — доверительный интервал. Статистически достоверное влияние оказывают предикторы, интервал значений которых не пересекает линию, соответствующую 1: возраст (p=0,006), нарушение магистрального кровотока (p=0,001), глубина поражения по классификации Вагнера (р=0,003), HbA1c (p=0,001). HbA1c — гликированный гемоглобин.
Таблица 2. Предикторы отсутствия заживления язвенных дефектов в результате консервативных мероприятий в когорте пациентов с синдромом диабетической стопы, получающих специализированную амбулаторную помощь
Предикторы | Общая когорта пациентов с СДС (n=503) | ||
ОШ | 95% ДИ | Р | |
Возраст, | 1,19 | 0,67–1,27 | 0,25 |
Пол (М vs Ж) | 0,59 | 0,33–1,07 | 0,88 |
Размер раны: >1 см2 vs ≥1 см2 | 1,44 | 0,75–2,74 | 0,29 |
Обращение за специализированной помощью, увеличение на 1 месяц | 1,07 | 1,03–1,11 | 0,001 |
HbA1c, | 0,95 | 0,79–1,16 | 0,71 |
Локализация: плантарная vs тыльная | 0,966 | 0,44–1,88 | 0,53 |
Инфекция: есть vs нет | 1,15 | 0,65–2,02 | 0,67 |
Глубина раны: поверхностная vs глубокая | 0,92 | 0,47–1,88 | 0,48 |
Нарушение магистрального кровотока: нет vs есть | 2,01 | 1,18–3,43 | 0,014 |
Примечание. ОШ — отношение шансов наступления события (в данной ситуации — отсутствие заживления в течение года); ДИ — доверительный интервал; СДС — синдром диабетической стопы; М — мужчины; Ж — женщины; HbA1c — гликированный гемоглобин.
Обсуждение
В работе проведено и представлено исследование исходов лечения 503 больных с язвенными дефектами при СДС, получающих специализированную амбулаторную помощь. Учитывая возможное влияние COVID 19 на структуру нозологий, количество пациентов, их возможность выполнять предписанный режим и посещать клинику, было принято решение проанализировать данные за 5 лет до пандемии, в период с 2014 по 2019 гг. Большинство язвенных дефектов у пациентов с СДС, получающих лечение в амбулаторном режиме, протекает на фоне адекватного магистрального кровотока (67%). Количество высоких ампутаций за исследуемый период (2014–2019 гг.) в общей группе составило 1,8%. Основным фактором риска их выполнения было нарушение магистрального кровотока в пораженной конечности. После стратификации группы по состоянию кровотока количество высоких ампутаций в группе с нейропатическими звенными дефектами составило 0,3%, а в группе с нейроишемическими поражениями — 8%. Полученные нами показатели сопоставимы с опубликованными в литературе в отношении высоких ампутаций конечностей среди пациентов, получающих помощь в амбулаторном режиме. Так, по данным крупнейшего проспективного многоцентрового исследования EURODIALE, доля высоких ампутаций составила 5% среди всех больных с СДС и 8% среди больных с нейроишемической формой СДС [10]. В Ноттингеме (Великобритания) высокие ампутации были выполнены у 5% пациентов с СДС [11], а в когортном исследовании, проведенном в Германии, — у 3% пациентов [12]. В двух последних исследованиях стратификации группы по магистральному кровотоку не проводилось. При этом, по нашим данным, риск выполнения высоких ампутаций у пациентов с ишемией конечности возрастает в 3,2 раза с увеличением возраста на каждые 10 лет, в 7,5 раза — при увеличении глубины поражения кожных покровов на 1 степень по Вагнеру, в 1,7 раза — при увеличении уровня HbA1c на 1%. Следует отметить, что данные по влиянию контроля углеводного обмена на вероятность выполнения высоких ампутаций у пациентов с нейроишемической формой СДС получены впервые. Опубликованы результаты исследования с участием пациентов с СД 1 типа без уточнения состояния магистрального кровотока, где относительный риск выполнения высоких ампутаций повышался в 1,68 раза при увеличении HbA1c на 1% [13]. Также есть указания на то, что при уровне HbA1c>7% относительный риск выполнения ампутаций на любом уровне увеличивается вдвое [14]. Учитывая, что снижение сахара крови до целевых значений относится к модифицируемым параметрам, нормализацию углеводного обмена можно рассматривать как важнейший компонент снижения количества высоких ампутаций у пациентов с СД и нарушением магистрального кровотока в артериях нижних конечностей.
Заживление без выполнения высоких и малых ампутаций в общей когорте пациентов с СДС достигнуто в 406 случаях (80,7%). Полученные данные о количестве заживших в течение года ран сопоставимы с опубликованными показателями ряда европейских клиник. Так, в исследовании EURODIALE заживления язвенных дефектов при СДС удалось достичь в 77% [15]. По данным проспективного исследования немецких коллег, частота заживления язвенных дефектов при СДС составила 57% при осложненных формах СДС, включая снижение кровотока в пораженной конечности, инфекцию, остеомиелит и до 93% — при неосложненных формах. Следует отметить, что в этом исследовании не указаны сроки, при которых был достигнут вышеуказанный результат. При этом процент высоких ампутаций составил 3% в общей группе больных с СДС [12].
Значимыми предикторами отсутствия заживления в результате консервативных мероприятий в течение года стали: нарушенный магистральный кровоток и несвоевременное обращение за специализированной медицинской помощью. При стратификации когорты по состоянию магистрального кровотока предиктором отсутствия заживления было несвоевременное обращение за специализированной медицинской помощью и размер поражения более 1 см2 при нейропатической форме СДС. Не выявлено доказательств влияния на исход демографических (возраст, пол) и клинических (тип СД, HbA1c, локализация язвенного дефекта, его глубина, инфицирование при первичном обращении) параметров. Полученные данные отличаются от опубликованных результатов когортных исследований. Так, в исследовании EURODIALE предикторами отсутствия заживления в общей группе пациентов с СДС были возраст, мужской пол, сердечная недостаточность, терминальная стадия ХБП, большой размер язвенного дефекта, нарушение магистрального кровотока, периферическая нейропатия. Параметром, определяющим отсутствие заживления у больных с нарушенным магистральным кровотоком, была инфекция [15]. В нашей работе влияния инфекции на исход течения язвенного дефекта в течение года не получено. Одним из возможных объяснений этого является обязательное назначение антибактериальных препаратов при наличии признаков инфицирования при первичном обращении, адекватная хирургическая обработка раны и более частые визиты (2–3 раза в неделю) в отделение для выполнения ухода за раной.
Отдельного внимания заслуживает такой показатель, как своевременность обращения за специализированной помощью. Этот параметр относится к одним из ключевых в плане профилактики высоких ампутаций, однако эксперты справедливо отмечают, что данная рекомендация основана на теоретических предпосылках, а не на реальных цифрах [10]. В нашей работе впервые получены объективные данные, подтверждающие чрезвычайную важность максимально быстрого обращения пациентов за специализированной помощью.
Заключение
Таким образом, восстановление магистрального кровотока в пораженной конечности, контроль инфекции и соблюдение режима разгрузки приводят к минимизации количества высоких ампутаций и заживлению язвенных дефектов в подавляющем большинстве случаев. Проведенный когортный анализ продемонстрировал высокую эффективность специализированной помощи данной категории больным на догоспитальном этапе. В этой связи организация амбулаторных кабинетов диабетической стопы имеет принципиально важное значение как в отношении профилактики высоких ампутаций нижних конечностей у больных СД, так и заживления хронических язвенных дефектов стоп.
Дополнительная информация
Источники финансирования. Работа выполнена по инициативе авторов без привлечения финансирования.
Конфликт интересов. Авторы декларируют отсутствие явных и потенциальных конфликтов интересов, связанных с содержанием настоящей статьи.
Участие авторов. Комелягина Е.Ю. — концепция и дизайн исследования, сбор клинического материала, отбор пациентов, обзор публикаций по теме статьи, обработка и анализ полученных данных, написание текста; Анциферов М.Б. — концепция и дизайн исследования, редактирование, финальное утверждение рукописи. Все авторы одобрили финальную версию статьи перед публикацией, выразили согласие нести ответственность за все аспекты работы, подразумевающую надлежащее изучение и решение вопросов, связанных с точностью или добросовестностью любой части работы.
Список литературы
1. Sage RA, Pinzur M, Stuck R, Napolitano C. Amputation and Rehabilitation of the Diabetic Foot. In: The Diabetic Foot. Totowa, NJ: Humana Press; 2007:363-389. doi: https://doi.org/10.1007/978-1-59745-075-1_18
2. Forsythe RO, Apelqvist J, Boyko EJ, et al. Performance of prognostic markers in the prediction of wound healing or amputation among patients with foot ulcers in diabetes: A systematic review. Diabetes Metab Res Rev. 2020;36(S1). doi: https://doi.org/10.1002/dmrr.3278
3. Harding JL, Pavkov ME, Magliano DJ, Shaw JE, Gregg EW. Global trends in diabetes complications: a review of current evidence. Diabetologia. 2019;62(1):3-16. doi: https://doi.org/10.1007/s00125-018-4711-2
4. Carinci F, Uccioli L, Massi Benedetti M, Klazinga NS. An in-depth assessment of diabetes-related lower extremity amputation rates 2000–2013 delivered by twenty-one countries for the data collection 2015 of the Organization for Economic Cooperation and Development (OECD). Acta Diabetol. 2020. doi: https://doi.org/10.1007/s00592-019-01423-5
5. Бреговский В.Б., Карпова И.А. Анализ специализированной помощи больным с синдромом диабетической стопы в Санкт-Петербурге за 2010-2021 гг. // Сахарный диабет. — 2022. — Т. 25. — №5. — С. 477-48. doi: https://doi.org/10.14341/DM12914
6. Дедов И.И., Шестакова М.В., Майоров А.Ю., и др. Алгоритмы специализированной медицинской помощи больным сахарным диабетом / Под редакцией И.И. Дедова, М.В. Шестаковой, А.Ю. Майорова. 11-й выпуск. // Сахарный диабет. — 2023. — Т. 26. — №2S. — С. 1-157. doi: https://doi.org/10.14341/DM13042
7. Schaper NC, van Netten JJ, Apelqvist J, Bus SA, Hinchliffe RJ, Lipsky BA. Practical Guidelines on the prevention and management of diabetic foot disease (IWGDF 2019 update). Diabetes Metab Res Rev. 2020;36(S1). doi: https://doi.org/10.1002/dmrr.3266
8. Lipsky BA, Berendt AR, Cornia PB, et al. 2012 Infectious Diseases Society of America Clinical Practice Guideline for the Diagnosis and Treatment of Diabetic Foot Infectionsa. Clin Infect Dis. 2012;54(12):e132-e173. doi: https://doi.org/10.1093/cid/cis346
9. Клинические рекомендации по диагностике и лечению синдрома диабетической стопы // Раны и раневые инфекции. — 2015. — Т. 2. — №3. — С. 63-83.
10. Prompers L, Huijberts M, Apelqvist J, et al. High prevalence of ischaemia, infection and serious comorbidity in patients with diabetic foot disease in Europe. Baseline results from the Eurodiale study. Diabetologia. 2007;50(1):18-25. doi: https://doi.org/10.1007/s00125-006-0491-1
11. Jeffcoate WJ, Chipchase SY, Ince P, Game FL. Assessing the Outcome of the Management of Diabetic Foot Ulcers Using Ulcer-Related and Person-Related Measures. Diabetes Care. 2006;29(8):1784-1787. doi: https://doi.org/10.2337/dc06-0306
12. Beckert S. A New Wound-Based Severity Score for Diabetic Foot Ulcers: A prospective analysis of 1,000 patients. Diabetes Care. 2006;29(5):988-992. doi: https://doi.org/10.2337/diacare.295988
13. Ólafsdóttir AF, Svensson A-M, Pivodic A, et al. Excess risk of lower extremity amputations in people with type 1 diabetes compared with the general population: amputations and type 1 diabetes. BMJ Open Diabetes Res Care. 2019;7(1):e000602. doi: https://doi.org/10.1136/bmjdrc-2018-000602
14. Arya S, Binney ZO, Khakharia A, et al. High Hemoglobin A1c Associated with Increased Adverse Limb Events in Peripheral Arterial Disease Patients Undergoing Revascularization. J Vasc Surg. 2017. doi: https://doi.org/10.1016/j.jvs.2016.10.028
15. Prompers L, Schaper N, Apelqvist J, et al. Prediction of outcome in individuals with diabetic foot ulcers: focus on the differences between individuals with and without peripheral arterial disease. The EURODIALE Study. Diabetologia. 2008;51(5):747-755. doi: https://doi.org/10.1007/s00125-008-0940-0
Об авторах
Е. Ю. КомелягинаРоссия
Комелягина Елена Юрьевна - д.м.н.
119034, Москва, ул. Пречистенка, 37
Конфликт интересов:
Авторы декларируют отсутствие явных и потенциальных конфликтов интересов, связанных с содержанием настоящей статьи
М. Б. Анциферов
Россия
Анциферов Михаил Борисович - д.м.н., профессор.
Москва
Конфликт интересов:
Авторы декларируют отсутствие явных и потенциальных конфликтов интересов, связанных с содержанием настоящей статьи
Дополнительные файлы
|
|
1. Рисунок 1. Когорта пациентов с синдромом диабетической стопы, вошедших в окончательный анализ. | |
| Тема | ||
| Тип | Исследовательские инструменты | |
Посмотреть
(194KB)
|
Метаданные ▾ | |
|
|
2. Figure 1. Cohort of patients with diabetic foot syndrome included in the final analysis. | |
| Тема | ||
| Тип | Исследовательские инструменты | |
Посмотреть
(167KB)
|
Метаданные ▾ | |
|
|
3. Рисунок 2. Исходы лечения язвенных дефектов при синдроме диабетической стопы в когорте пациентов, наблюдавшихся в отделении диабетической стопы с 2014 по 2019 гг. | |
| Тема | ||
| Тип | Исследовательские инструменты | |
Посмотреть
(103KB)
|
Метаданные ▾ | |
|
|
4. Figure 2. Outcomes of ulcer defects in diabetic foot syndrome in a cohort of patients followed up in the diabetic foot department from 2014 to 2019. | |
| Тема | ||
| Тип | Исследовательские инструменты | |
Посмотреть
(99KB)
|
Метаданные ▾ | |
|
|
5. Рисунок 3. Предикторы выполнения высоких ампутаций у пациентов с нейроишемической формой синдрома диабетической стопы. | |
| Тема | ||
| Тип | Исследовательские инструменты | |
Посмотреть
(178KB)
|
Метаданные ▾ | |
|
|
6. Figure 3. Predictors of the need for high amputations in patients with neuroischemic DFS. | |
| Тема | ||
| Тип | Исследовательские инструменты | |
Посмотреть
(173KB)
|
Метаданные ▾ | |
Рецензия
Для цитирования:
Комелягина Е.Ю., Анциферов М.Б. Анализ эффективности лечения больных с синдромом диабетической стопы в амбулаторных условиях. Сахарный диабет. 2024;27(4):376-383. https://doi.org/10.14341/DM13127
For citation:
Komelyagina E.Y., Antsiferov M.B. Analysis of the effectiveness of outpatient treatment of patients with diabetic foot. Diabetes mellitus. 2024;27(4):376-383. https://doi.org/10.14341/DM13127
JATS XML

Контент доступен под лицензией Creative Commons Attribution-NonCommercial-NoDerivatives 4.0 International License (CC BY-NC-ND 4.0).















































