Перейти к:
Система помощи принятия врачебных решений на базе искусственного интеллекта для первичной настройки параметров инсулиновой помпы у детей с сахарным диабетом 1 типа
https://doi.org/10.14341/DM13081
Аннотация
ОБОСНОВАНИЕ. Общепринятые рекомендации по первичной настройке инсулиновой помпы в настоящее время не определены, поэтому данный процесс во многом носит субъективный характер и зависит от личного опыта и умения врача работать с инсулиновыми помпами.
ЦЕЛЬ. Разработка системы поддержки принятия врачебных решений (СППВР), определяющей первичные настройки инсулиновой помпы, которые имели бы удовлетворительную согласованность с экспертным мнением врачей.
МАТЕРИАЛЫ И МЕТОДЫ. Модель разработана на основании данных от 2850 детей с сахарным диабетом 1 типа (СД1), которых перевели на непрерывную подкожную инфузию инсулина, включая возраст, вес, суточную потребность в инсулине, HbA1c. В основе модели лежит нейронная сеть.
Проводилась проспективная оценка согласованности рекомендаций СППВР и врача на 35 пакетах данных детей с СД1 (медиана возраста 9,3 года [6,4; 11,5]). Использовались 4 степени согласованности: полная согласованность, когда врач согласился с предложенными программой рекомендациями; частичная согласованность, когда врач не согласился с предложенными программой рекомендациями, но разница между врачебными рекомендациями и рекомендациями СППВР была в диапазоне ±15%; полная несогласованность — разница была более ±15%; допустимая согласованность — сумма полной и частичной согласованности. Нулевая гипотеза — не существует разницы в согласованности/несогласованности между врачами и СППВР.
РЕЗУЛЬТАТЫ. Частота полной согласованности между СППВР и рекомендациями врача по инициации помповой инсулинотерапии составляет 29,8–43,8%, а полной несогласованности — 33,7–41,1%. Допустимая согласованность составила 58,9–66,3%. Значимых различий в медианных показателях параметров инсулиновой помпы между СППВР и врачами относительно исходных значений нет.
ЗАКЛЮЧЕНИЕ. Полученные результаты соответствуют ранее проведенным исследованиям. Алгоритм демонстрирует приемлемую производительность, а СППВР — сопоставимость рекомендаций по сравнению с мнением врачей-экспертов, без значимых отклонений между различными параметрами.
Ключевые слова
Для цитирования:
Лаптев Д.Н., Сорокин Д.Ю. Система помощи принятия врачебных решений на базе искусственного интеллекта для первичной настройки параметров инсулиновой помпы у детей с сахарным диабетом 1 типа. Сахарный диабет. 2024;27(6):555-564. https://doi.org/10.14341/DM13081
For citation:
Laptev D.N., Sorokin D.Y. Neural network based clinical decision support system for the calculation the initial continuous subcutaneous insulin infusion settings. Diabetes mellitus. 2024;27(6):555-564. (In Russ.) https://doi.org/10.14341/DM13081
ОБОСНОВАНИЕ
Лечение сахарного диабета 1 типа (СД1) является многофакторным процессом, один из основных компонентов которого — инсулинотерапия. При установке диагноза СД1 инициируют интенсифицированную базис-болюсную схему инсулинотерапии, которая включает в себя использование двух инсулинов — короткого (болюсный) и длительного (базальный) действия. В дальнейшем, по мере адаптации пациента к своему заболеванию, осуществляется перевод пациента на непрерывную подкожную инфузию инсулина (НПИИ) с помощью инсулиновой помпы. Процесс перевода на помповую инсулинотерапию происходит, как правило, в условиях стационарного лечения и включает в себя первичную настройку параметров инсулиновой помпы с последующим подбором доз согласно гликемическому профилю, а также обучение пациента основам помповой инсулинотерапии. Общепринятые рекомендации по первичной настройке инсулиновой помпы в настоящее время не определены, поэтому данный процесс во многом носит субъективный характер и зависит от личного опыта и умения врача работать с инсулиновыми помпами. Основным показателем, используемым для расчета настроек инсулиновой помпы, является суточная доза инсулина (СДИ) [1][2], в то же время и другие индивидуальные и клинические показатели пациента, как и время суток [3], могут влиять на потребность в инсулине, однако в реальной практике они чаще всего не учитываются. Учитывая данные сложности актуальным является разработка алгоритма первичной настройки инсулиновой помпы, в основе которой будут лежать машинные методы обучения, и оценка степени согласованности генерируемых ею настроек с экспертным мнением врачей.
Нейронные сети, как подкласс машинного обучения, уже давно положительно зарекомендовали себя в медицине для решения комплексных медицинских задач. Искусственные нейронные сети (НС) представляют собой адаптивные и вычислительные функции, которые имитируют структуру и поведение нейронов центральной нервной системы человека [4]. НС могут быть обучены различать и классифицировать сложные закономерности с помощью итеративного процесса обучения. После надлежащего обучения НС могут прогнозировать с большей точностью, чем традиционные статистические модели. Благодаря своей способности выявлять многогранные нелинейные отношения между предикторами и исходами, НС нашли эффективное применение в системах поддержки принятия врачебных решений (СППВР) [5].
ЦЕЛЬ ИССЛЕДОВАНИЯ
Целью исследования являлась разработка СППВР, определяющей первичные настройки инсулиновой помпы, которые имели бы удовлетворительную согласованность с экспертным мнением врачей.
МАТЕРИАЛЫ И МЕТОДЫ
Проведены два исследования.
I. Разработка математической модели по первичной настройке инсулиновой помпы
Место и время проведения исследования
Место проведения. Детское отделение СД ГНЦ РФ ФГБУ «НМИЦ эндокринологии» Минздрава России.
Время исследования. Сбор данных для машинного обучения проводился с 2020 г. по май 2023 г., разработка математической модели осуществлена в мае 2023 г.
Изучаемые популяции
Популяция: дети с СД1 на помповой инсулинотерапии.
Критерии включения:
1) дети обоих полов;
2) возраст от 1 до 18 лет;
3) СД1 (Е10 Инсулинозависимый сахарный диабет);
4) использование НПИИ.
Критерии исключения:
1) клинически значимые, острые заболевания сердечно-сосудистой, нервной, мочеполовой систем, желудочного-кишечного тракта и заболевания крови;
2) инсулинотерапия путем множественных инъекций инсулина в течение более 14 дней за последний месяц;
3) системная терапия препаратами глюкокортикоидов;
4) наличие в анамнезе эмоциональных, поведенческих или других расстройств, которые могут помешать контролю СД и участию в исследовании.
Способ формирования выборки из изучаемой популяции
Способ формирования выборки — сплошной.
Дизайн исследования
Дизайн исследования: проспективное.
Математические методы и программные продукты
Для разработки модели был проведен ретроспективный анализ клинических данных и настроек инсулиновой помпы пациентов с СД1 в возрасте от 0 до 18 лет, проходивших стационарное лечение в ГНЦ ФГБУ «НМИЦ эндокринологии» Минздрава России и находящихся на помповой инсулинотерапии независимо от длительности заболевания и длительности использования помпы. Регистрация настроек инсулиновой помпы происходила на момент выписки пациента из стационара, что также соответствовало завершению коррекции инсулинотерапии.
Для построения модели и оценки ее качества, общая выборка случайным образом разделена на тренировочную и тестовую в соотношении 90%:10%. При обучении НС тренировочная выборка была также случайным образом разделена на непосредственно тренировочную и валидационную в соотношении 90%:10%.
Предикторы и прогнозируемые показатели
В качестве предикторов были отобраны клинические и антропометрические показатели, которые могут значимо влиять на настройки инсулиновой помпы, по данным ранее проведенных исследований [1][2][6] и в то же время быть доступны врачу при переводе пациента на помповую инсулинотерапию: паспортный возраст (года), гликированный гемоглобин (HbA1c, %), масса тела (кг), СДИ (Ед/сут). Прогнозируемыми, выходными показателями были почасовые настройки (за каждый час суток, всего 24 настройки за сутки для каждого параметра) базального профиля, углеводного коэффициента (УК) и коэффициента чувствительности к инсулину (ЧИ).
Подготовка данных
Для достижения максимальной производительности и более простой реализации модели в исходном массиве данных было предварительно проведено:
1) удаление дубликатов и выбросов, если наблюдение в 1,5 раза превышает межквартильный размах, превышающий третий квартиль (Q3), или в 1,5 раза превышает межквартильный размах, меньше первого квартиля (Q1);
2) исключение из анализа случаев с более чем 15% отсутствующих значений (менее 85% данных доступны);
3) приведение числовых значений переменных к одинаковой области их измерения с использованием алгоритма максимального абсолютного масштабирования, который масштабирует данные до максимального значения: xscaled = x/max (x), где x значение признака;
4) подстановка (замена) отсутствующих значений (для случаев с менее чем 15% отсутствующих данных) используя метод k-ближайших соседей (kNN) с евклидовым расстоянием 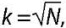 где N размер выборки;
где N размер выборки;
5) отбор наиболее значимых признаков.
Реализация искусственной нейронной сети
НС представляет собой абстракцию структуры человеческого мозга и пытается имитировать ее работу [7]. НС состоит из одного входного и выходного слоя, а также одного или нескольких скрытых слоев.
Каждый слой НС включает несколько нейронов, которые выполняют разные задачи. Входной слой получает данные и, при необходимости, преобразует их в нормализованные фрагменты, подходящие для математических вычислений. Процесс вычисления происходит в скрытых слоях, которые имеют наибольшее количество нейронов и выполняют операцию вычисления на основании межнейронных связей — весов. Выходное значение нейрона определяется функцией активации в зависимости от результата взвешенной суммы входов и порогового значения. В выходном слое нейроны получают результаты вычислений слоя обработки и представляют их пользователю.
В этом исследовании, с использованием открытой библиотеки Scikit-learn 1.2.2 [8] на языке программирования Python 3.10.2, была реализована НС прямого распространения — многослойный перцептрон.
В качестве функции активации нейронов скрытых слоев использовалась функция ReLu (rectified linear unit). Для коррекции весов нейронов НС при обучении модели использовался оптимизированный метод стохастического градиентного спуска Adam – ADAptive Momentum [9]. В качестве функции потерь использовался расчет среднеквадратичной ошибки.
Гиперпараметры НС подбирались эмпирически до получения наилучшей конфигурации НС, с учетом оптимальной скорости обучения и производительности. Для сравнения различных конфигураций использовалась оценка коэффициента детерминации (R2) предсказания.
Система помощи принятия врачебных решений (СППВР)
СППВР реализована на языке программирования Python 3.10.2 с использованием открытой библиотеки (фреймворка) Dash Open Source 2.10.0 (https://dash.plotly.com/).
II. Оценка согласованности рекомендаций СППВР с экспертным мнением врачей
Место и время проведения исследования
Место проведения. Детское отделение СД ГНЦ РФ ФГБУ «НМИЦ эндокринологии» Минздрава России.
Время исследования. С июня по сентябрь 2023 г.
Изучаемые популяции
Популяция: дети с СД1, переходящие с терапии множественными инъекциями инсулина (МИИ) на НПИИ.
Критерии включения:
1) дети обоих полов;
2) возраст от 1 до 18 лет;
3) СД1 (Е10 Инсулинозависимый сахарный диабет);
4) использование МИИ.
Критерии исключения:
1) клинически значимые, острые заболевания сердечно-сосудистой, нервной, мочеполовой систем, желудочного-кишечного тракта и заболевания крови;
2) системная терапия препаратами глюкокортикоидов;
3) наличие в анамнезе эмоциональных, поведенческих или других расстройств, которые могут помешать контролю сахарного диабета и участию в исследовании.
Способ формирования выборки из изучаемой популяции
Способ формирования выборки — сплошной.
Дизайн исследования
Дизайн исследования: одномоментное.
Оценка согласованности предсказанного результата
На базе детского отделения СД ГНЦ РФ ФГБУ «НМИЦ эндокринологии» Минздрава России была проведена оценка согласованности предложенных первичных настроек инсулиновой помпы между СППВР и врачами. Оценку проводили у пациентов, которых переводили с терапии множественными инъекциями инсулина (МИИ) на НПИИ, всего 35 пациентов. Осуществлялась оценка согласованности почасовых настроек — по 24 точки для базального профиля, УК и ЧИ — всего 72 точки сравнения в каждом пакете. Общее количество точек сравнения составило 2520.
В начале были получены рекомендации СППВР, которые были направлены на рассмотрение лечащему врачу с последующей их частичной или полной коррекцией, при необходимости. Всего в исследовании приняло участие 7 детских эндокринологов детского отделения СД ГНЦ РФ ФГБУ «НМИЦ эндокринологии» Минздрава России. Каждый из лечащих врачей имеет большой опыт в переводе и настройке помповой инсулинотерапии.
В целях исследования было определено 3 степени согласованности: 1-я степень — полная согласованность, когда врач согласился с предложенными программой рекомендациями; 2-я степень — частичная согласованность, когда врач не согласился с предложенными программой рекомендациями, но разница между врачебными рекомендациями и рекомендациями СППВР была в диапазоне ±15%; 3-я степень — полная несогласованность, когда врач не согласился с предложенными программой рекомендациями и разница между врачебными рекомендациями и рекомендациями СППВР была более ±15%.
Разница в ±15% между врачебными рекомендациями и рекомендациями СППВР является клинически допустимой, поэтому мы ввели такое понятие, как допустимая согласованность, которая отражает сумму полной и частичной согласованности.
Статистический анализ
Для оценки значимости связи предикторов с настройками инсулиновой помпы использовался однофакторный дисперсионный анализ ANOVA.
При оценке согласованности между рекомендациями ССПВР и врачебными рекомендациями размер выборки предварительно не рассчитывался. Статистическая обработка проводилась в Python 3.10.2 с использованием открытых библиотек: statsmodels 0.13.2 (Seabold, Skipper, and Josef Perktold. “statsmodels: Econometric and statistical modeling with python.” Proceedings of the 9th Python in Science Conference. 2010), SciPy 1.9.1 (https://scipy.org/). Совокупности количественных показателей, описывались при помощи значений медианы (Me), нижнего и верхнего квартилей (Q1–Q3). Различие между количественными признаками в зависимых выборках оценивалось с помощью критерия Уилкоксона, в независимых выборках — с помощью критерия Манна–Уитни. Нулевая гипотеза заключалась в том, что не существует разницы в согласованности/ несогласованности между врачами и СППВР, поэтому любое значимое значение P (р<0,05) указывало на наличие значительной разницы между рекомендациями врачей и СППВР, что указывало на меньшую эффективность модели.
Этическая экспертиза
Локальным этическим комитетом ГНЦ РФ ФГБУ «Национальный медицинский исследовательский центр эндокринологии» Минздрава России, согласно протоколу №17 заседания Комитета от 28.10.2020, постановлено, что планируемая научная работа соответствует этическим стандартам добросовестной клинической практики и может быть проведена на базе Института детской эндокринологии ГНЦ РФ ФГБУ «НМИЦ эндокринологии» Минздрава России. Законные представители пациентов дали информированное согласие на сбор данных и участие в исследовании.
РЕЗУЛЬТАТЫ
I. Математическая модель по первичной настройке инсулиновой помпы
Характеристика участников при разработке математической модели
После исключения не соответствующих и/или неполных записей (более 15% отсутствующих значений), итоговая выборка составила 2850 пациентов. Из общей выборки выделана тренировочная (90% случаев — 2565 пациентов) и тестовая (10% случаев — 285 пациентов) выборки.
Характеристики выборок пациентов, данные которых использованы для обучения и тестирования модели представлены в табл. 1.
Таблица 1. Клиническая характеристика общей, тренировочной и тестовой выборок пациентов
Вся выборка | Тренировочная выборка | Тестовая выборка | Уровень р | |
n | 2850 | 2565 | 285 | |
Возраст (годы) | 11,1 (7,5–14,3) | 11,1 (7,5–14,3) | 10,8 (8–14) | 0,573 |
Вес (кг) | 38 (25–54,7) | 38 (25–55) | 36,2 (26–52,7) | 0,559 |
HbA1c (%) | 7,8 (7–8,7) | 7,8 (7–8,7) | 8 (7,2–8,8) | 0,118 |
СДИ (Ед) | 30 (18–45) | 30 (18–45) | 30 (19,9–45) | 0,935 |
Примечание. Данные представлены в виде: среднее значение (SD); СДИ — суточная доза инсулина.
Предикторы
Отобранные признаки (возраст, вес, HbA1c, СДИ) статистически значимо (p<0,001) влияли на практически все почасовые параметры помповой инсулинотерапии, за исключением показателя HbA1c который значимо не был связан с УК в первый (р=0,107) и второй (р=0,023) час ночи. Однако учитывая, что показатель HbA1c значимо влиял на другие параметры помповой терапии, в дальнейшем все предикторы были использованы для построения различных конфигураций НС.
Настройка и оценка производительности нейронных сетей
Для определения оптимальной конфигурации НС, были проанализированы показатели прогностической эффективности нескольких моделей с последовательным включением каждого предиктора на основании более высокого значения F (сначала с самым высоким). Результаты представлены на рис. 1.
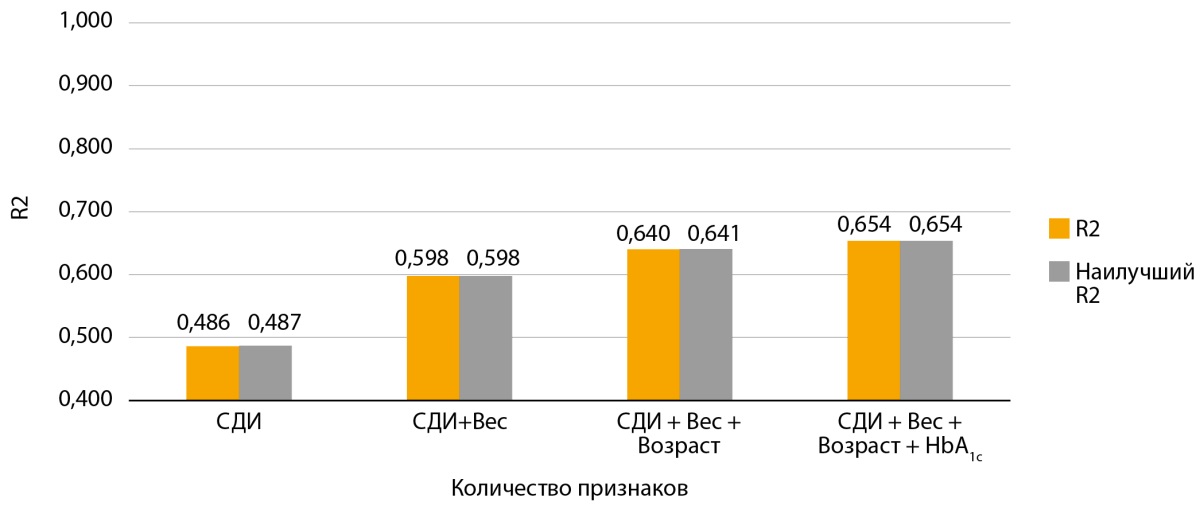
Рисунок 1. Коэффициент детерминации R2 модели, полученный на валидационной выборке в зависимости от количества предикторов в процессе их последовательного добавления по убыванию статистической величины.
Примечание. СДИ — суточная доза инсулина; R2 — коэффициент детерминации
В целом наиболее значимыми предикторами являлись СДИ и вес пациента, однако включение других признаков также увеличивало качество прогноза. В связи с этим, для итоговой конфигурации НС было принято решение использовать все предварительно отобранные предикторы.
На рис. 2 представлена динамика ошибки — значения функции потерь и коэффициента детерминации R2 в процессе обучения итоговой конфигурации НС. Дальнейшее изменение архитектуры НС (увеличение скрытых слоев, количества нейронов в скрытых слоях и скорости обучения) не привело к улучшению характеристик НС. Наилучшей оказалась конфигурация НС прямого распределения с входным и выходящим слоями, тремя скрытыми слоями по 50 нейронов в каждом.
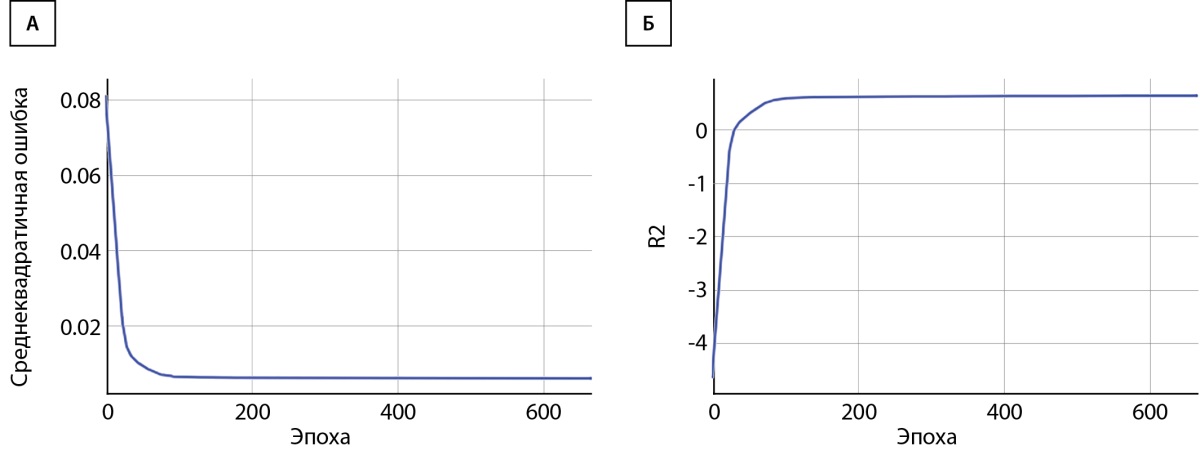
Рисунок 2. Значение функции потерь (А) и коэффициента детерминации R2 (Б) на тренировочной выборке.
После обучения оценка производительности (качества) НС проводилась на тестовой выборке. На тестовой выборке среднеквадратичная ошибка итоговой конфигурации составила 0,0061, а коэффициент детерминации 0,639, что незначительно отличалось от результатов, полученных на тренировочной выборке.
Интерфейс математической модели
С использованием полученной модели НС была разработана программа — СППВР (рис. 3). Программа имеет веб-интерфейс, и для получения результата необходимо ввести в соответствующие поля обязательную информацию: дату рождения, вес, HbA1c и СДИ пациента. Также возможно указать ФИО или идентификатор пациента, модель инсулиновой помпы и способ измерения УК (в граммах или хлебных единицах). Указание модели инсулиновой помпы необходимо для определения точности округления настраиваемых параметров инсулиновой помпы, так как шаг изменения настройки зависит от конкретной модели.
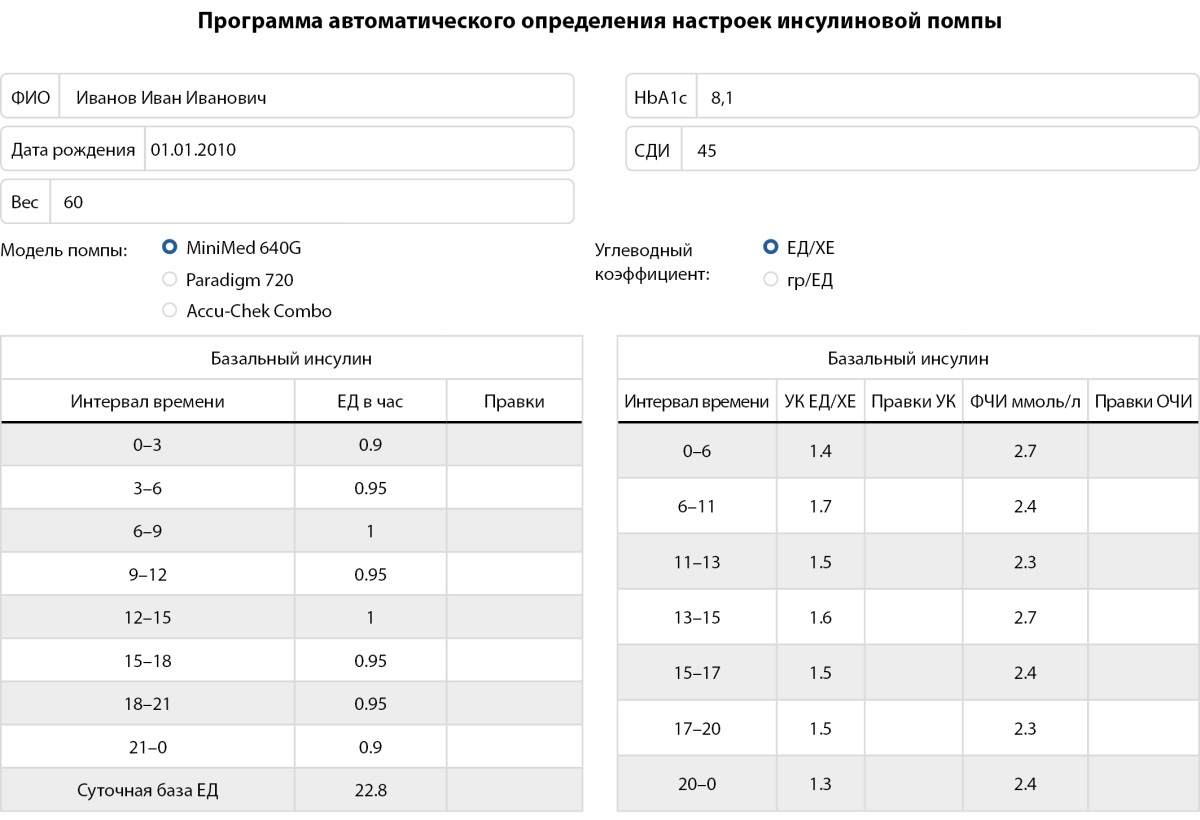
Рисунок 3. Интерфейс системы поддержки принятия врачебных решений.
Примечание. УК — углеводный коэффициент; ЧИ — коэффициент чувствительности к инсулину.
После внесения необходимой информации производится расчет базальных и болюсных настроек инсулиновой помпы. Настройки базального профиля представляются в виде усредненных за 3 часа значений, настройки болюсного введения (УК и ЧИ) предоставляются в виде значений, усредненных за различные периоды времени, соответствующие ночному времени и времени приемов пищи, когда коэффициенты могут существенно различаться.
Свободные поля рядом с предсказанными значениями могут использоваться для внесения корректировок врачом.
II. Оценка согласованности предсказания модели и рекомендации врача
В оценке согласованности приняло участие 35 пациентов, из них 54,3% мальчики. Медиана возраста составила 9,3 года [ 6,4; 11,5], HbA1c — 7,4% [ 6,8; 8,6], длительности СД1 — 2,2 года [ 1,1; 5,1], СДИ — 0,7 ЕД/кг/сут [ 0,6; 1,0] или же 24,0 ЕД/сут [ 16,0; 30,8]. Полученная выборка по возрасту и степени компенсации углеводного обмена является репрезентативной по отношению к целевой популяции детей с СД1 ( табл. 2).
Таблица 2. Клинико-лабораторная характеристика пациентов целевой популяции на основании ранее проведенных исследований
Клиническое исследование | Возраст, лет | HbA1c, % |
Романенкова Е.М. и соавт., n=703 [10] | 11,3 [ 7,3; 14,6] | 7,4 [ 6,5; 8,6] |
Лаптев Д.Н. и соавт., n=469 [11] | 11,3 [ 8,4; 14,6] | 7,4 [ 6,6; 8,4] |
Лаптев Д.Н. и соавт., n=228 [12] | 11,2 [ 8,6; 14,7] | 7,6 [ 6,8; 8,9] |
Примечание. Данные представлены в виде медианы и интерквартильного интервала: Me [Q1; Q3].
Медиана полной согласованности базального профиля (рис. 4А) составила 12,5% [ 0–50], УК — 25% [ 8,3–54,2], ЧИ — 45,8% [ 0–91,7]. Медиана частичной согласованности базального профиля (рис. 4Б) составила 12,5% [ 0–60,4], УК — 29,2% [ 0–41,7], ЧИ — 0,0% [ 0–45,8]. Медиана полной несогласованности базального профиля (рис. 4В) составила 25,0% [ 0–81,3], УК — 37,5% [ 0–58,3], ЧИ — 0% [ 0–95,8]. Медиана допустимой согласованности (сумма полной и частичной согласованности) базального профиля (рис. 4Г) составила 75% [ 12,5–100], УК — 62,5% [ 41,7–100], ЧИ — 100% [ 0–100]. Из рис. 4 видно, что значимых различий в согласованности параметров инсулиновой помпы между СППВР и врачами нет.
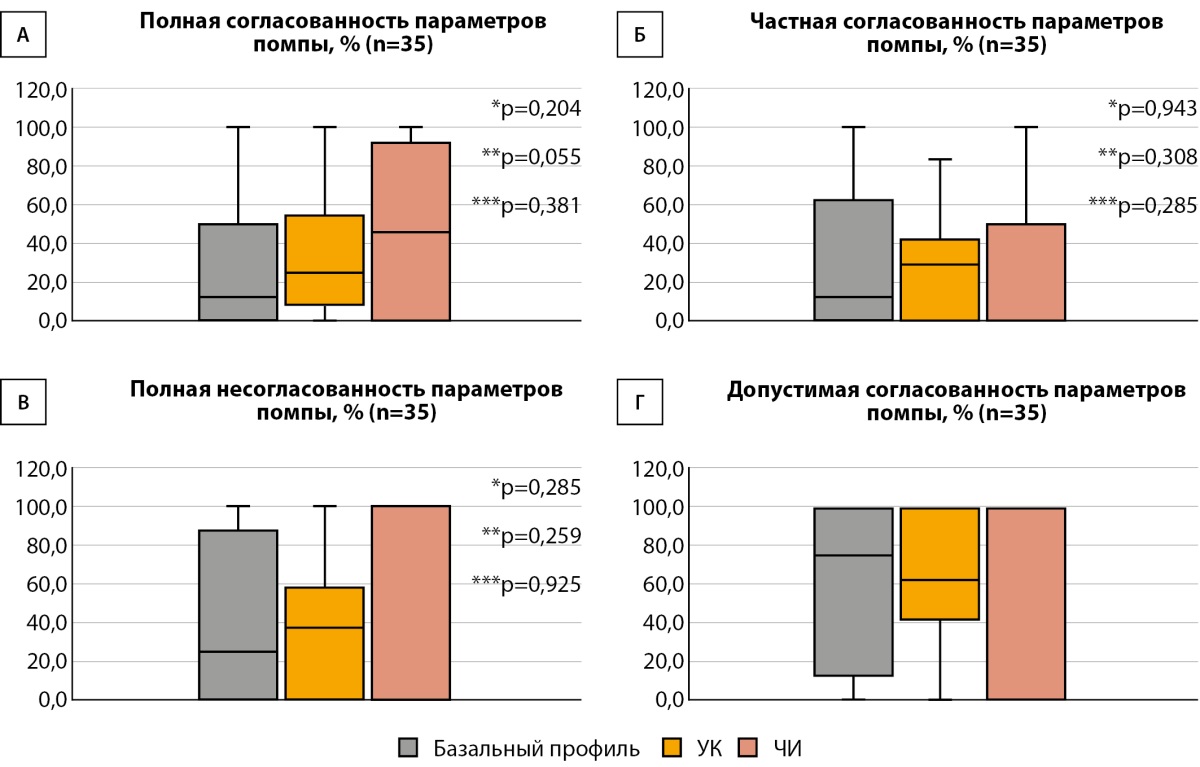
Рисунок 4. Степени согласованности рекомендаций между системой поддержки принятия врачебных решений и врачами (Ме, Q1–Q3, min, max).
Примечание. УК — углеводный коэффициент; ЧИ — коэффициент чувствительности к инсулину.
* — соотношение базального профиля и УК по критерию Уилкоксона.
** — соотношение базального профиля и ЧИ по критерию Уилкоксона.
*** — соотношение УК и ЧИ по критерию Уилкоксона.
Значимых различий в медианных показателях параметров инсулиновой помпы между СППВ и врачами нет (рис. 5). Медиана часового показателя базальной скорости, предложенного СППВР составила 0,38 Ед/час [ 0,22; 0,61], врачом — 0,4 Ед/час [ 0,17; 0,51] (р=0,541). Медиана среднесуточного показателя УК, предложенного СППВР составила 0,85 Ед/ХЕ [ 0,7; 1,03], врачом — 0,83 Ед/ХЕ [ 0,74; 1,1] (р=0,906). Медиана среднесуточного показателя ЧИ, предложенного СППВР составила 6,3 ммоль/л [ 4,9; 9,8], врачом — 6,5 ммоль/л [ 4,2; 9,7] (р=0,963).
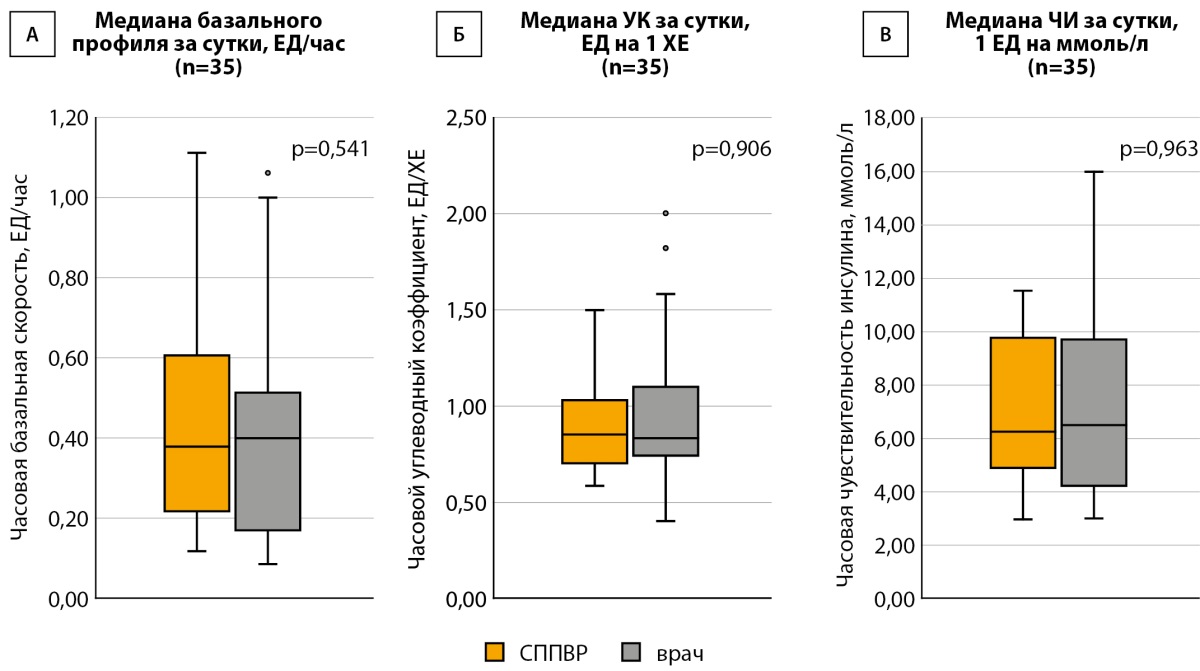
Рисунок 5. Сравнение медианы показателей параметров помпы за сутки между системой поддержки принятия врачебных решений и врачами (Ме, Q1–Q3, min, max).
Примечание. СППВР — система поддержки принятия врачебных решений; УК — углеводный коэффициент; ЧИ — коэффициент чувствительности к инсулину; ХЕ — хлебная единица.
ОБСУЖДЕНИЕ
Разработка математической модели по первичной настройке инсулиновой помпы
В данной работе мы продемонстрировали процедуру разработки на большой выборке детей с СД1 простой искусственной НС — многослойного перцептрона, для предсказания параметров помповой инсулинотерапии на основании четырех, доступных в большинстве случаев врачу, предикторов. Для практического использования полученной модели нами было разработано веб-приложение — СППВР. Система предназначена для врачей-детских эндокринологов и помогает рассчитать настройки базального профиля и калькулятора помощника болюса при инициации помповой инсулинотерапии у детей с СД1.
Несмотря на то, что помповая инсулинотерапия активно используется у пациентов с СД1, первичная настройка параметров помповой терапии может представлять трудности для врачей, что может являться барьером к распространению и использованию помповой терапии [13] и отражаться на показателях профилей глюкозы в первое время.
Настройки инсулиновой помпы определяют количество вводимого инсулина в болюсном (приемы пищи и коррекция гипергликемии) и базальном режимах (фоновое введение инсулина). В отличие от традиционной инсулинотерапии путем множественных инъекций инсулина (МИИ) схема инсулинотерапии на помповой терапии, как правило, более дифференцирована и в целом существует возможность установить различное дозирование на каждые 30–60 минут в течение суток.
На сегодняшний день не существует валидизированных алгоритмов определения дозировок инсулина на помпе у детей и в основном при инициации помповой терапии врачи полагаются на текущую схему введения инсулина [14], при этом коэффициенты УК и ЧИ могут рассчитываться по различным формулам [1][2][15]. Основными показателями, от которых зависят количественные значения вводимого инсулина инсулиновой помпой является СДИ и вес пациента [15][16]. В то же время другие клинические характеристики могут определять качественные особенности введения инсулина в течение суток. Так у детей, возраст пациента определяет особенности распределения базального инсулина в течение суток [2][6], а HbA1c может указывать на необходимость корректировки СДИ в большую (при высоком значении НbА1с) или меньшую (при низком значении НbА1с) сторону.
Таким образом, разработанный алгоритм может не только упростить и ускорить работу врача, но и обеспечить более точный расчет параметров помповой инсулинотерапии, с учетом клинических и возрастных особенностей ребенка с СД1.
Оценка согласованности предсказания модели и рекомендации врача
Для оценки возможности клинического использования, нами проведена оценка сопоставимости предсказаний модели НС (рекомендаций СППВР) с рекомендациями врачей при инициации помповой инсулинотерапии у детей с СД1. В целом наблюдалась сопоставимая согласованность (статистически не значимые различия) различных параметров инсулиновой помпы: базального профиля, УК и ЧИ, что говорит о равномерности распределения согласованных и несогласованных решений между этими параметрами. Помимо этого, рекомендации СППВР в отношении медианных показателей базальной скорости, УК и ЧИ значимо не различались с рекомендациями врачей — экспертов, что указывает на общую сопоставимость рекомендаций врача и системы.
Сопоставление с другими публикациями
В настоящее время нет отечественных и зарубежных исследований по оценке согласованности рекомендаций между СППВР и врачом по первичной настройке инсулиновой помпы, однако есть исследование по оценке согласованности в коррекции инсулинотерапии пациентов, которые уже находятся на помповой инсулинотерапии. В исследовании Nimri R с соавт.[16] оценивалась согласованность между врачами (26 специалистов из 16 стран), а также между врачами и автоматизированным алгоритмом Advisor Pro (DreaMed Diabetes Ltd, Петах-Тиква, Израиль) в коррекции помповой инсулинотерапии у 15 пациентов с СД1 (средний возраст составил 16,2 года ±4,3, средний уровень HbA1c 8,3%±0,9. Полная согласованность оценивалась, когда оба специалиста хотели изменить показатель в одном направлении (например, увеличить УК); частичная согласованность — когда один специалист хотел изменить показатель, а второй оставить его без изменений; полная несогласованность — когда оба специалиста предлагали противоположные рекомендации по одному параметру. Полное согласие между врачами, а таже между врачами и программой по всем трем параметрам инсулиновой помпы было одинаковым ~45% (среднее значение). Было обнаружено, что уровень разногласий несколько выше для коррекции базального профиля, чем для коррекции УК и ЧИ. В нашем исследовании также выявлено, что уровень полной несогласованности по первичной настройке базального профиля несколько выше, чем для УК и ЧИ.
Как видно, указанное исследование демонстрирует не высокую согласованность в принятии клинических решений между различными специалистами. Учитывая, что в исследовании Nimri R с соавт. [17] оценивалась согласованность между врачами и программой по коррекции инсулинотерапии, а в нашем по первичной настройке инсулиновой помпы, а также отсутствие статистически значимых различий между разработанной нами СППВР и врачом, мы считаем, что программа дает приемлемые рекомендации по первичной настройке параметров инсулиновой помпы.
Клиническая значимость результатов
Применение СППВР позволит сэкономить врачам — детским эндокринологам время на первичную настройку инсулиновой помпы. Кроме того, это потенциально может повысить эффективность лечения и сократить время на подбор настроек инсулиновой помпы, который проводится эмпирически по показателям профиля глюкозы, особенно в случае применения медицинскими работниками с недостаточным опытом работы с помповой инсулинотерапией.
Ограничения исследования
На этапе разработки модели и тестирования согласованности рекомендаций СППВР и врача потенциальным ограничением исследования, согласно адаптированному Кокрановскому опроснику [18], является конфликт интересов — разработчики СППВР предоставили лечащим врачам рекомендации СППВР по первичной настройке инсулиновой помпы, после чего разработчики провели аналитику по частоте согласованности рекомендаций СППВР с экспертным мнением врачей.
ЗАКЛЮЧЕНИЕ
Нами представлены результаты разработки на большой выборке пациентов алгоритма, в основе которого лежит НС, первичной настройки инсулиновой помпы и клинической оценки СППВР, созданной на базе этой модели. Алгоритм демонстрирует приемлемую производительность, а СППВР — сопоставимость рекомендаций по сравнению с мнением врачей-экспертов, без значимых отклонений между различными параметрами.
ДОПОЛНИТЕЛЬНАЯ ИНФОРМАЦИЯ
Источники финансирования. Исследование выполнено при финансовой поддержке Министерства науки и высшего образования Российской Федерации (номер гранта: 075-15-2022-310).
Участие авторов. Лаптев Д.Н. — дизайн исследования, сбор данных настроек инсулиновой помпы, статистическая обработка, разработка модели и подбор параметров нейронной сети, написание кода СППВР, написание текста публикации; Сорокин Д.Ю. — проведение клинического исследования, статистический анализ полученных данных исследования, написание текста публикации.
Все авторы одобрили финальную версию статьи перед публикацией, выразили согласие нести ответственность за все аспекты работы, подразумевающую надлежащее изучение и решение вопросов, связанных с точностью или добросовестностью любой части работы.
Благодарности. Авторы выражают благодарность сотрудникам детского отделения сахарного диабета ГНЦ РФ ФГБУ «НМИЦ эндокринологии» МЗ РФ: Андриановой Екатерине Андреевне, Емельянову Андрею Олеговичу, Ереминой Ирине Александровне, Кураевой Тамаре Леонидовне, Светловой Галине Николаевне, Сечко Елене Александровне, Титович Елене Витальевне — в оценке согласованности рекомендации между СППВР и экспертным мнением врача в первичной настройке инсулиновой помпы.
Список литературы
1. Walsh J, Roberts R, Bailey T. Guidelines for insulin dosing in continuous subcutaneous insulin infusion using new formulas from a retrospective study of individuals with optimal glucose levels. J Diabetes Sci Technol. 2010;4(5):1174-1181. https://doi.org/10.1177/193229681000400516
2. Лаптев Д.Н., Филиппов Ю.И., Емельянов А.О., Кураева Т.Л. Оптимизация настроек инсулиновых помп у детей и подростков с сахарным диабетом 1 типа с учетом возрастных особенностей // Сахарный диабет. — 2013. — Т. 16. — №3. — С.:109-115. https://doi.org/10.14341/2072-0351-98
3. Bongiovanni M, Fresa R, Visalli N, et al. A Study of the Carbohydrate-to-Insulin Ratio in Pregnant Women with Type 1 Diabetes on Pump Treatment. Diabetes Technol Ther. 2016;18(6):360-365. https://doi.org/10.1089/dia.2015.0246
4. Streun GL, Elmiger MP, Dobay A, et al. A machine learning approach for handling big data produced by high resolution mass spectrometry after data independent acquisition of small molecules - Proof of concept study using an artificial neural network for sample classification. Drug Test Anal. 2020;12(6):836-845. https://doi.org/10.1002/dta.2775
5. Rong D, Xie L, Ying Y. Computer vision detection of foreign objects in walnuts using deep learning. Comput Electron Agric. 2019;162:1001–1010. https://dx.doi.org/10.1016/j.compag.2019.05.019
6. Holterhus PM, Odendahl R, Oesingmann S, et al. Classification of distinct baseline insulin infusion patterns in children and adolescents with type 1 diabetes on continuous subcutaneous insulin infusion therapy. Diabetes Care. 2007;30(3):568-573. https://doi.org/10.2337/dc06-2105
7. Encyclopedia of Information Science and Technology, Fourth Edition: / ed. Khosrow-Pour, D.B.A. M. IGI Global, 2018
8. Pedregosa F, Varoquaux G, Gramfort A, et al. Scikit-learn: Machine learning in Python. J Mach Learn Res. 2011
9. Kingma DP, Ba J. Adam: A Method for Stochastic Optimization. 3rd Int Conf Learn Represent ICLR 2015 - Conf Track Proc. December 2014. http://arxiv.org/abs/1412.6980
10. Романенкова Е.М., Еремина И.А., Титович Е.В., и др. Уровень С-пептида и распространенность панкреатических аутоантител у детей с сахарным диабетом 1 типа при разной длительности заболевания // Сахарный диабет. — 2022. — Т. 25. — No2. — С.155-165. https://doi.org/10.14341/DM12843
11. Лаптев Д.Н., Безлепкина О.Б., Демина Е.С., и др. Результаты клинической апробации системы freestyle libre у детей с сахарным диабетом 1 типа: улучшение гликемического контроля в сочетании со снижением риска тяжелой гипогликемии и диабетического кетоацидоза // Проблемы эндокринологии. — 2022. — Т. 68. — №3. — С. 86-92. https://doi.org/10.14341/probl12877
12. Лаптев Д.Н., Емельянов А.О., Андрианова Е.А., и др. Применение Flash-мониторинга глюкозы у детей с сахарным диабетом 1 типа в реальной клинической практике // Сахарный диабет. — 2021. — Т. 24. — №6. — С.504-510. https://doi.org/10.14341/DM12817
13. Gajewska KA, Biesma R, Bennett K, Sreenan S. Barriers and facilitators to accessing insulin pump therapy by adults with type 1 diabetes mellitus: a qualitative study. Acta Diabetol. 2021;58(1):93-105. https://doi.org/10.1007/s00592-020-01595-5
14. Sherr JL, Schoelwer M, Dos Santos TJ, et al. ISPAD Clinical Practice Consensus Guidelines 2022: Diabetes technologies: Insulin delivery. Pediatr Diabetes. 2022;23(8):1406-1431. https://doi.org/10.1111/pedi.13421
15. Alemzadeh R, Hoffmann RG, Dasgupta M, Parton E. Development of optimal kids insulin dosing system formulas for young children with type 1 diabetes mellitus. Diabetes Technol Ther. 2012;14(5):418-422. https://doi.org/10.1089/dia.2011.0184
16. Bode BW, Sabbah HT, Gross TM, Fredrickson LP, Davidson PC. Diabetes management in the new millennium using insulin pump therapy. Diabetes Metab Res Rev. 2002;18 Suppl 1:S14-S20. https://doi.org/10.1002/dmrr.205
17. Nimri R, Dassau E, Segall T, et al. Adjusting insulin doses in patients with type 1 diabetes who use insulin pump and continuous glucose monitoring: Variations among countries and physicians. Diabetes Obes Metab. 2018;20(10):2458-2466. https://doi.org/10.1111/dom.13408
18. Реброва О.Ю., Федяева В.К., Хачатрян Г.Р. Адаптация и валидизация вопросника для оценки риска систематических ошибок в рандомизированных контролируемых испытаниях // Медицинские технологии. Оценка и выбор. — 2015. — Т.19. — №1. — С.9-17
Об авторах
Д. Н. ЛаптевРоссия
Лаптев Дмитрий Никитич - д.м.н., профессор; Researcher ID: O-1826-2013; Scopus Author ID: 24341083800.
Москва
Конфликт интересов:
Имеется конфликт интересов - клиническое исследование проводилось группой лиц, принимавших участие в разработке СППВР.
Д. Ю. Сорокин
Россия
Сорокин Даниил Юрьевич; Researcher ID: HJY-5714-2023.
117036, Москва, улица Дм. Ульянова, д. 11
Конфликт интересов:
Имеется конфликт интересов - клиническое исследование проводилось группой лиц, принимавших участие в разработке СППВР.
Дополнительные файлы
|
|
1. Рисунок 1. Коэффициент детерминации R2 модели, полученный на валидационной выборке в зависимости от количества предикторов в процессе их последовательного добавления по убыванию статистической величины. | |
| Тема | ||
| Тип | Исследовательские инструменты | |
Посмотреть
(247KB)
|
Метаданные ▾ | |
|
|
2. Рисунок 2. Значение функции потерь (А) и коэффициента детерминации R2 (Б) на тренировочной выборке. | |
| Тема | ||
| Тип | Исследовательские инструменты | |
Посмотреть
(217KB)
|
Метаданные ▾ | |
|
|
3. Рисунок 3. Интерфейс системы поддержки принятия врачебных решений. | |
| Тема | ||
| Тип | Исследовательские инструменты | |
Посмотреть
(502KB)
|
Метаданные ▾ | |
|
|
4. Рисунок 4. Степени согласованности рекомендаций между системой поддержки принятия врачебных решений и врачами (Ме, Q1–Q3, min, max). | |
| Тема | ||
| Тип | Исследовательские инструменты | |
Посмотреть
(541KB)
|
Метаданные ▾ | |
|
|
5. Рисунок 5. Сравнение медианы показателей параметров помпы за сутки между системой поддержки принятия врачебных решений и врачами (Ме, Q1–Q3, min, max). | |
| Тема | ||
| Тип | Исследовательские инструменты | |
Посмотреть
(435KB)
|
Метаданные ▾ | |
Рецензия
Для цитирования:
Лаптев Д.Н., Сорокин Д.Ю. Система помощи принятия врачебных решений на базе искусственного интеллекта для первичной настройки параметров инсулиновой помпы у детей с сахарным диабетом 1 типа. Сахарный диабет. 2024;27(6):555-564. https://doi.org/10.14341/DM13081
For citation:
Laptev D.N., Sorokin D.Y. Neural network based clinical decision support system for the calculation the initial continuous subcutaneous insulin infusion settings. Diabetes mellitus. 2024;27(6):555-564. (In Russ.) https://doi.org/10.14341/DM13081
JATS XML

Контент доступен под лицензией Creative Commons Attribution-NonCommercial-NoDerivatives 4.0 International License (CC BY-NC-ND 4.0).















































