Перейти к:
Индивидуализация базальной инсулинотерапии сахарного диабета 2 типа: данные крупных рандомизированных контролируемых исследований
https://doi.org/10.14341/DM12774
Аннотация
Начало инсулиновой терапии с аналогов базального инсулина стало стандартом лечения сахарного диабета 2 типа (СД2). Своевременное назначение инсулина позволяет не только замедлить прогрессирование СД2, но и снизить частоту и тяжесть связанных с ним осложнений. В настоящей работе проведен обзор эффективности и безопасности применения новейших базальных аналогов инсулина при СД2 с позиции современных клинических рекомендаций, а также рассмотрены обновленные данные по эффективности и безопасности терапии различными представителями класса с учетом их влияния на риск гипогликемий и вариабельность гликемии. Имеющиеся данные свидетельствуют о том, что инсулин деглудек 200 Ед/мл может быть препаратом выбора при высоком риске развития тяжелых форм гипогликемии. Поскольку тяжелая гипогликемия и высокая вариабельность гликемии являются важными факторами риска сердечно-сосудистых событий и смертности, в настоящее время представляется целесообразным подходить более дифференцированно к назначению конкретного инсулина при лечении СД2 с учетом влияния на риск гипогликемий и вариабельность гликемии.
Для цитирования:
Недогода С.В., Барыкина И.Н., Саласюк А.С., Лутова В.О., Попова Е.А. Индивидуализация базальной инсулинотерапии сахарного диабета 2 типа: данные крупных рандомизированных контролируемых исследований. Сахарный диабет. 2022;25(6):564-569. https://doi.org/10.14341/DM12774
For citation:
Nedogoda S.V., Barykina I.N., Salasyuk A.S., Lutova V.O., Popova E.A. Individualisation of basal insulin therapy of type 2 diabetes: evidence from large randomized controlled trials. Diabetes mellitus. 2022;25(6):564-569. (In Russ.) https://doi.org/10.14341/DM12774
ВВЕДЕНИЕ
Недостаточная секреция инсулина является основным патогенетическим механизмом развития и прогрессирования сахарного диабета 2 типа (СД2), и поэтому инсулинотерапия остается краеугольным камнем лечения данной патологии.
Инсулин — это мощный сахароснижающий агент с доказанной эффективностью в отношении снижения уровня гликированного гемоглобина (HbA1c). Помимо этого, своевременная инсулинотерапия представляет собой один из наиболее эффективных инструментов защиты функции β-клеток поджелудочной железы, эндотелия и других конечных органов от вредного воздействия гипергликемии [1]. Даже у пациентов с тяжелой гипергликемией (HbA1c>9–10%) на момент постановки диагноза инсулин способен контролировать глюко- и липотоксичность в течение нескольких дней терапии путем подавления избыточной периферической инсулинорезистентности, гликогенеза в печени, липолитической активности жировой ткани и низкоинтенсивного неинфекционного воспаления [1][2]. Имеются убедительные доказательства того, что лечение инсулином может привести к длительному восстановлению остаточной функции β-клеток поджелудочной железы [3][4]. При ранней инсулинотерапии стойкая ремиссия дисгликемии была достигнута почти в 50% случаев, а прогрессирование диабета значительно снижалось по сравнению со стандартным лечением [2].
Таким образом, своевременное назначение инсулина может замедлить прогрессирование диабета, снизить частоту и тяжесть связанных с диабетом осложнений. При этом именно базальный инсулин является предпочтительным стартовым вариантом в большинстве клинических ситуаций [2].
Внедрение в клиническую практику аналогов базального инсулина изменило парадигму и стало стандартом лечения СД2. Простота введения, легкость корректировки дозы и контроля уровня гликемии, низкий относительный риск гипогликемии иограниченная прибавка массы тела повысили уверенность врачей и пациентов в принятии решений о старте инсулинотерапии [5].
ПОЗИЦИИ БАЗАЛЬНЫХ ИНСУЛИНОВ В РЕКОМЕНДАЦИЯХ
Согласно позиции Клинических рекомендаций по лечению взрослых пациентов с СД2 Министерства здравоохранения РФ и обновленного 10-го выпуска «Алгоритмов специализированной медицинской помощи больным сахарным диабетом» [6][7], назначение базального инсулина либо фиксированной комбинации базального инсулина и агониста рецепторов глюкагоноподобного пептида 1 типа рекомендуется пациентам с СД2 при уровне HbА1c, превышающем индивидуальный целевой на фоне неэффективности диеты и оптимальной дозы других сахароснижающих препаратов или их комбинаций, для улучшения гликемического контроля.
При этом рекомендации отдают предпочтение использованию в качестве базального инсулина аналогов инсулина длительного и сверхдлительного действия пациентами с СД2 для уменьшения риска гипогликемий и/или вариабельности гликемии (уровень убедительности рекомендаций — А; уровень достоверности доказательств — 1).
Имеется прямое указание на то, что «при сопоставимой сахароснижающей эффективности инсулины НПХ (нейтральный протамин Хагедорна) характеризуются более высоким риском гипогликемий по сравнению с аналогами инсулина длительногои сверхдлительного действия. Аналоги инсулина гларгин 300 Ед/мл и деглудек характеризуются меньшим риском гипогликемий по сравнению с гларгином 100 Ед/мл и детемир» [7], несмотря на то, что на настоящий момент достаточно мало прямых рандомизированных клинических исследований (РКИ), сравнивающих между собой данные альтернативы.
Клинические рекомендации по лечению СД Американской диабетической ассоциации также свидетельствуют, что базальный инсулин является наиболее удобной начальной схемой введения инсулина и может быть добавлен к метформину и другим пероральным препаратам [8], кроме того, даже относительно молодым пациентам с выраженной гипергликемией (уровень глюкозы в крови ≥13,9 ммоль/л или HbA1с≥8,5%) без ацидоза на момент постановки диагноза, которые имеют симптомы полиурии, полидипсии, никтурии и/или потери массы тела, сначала следует назначить базальный инсулин, пока назначают и титруют метформин [9]. В то же время эксперты призывают при выборе инсулинов использовать подход, ориентированный напациента, оценивая влияние терапии на сердечно-сосудистые (СС) и почечные сопутствующие заболевания, эффективность, а также риск гипербазализации при терапии инсулином (клинические сигналы, которые могут свидетельствовать огипербазализации: доза базального инсулина более 0,5 МЕ/кг, высокая вариабельность гликемии, гипогликемии) [10].
Таким образом, анализ последних рекомендаций по лечению СД2 подтверждает наличие преимуществ длительно действующих базальных инсулинов как препаратов выбора для старта инсулинотерапии, несмотря на необходимость дальнейшего анализа реальной клинической практики.
СЕРДЕЧНО-СОСУДИСТАЯ БЕЗОПАСНОСТЬ БАЗАЛЬНОЙ ИНСУЛИНОТЕРАПИИ
Еще в 2008 г. FDA (Управление по санитарному надзору за качеством пищевых продуктов и медикаментов, США), а затем и ЕМЕА (Европейское агентство лекарственных средств) ввели требование обязательной оценки безопасности всех сахароснижающих препаратов с проверкой нулевой гипотезы об отсутствии увеличения риска СС-исходов на фоне нового препарата по сравнению с плацебо (non-inferiority) [11].
Первым РКИ, оценившим сердечно-сосудистую безопасность базальной инсулинотерапии, стало исследование ORIGIN. Показано, что назначение инсулина гларгин 100 Ед/мл не оказывало значимого влияния на риск СС-смерти или развития основных СС-событий (были рандомизированы 12 537 человек, средний период наблюдения — 6,2 года) [12].
Пять лет спустя были опубликованы результаты СС-безопасности нового сверхдлительного аналога инсулина деглудек. РКИ DEVOTE — это международное многоцентровое двойное слепое клиническое исследование, в котором исследовалась СС-безопасность инсулина деглудек по сравнению с инсулином гларгин 100 Ед/мл в течение 104 нед. Кроме того, DEVOTE стало первым РКИ с оценкой СС-безопасности, в котором сравнивались два базальных инсулина, с участием более 7,5 тыс. пациентов с СД2 и высоким риском развития СС-заболеваний или их наличием, которые уже получали терапию в соответствии со стандартами медицинской помощи для снижения СС-риска. Исследование показало, что деглудек не повышал СС-риск посравнению с инсулином гларгин 100 Ед/мл и обеспечивал значительное снижение частоты тяжелых и тяжелых ночных гипогликемий (тяжелых гипогликемий — на 40% и тяжелых ночных гипогликемий — на 53% по сравнению с инсулином гларгин 100 Ед/мл) при сопоставимом уровне гликемического контроля [13].
Следует отметить, что активным препаратом сравнения, использованным в этом исследовании, был инсулин гларгин 100 Ед/мл (U100). В настоящее время в РФ также используется инсулин гларгин 300 Ед/мл, имеющий улучшенные фармакокинетические и фармакодинамические свойства [14].
Таким образом, показано, что новейшие базальные аналоги длительного (инсулин гларгин 300 Ед/мл) и сверхдлительного (инсулин деглудек) действия могут вызывать более низкий риск гипогликемии по сравнению с гларгином 100 Ед/мл при использовании в комбинации с пероральными препаратами [13][15–18], однако сравнение их эффективности является предметом активного изучения.
ГИПОГЛИКЕМИИ И СЕРДЕЧНО-СОСУДИСТЫЙ РИСК
Хорошо известно, что для пациентов с СД2 тяжелая гипогликемия является важным фактором риска СС событий и смертности, а частота ее развития недооценивается [19].
Когортное исследование, проведенное в Дании, показало, что за последние два десятилетия (с 1996 по 2017 гг.) у пациентов как с СД 1 типа (СД1), так и с СД2 наблюдалась значимая взаимосвязь между эпизодами возникновения тяжелых гипогликемий и риском смерти от любых причин. Для пациентов с СД2 (общее количество включенных в анализ пациентов — 333 581) риск смерти от всех причин повышался после эпизодов тяжелой гипогликемии практически в 2 раза (относительный риск — ОР 1,77; 95% доверительный интервал — ДИ 1,67–1,87), у пациентов с СД1 (n=44 033) ОР смерти от всех причин при наличии в анамнезе тяжелой гипогликемии составил 1,11, 95% ДИ — 1,06–1,17 [20].
Другое крупное популяционное исследование, проведенное в Финляндии [21], также косвенно подтвердило, что различия базальных инсулинов в способности вызывать риск гипогликемий влияют на прогноз пациентов. Были проанализированы данные 23 751 пациента с СД2, инициировавшего базальную инсулинотерапию в 2006–2009 гг., срок наблюдения составил до 4 лет (в среднем 1,7 года). При использовании инсулина НПХ в качестве эталона скорректированные ОР для смертности отвсех причин составили 0,39 (95% ДИ 0,30–0,50) для детемира и 0,55 (95% ДИ 0,44–0,69) для гларгина. По сравнению с гларгином ОР смертности от всех причин для детемира составил 0,71 (95% ДИ 0,54–0,93).
Однако до настоящего времени специалистами используется ограниченное количество параметров оценки эффективности терапии СД, зачастую включающее только оценку HbA1c, глюкозы плазмы натощак и постпрандиальной, несмотря на то, что данные параметры имеют ограниченную прогностическую ценность в отношении оценки риска кардиоваскулярных катастроф.
Показано, что дополнительное использование таких параметров контроля заболевания, как вариабельность гликемии, позволяет более точно оценивать риск пациента. Так, очень интересные данные предоставил субанализ данных исследования DEVOTE, изучивший связь повседневной гликемической вариабельности (измерение уровня глюкозы в крови перед завтраком) с тяжелой гипогликемией и СС-исходами [22]. Показано, что вариабельность гликемии была значимо связана с частотой тяжелых гипогликемий (ОР 4,11; 95% ДИ 3,15–5,35), больших неблагоприятных СС событий (major adverse cardiovascular events, MACE) (ОР 1,36; 95% ДИ 1,12–1,65) и смертностью от всех причин (ОР 1,58; 95% ДИ 1,23–2,03). Удвоение показателя вариабельности гликемии натощак приводит к повышению риска тяжелой гипогликемии, MACE и смертности от всех причин в 2,7, 1,2 и 1,4 раза соответственно. После внесения поправок на исходные характеристики пациентов сохранялась значимая взаимосвязь вариабельности гликемии натощак с тяжелой гипогликемией и смертностью от всех причин.
Похожие данные были получены при ретроспективном анализе результатов исследований SWITCH 1 и SWITCH 2. Согласно полученным данным, высокая вариабельность гликемии натощак в течение суток приводила к достоверно более высокой частоте развития как общего числа гипогликемий, так и числа симптоматических гипогликемий в ночное время, независимо от типа СД у пациентов [23][24].
Резолюция по итогам первой рабочей встречи Научно-консультативного совета по вопросу «Актуальные проблемы вариабельности гликемии как нового критерия гликемического контроля и безопасности терапии сахарного диабета» [25] актуализировала тот факт, что «вариабельность гликемии четко связана с риском развития тяжелой гипогликемии, нарушением гормонального ответа на гипогликемию и может являться предиктором нарушенного распознавания гипогликемий вдолгосрочной перспективе». Вариабельность гликемии все чаще рассматривается как самостоятельный предиктор микро- и макрососудистых осложнений СД, общей и СС-смертности при СД2, во многом превосходящий по прогностической значимости традиционные критерии достижения контроля СД2 [25][26]. Вариабельность гликемии напрямую связана с усилением оксидативного стресса [27], истощением функции β-клеток и снижением их массы [28], а также, даже в большей степени, чем уровень HbA1c, влияет на показатели, отражающие состояние сосудистой стенки (толщина комплекса интима-медиа сонных артерий и эндотелий-зависимая вазодилатация плечевой артерии), и коронарные артерии [29]
При этом новейшие базальные аналоги инсулина разрабатываются с учетом влияния на вариабельность гликемии, а их использование позволяет максимально имитировать естественную базальную секрецию инсулина, что способствует повышению безопасности инсулинотерапии. В этой связи чрезвычайно интересными являются результаты прямого сравнения новейших базальных инсулинов — деглудек и гларгин 300 Ед/мл.
Данные CONFIRM — крупного ретроспективного наблюдательного исследования реальной клинической практики, сравнивающего эффективность инсулина деглудек и инсулина гларгин 300 Ед/мл, в которое вошли более 4000 взрослых пациентов сСД2, впервые начавших терапию базальным инсулином, показало значительно более низкий уровень HbA1c в течение 6 мес терапии инсулином деглудек по сравнению с инсулином гларгин 300 Ед/мл (-1,5 и -1,2% соответственно; p=0,029).
Риск гипогликемий, вторичная конечная точка данного исследования, был на 30% меньше на терапии инсулином деглудек по сравнению с терапией инсулином гларгин 300 Ед/мл (p=0,045). Также было показано, что пациенты, получающие инсулин деглудек, с большей вероятностью оставались на назначенной терапии. При назначении пациентам инсулина гларгин 300 Ед/мл риск прекращения назначенной терапии был на 37% выше через 2 года терапии (p<0,001) [30].
Отдельного обсуждения требуют результаты исследования CONCLUDE [31]. Это прямое рандомизированное открытое многонациональное сравнительное исследование оценки частоты гипогликемий при применении инсулина деглудек 200 Ед/мл иинсулина гларгин 300 Ед/мл у пациентов с СД2, получавших базальный инсулин, включило 1609 рандомизированных участников. Конечные точки оценивались в течение 36-недельного периода титрования дозы и общего периода лечения до 88 нед. Несмотря на то что общая частота развития гипогликемий не была значительно ниже при приеме деглудека 200 Ед/мл по сравнению с гларгином 300 Ед/мл (ОР 0,88; 95% ДИ 0,73–1,06) через 36 нед терапии, было показано значительно меньшее количество ночных симптоматических гипогликемий (ОР 0,63; 95% ДИ 0,48–0,84) и тяжелых гипогликемий (ОР 0,20; 95% ДИ 0,07–0,57) при применении деглудека 200 Ед/мл по сравнению с гларгином 300 Ед/мл. При анализе данных всего периода лечения общая частота развития гипогликемий при приеме деглудека 200 Ед/мл оказалась ниже по сравнению с гларгином 300 Ед/мл (ОР 0,77; 95% ДИ 0,65–0,92), сохранялось превосходство деглудека в отношении снижения риска развития ночных симптоматических и тяжелых гипогликемий (рис. 1).
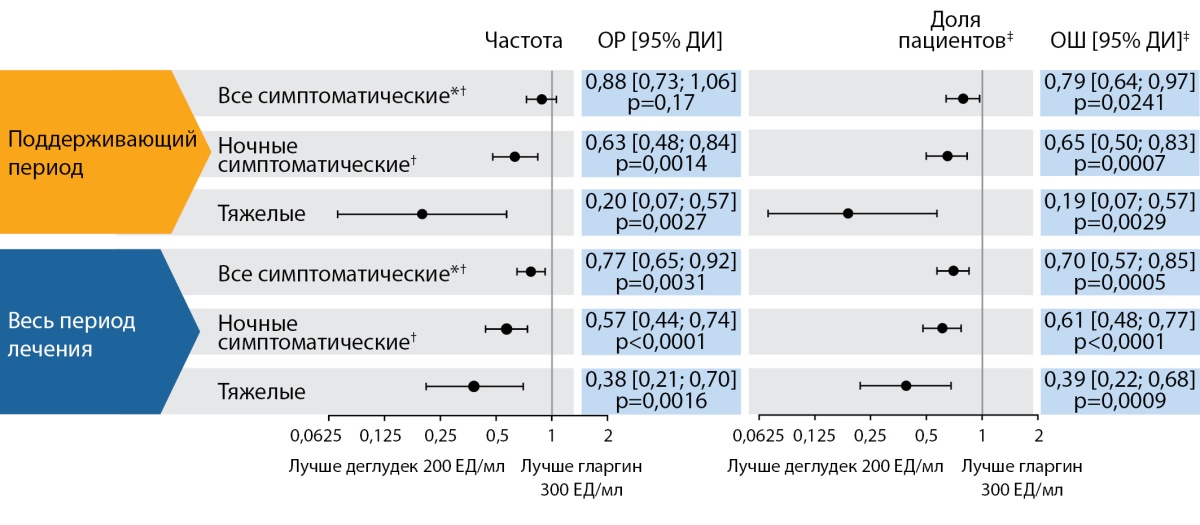
Рисунок 1. Результаты исследования CONCLUDE: гипогликемические события на 100 человеко-лет наблюдения [31][32].
Примечание. *первичная конечная точка; † — событие, определяемое как тяжелое (требующее помощи третьей стороны) или уровень глюкозы в крови <3,1 ммоль/л, подтвержденное симптомами. Все сообщения о ночной гипогликемии поступали в период с 00:01 до 05:59; ‡ — частота развития всех подтвержденных симптоматических гипогликемий в течение поддерживающего периода (первичная конечная точка) была ниже при применении инсулина деглудек по сравнению с инсулином гларгин 300 ЕД/мл (ОР 0,88; 95% ДИ 0,73–1,06; статистически незначимо). Частота развития тяжелых гипогликемий в течение поддерживающего периода (вторичная конечная точка) была ниже при применении инсулина деглудек по сравнению с инсулином гларгин 300 ЕД/мл (ОР 0,20; 95% ДИ 0,07–0,57; p=0,0027, статистически значимо).
Помимо этого, процент участников, у которых наблюдалась общая симптоматическая гипогликемия в течение периода титрации, был ниже у пациентов, получавших деглудек 200 Ед/мл (40,6%), по сравнению с получавшими гларгин 300 Ед/мл (46,3%): OР 0,79 (95% ДИ 0,64–0,97). В течение всего периода лечения частота и доля участников, у которых наблюдалась общая симптоматическая гипогликемия, также были ниже в группе получавших деглудек 200 Ед/мл по сравнению с получавшими гларгин 300 Ед/мл [31].
Как видно из представленных данных, деглудек 200 Ед/мл может рассматриваться как предпочтительный препарат при риске развития тяжелых форм гипогликемии у пациента.
Однако, несмотря на то, что результаты РКИ CONCLUDE представляют большой интерес для клинициста, они требуют осторожной интерпретации. Во-первых, первичная конечная точка не была достигнута, поэтому анализ вторичных конечных точек является исследовательским. До сих пор не объяснены механизмы, которые могут обуславливать преимущество деглудека 200 Ед/мл. Кроме того, РКИ CONCLUDE характеризовалось некоторыми организационными проблемами, связанными с недостаточной надежностью глюкометров, первоначально использовавшихся в исследовании, особенно в диапазонах с низким уровнем глюкозы в крови, поэтому нельзя исключать потенциальное влияние данного факта на конечные результаты исследования [33].
ЗАКЛЮЧЕНИЕ
Несмотря на значительные успехи, инсулинотерапия все еще сталкивается с множеством препятствий, проблем и неопределенностей. Анализ имеющихся данных позволяет сделать вывод о том, что в настоящее время представляется целесообразным подходить более дифференцированно к назначению конкретного инсулина при лечении СД2 с учетом его влияния на конечные точки и количество эпизодов гипогликемий. Кроме того, в РКИ CONCLUDE продемонстрирована важность контроля надежности глюкометров. Недостаточная точность или неправильное использование глюкометра может легко свести на нет любое преимущество современных инсулинов в отношении гликемического контроля и снижения риска гипогликемии.
ДОПОЛНИТЕЛЬНАЯ ИНФОРМАЦИЯ
Источники финансирования. Работа выполнена по инициативе авторов без привлечения финансирования.
Конфликт интересов. Авторы декларируют отсутствие явных и потенциальных конфликтов интересов, связанных с содержанием настоящей статьи.
Участие авторов. Недогода С.В. — определение темы, концепции, дизайна работы, написание текста; Барыкина И.Н. — сбор и анализ материалов, написание текста; Саласюк А.С. — сбор и анализ материалов, написание текста; Лутова В.О. — сбор и анализ материалов, написание текста; Попова Е.А. — сбор и анализ материалов, написание текста.
Все авторы одобрили финальную версию статьи перед публикацией, выразили согласие нести ответственность за все аспекты работы, подразумевающую надлежащее изучение и решение вопросов, связанных с точностью или добросовестностью любой части работы.
Список литературы
1. Owens DR. Clinical evidence for the earlier initiation of insulin therapy in type 2 diabetes. Diabetes Technol Ther. 2013;15(9):776-785. doi: https://doi.org/10.1089/dia.2013.0081
2. Hanefeld M, Fleischmann H, Siegmund T, Seufert J. Rationale for Timely Insulin Therapy in Type 2 Diabetes Within the Framework of Individualised Treatment: 2020 Update. Diabetes Ther. 2020;11(8):1645-1666. doi: https://doi.org/10.1007/s13300-020-00855-5
3. Madnani S, Anjana R, Warade S, et al. Short-term insulin therapy at the time of diagnosis of Type 2 diabetes leads to better glycemic control and improved beta cell function. J Diabetol. 2019;10(3):97. doi: https://doi.org/10.4103/jod.jod_39_18
4. Weng J, Li Y, Xu W, et al. Effect of intensive insulin therapy on beta-cell function and glycaemic control in patients with newly diagnosed type 2 diabetes: a multicentre randomised parallel-group trial. Lancet. 2008;371(9626):1753-1760. doi: https://doi.org/10.1016/S0140-6736(08)60762-X
5. Forst T, Choudhary P, Schneider D, et al. A practical approach to the clinical challenges in initiation of basal insulin therapy in people with type 2 diabetes. Diabetes Metab Res Rev. 2021;37(6):e3418. doi: https://doi.org/10.1002/dmrr.3418
6. Дедов И.И., Шестакова М.В., Майоров А.Ю., и др. Алгоритмы специализированной медицинской помощи больным сахарным диабетом (10-й выпуск) // Сахарный диабет. — 2021. — Т. 24. — №S1. — С.1-235. doi: https://doi.org/10.14341/DM12802
7. КР290. Сахарный диабет 2 типа у взрослых, Общественная организация «Российская ассоциация эндокринологов», 2019 г. Ссылка активна на 10.06.2021 г. Доступно по: http://cr.rosminzdrav.ru/recomend/290_1
8. Forst T, Choudhary P, Schneider D, et al. 9. Pharmacologic Approaches to Glycemic Treatment: Standards of Medical Care in Diabetes — 2021. Diabetes Care. 2021;44(S1):S111-S124. doi: https://doi.org/10.2337/dc21-S009
9. Arslanian S, Bacha F, Grey M, et al. Evaluation and Management of Youth-Onset Type 2 Diabetes: A Position Statement by the American Diabetes Association. Diabetes Care. 2018;41(12):2648-2668. doi: https://doi.org/10.2337/dci18-0052
10. Cowart K. Overbasalization: Addressing hesitancy in treatment intensification beyond basal insulin. Clin Diabetes. 2020;38(3):304-310. doi: https://doi.org/10.2337/cd19-0061
11. Кобалава Ж.Д., Киякбаев Г.К. Сахарный диабет 2 типа и сердечно-сосудистые осложнения: можно ли улучшить прогноз назначением сахароснижающих препаратов? // Российский кардиологический журнал. — 2018. — Т. 44. — №8. — С. 79-91. doi: https://doi.org/10.15829/1560-4071-2018-8-79-91
12. Kobalava ZD, Kiyakbaev GК. Basal Insulin and Cardiovascular and Other Outcomes in Dysglycemia. N Engl J Med. 2012;367(4):319-328. doi: https://doi.org/10.1056/NEJMoa1203858
13. Marso SP, McGuire DK, Zinman B, et al. Efficacy and Safety of Degludec versus Glargine in Type 2 Diabetes. N Engl J Med. 2017;377(8):723-732. doi: https://doi.org/10.1056/NEJMoa1615692
14. Ritzel R, Roussel R, Giaccari A, et al. Better glycaemic control and less hypoglycaemia with insulin glargine 300 U/mL vs glargine 100 U/mL: 1-year patient-level meta-analysis of the EDITION clinical studies in people with type 2 diabetes. Diabetes, Obes Metab. 2018;20(3):541-548. doi: https://doi.org/10.1111/dom.13105
15. Rodbard HW, Cariou B, Zinman B, et al. BEGIN Once Long trial investigators. Comparison of insulin degludec with insulin glargine in insulin-naive subjects with Type 2 diabetes: a 2-year randomized, treat-to-target trial. Diabet Med. 2013;30(11):1298-1304. doi: https://doi.org/10.1111/dme.12303
16. Wysham C, Bhargava A, Chaykin L, et al. Effect of Insulin Degludec vs Insulin Glargine U100 on Hypoglycemia in Patients With Type 2 Diabetes: The SWITCH 2 Randomized Clinical Trial. JAMA. 2017;318(1):45-56. doi: https://doi.org/10.1001/jama.2017.7117
17. Zinman B, Philis-Tsimikas A, Cariou B, et al. Insulin Degludec Versus Insulin Glargine in Insulin-Naive Patients With Type 2 Diabetes. Diabetes Care. 2012;35(12):2464-2471. doi: https://doi.org/10.2337/dc12-1205
18. Bolli GB, Riddle MC, Bergenstal RM, et al. New insulin glargine 300 U/ml compared with glargine 100 U/ml in insulin-naïve people with type 2 diabetes on oral glucose-lowering drugs: a randomized controlled trial (EDITION 3). Diabetes, Obes Metab. 2015;17(4):386-394. doi: https://doi.org/10.1111/dom.12438
19. Frier B. Identifying and treating hypoglycemia in insulin-treated diabetes. J Diabetes Endocr Pract. 2021;04(01):2-3. doi: https://doi.org/10.4103/jdep.jdep_11_21
20. Jensen MH, Dethlefsen C, Hejlesen O, Vestergaard P. Association of severe hypoglycemia with mortality for people with diabetes mellitus during a 20-year follow-up in Denmark: a cohort study. Acta Diabetol. 2020;57(5):549-558. doi: https://doi.org/10.1007/s00592-019-01447-x
21. Strandberg AY, Hoti FJ, Strandberg TE, et al. All-Cause and Cause-Specific Mortality among Users of Basal Insulins NPH, Detemir, and Glargine. PLoS One. 2016;11(3):e0151910. doi: https://doi.org/10.1371/journal.pone.0151910
22. Zinman B, Marso SP, Poulter NR, et al. Day-to-day fasting glycaemic variability in DEVOTE: associations with severe hypoglycaemia and cardiovascular outcomes (DEVOTE 2). Diabetologia. 2018;61(1):48-57. doi: https://doi.org/10.1007/s00125-017-4423-z
23. Bailey TS, Bhargava A, DeVries JH, et al. Day-to-day variability of fasting self-measured plasma glucose (SMPG) correlates with risk of hypoglycemia in adults with type 1 (T1D) or type 2 diabetes (T2D). Diabetes. 2017;66(S1):A104-105(394-P). doi: https://doi.org/10.2337/db17-381-663
24. Bailey TS, Bhargava A, DeVries JH, et al. Within-day variability based on 9-point profiles correlates with risk of overall and nocturnal hypoglycemia in adults with type 1 (t1d) and type 2 diabetes (T2D). Diabetes. 2017;66(S1):A107(404-P). doi: https://doi.org/10.2337/db17-381-663
25. Анциферов М.Б., Галстян Г.Р., Зилов А.В., и др. Резолюция по итогам первой рабочей встречи научно-консультативного совета по вопросу «Актуальные проблемы вариабельности гликемии как нового критерия гликемического контроля и безопасности терапии сахарного диабета» // Сахарный диабет. — 2019. — Т. 22. — №3. — С. 281-288. doi: https://doi.org/10.14341/DM10227
26. Nalysnyk L, Hernandez-Medina M, Krishnarajah G. Glycaemic variability and complications in patients with diabetes mellitus: evidence from a systematic review of the literature. Diabetes Obes Metab. 2010;12(4):288-298. doi: https://doi.org/10.1111/j.1463-1326.2009.01160.x
27. Ohara M, Fukui T, Ouchi M, et al. Relationship between daily and day-to-day glycemic variability and increased oxidative stress in type 2 diabetes. Diabetes Res Clin Pract. 2016;122(1):62-70. doi: https://doi.org/10.1016/j.diabres.2016.09.025
28. Kohnert KD, Freyse EJ, Salzsieder E. Glycaemic variability and pancreatic β-cell dysfunction. Curr Diabetes Rev. 2012;8(5):345-354. doi: https://doi.org/10.2174/157339912802083513
29. Zhang X, Xu X, Jiao X, et al. The Effects of Glucose Fluctuation on the Severity of Coronary Artery Disease in Type 2 Diabetes Mellitus. J Diabetes Res. 2013;2013(1):1-6. doi: https://doi.org/10.1155/2013/576916
30. Tibaldi J, Hadley-Brown M, Liebl A, et al. A comparative effectiveness study of degludec and insulin glargine 300 U/mL in insulin-naïve patients with type 2 diabetes. Diabetes Obes Metab. 2019;21(4):1001-1009. doi: https://doi.org/10.1111/dom.13616
31. Philis-Tsimikas A, Klonoff DC, Khunti K, et al. CONCLUDE Study Group. Risk of hypoglycaemia with insulin degludec versus insulin glargine U300 in insulin-treated patients with type 2 diabetes: the randomised, head-to-head CONCLUDE trial. Diabetologia. 2020;63(4):698-710. doi: https://doi.org/10.1007/s00125-019-05080-9
32. 55th EASD Annual Meeting, 2019. Session: CONCLUDE: a trial COmparing the efficacy aNd safety of insulin degLUDEc and insulin glargine 300 units/mL in subjects with type 2 diabetes mellitus inadequately treated with basal insulin and oral antidiabetic drugs [cited 10.06.2021]. Available from: https://www.easd.org/virtualmeeting/home.html%20#!resources/commentary-647369f8-68f1-41d3-9d0b-b5ba9b3cb1ac
33. Del Prato S. How conclusive is the CONCLUDE trial? Diabetologia. 2020;63(4):692-697. doi: https://doi.org/10.1007/s00125-020-05086-8
Об авторах
С. В. НедогодаРоссия
Недогода Сергей Владимирович, д.м.н., профессор
Researcher ID: O-4656-2014; Scopus Author ID: 6507198479; eLibrary SPIN: 7005-7846
Волгоград
Конфликт интересов:
Автор декларирует отсутствие явных и потенциальных конфликтов интересов, связанных с содержанием настоящей статьи.
И. Н. Барыкина
Россия
Барыкина Ирина Николаевна, к.м.н., доцент
Researcher ID: E-2791-2016; Scopus Author ID: 55673000500; eLibrary SPIN: 5894-7499
Волгоград
Конфликт интересов:
Автор декларирует отсутствие явных и потенциальных конфликтов интересов, связанных с содержанием настоящей статьи.
А. С. Саласюк
Россия
Саласюк Алла Сергеевна, д.м.н.
Researcher ID: D-1795-2016; Scopus Author ID: 55807712600; eLibrary SPIN: 2651-2916
400001, Волгоград, ул. Циолковского, д. 1
Конфликт интересов:
Автор декларирует отсутствие явных и потенциальных конфликтов интересов, связанных с содержанием настоящей статьи.
В. О. Лутова
Россия
Лутова Виктория Олеговна, к.м.н.
Researcher ID: D-1884-2016; Scopus Author ID: 57189647005; eLibrary SPIN: 4601-9910
Волгоград
Конфликт интересов:
Автор декларирует отсутствие явных и потенциальных конфликтов интересов, связанных с содержанием настоящей статьи.
Е. А. Попова
Россия
Попова Екатерина Андреевна, к.м.н.
Researcher ID: AAE-7003-2020; Scopus Author ID: 57194330452; eLibrary SPIN: 6983-1086
Волгоград
Конфликт интересов:
Автор декларирует отсутствие явных и потенциальных конфликтов интересов, связанных с содержанием настоящей статьи.
Дополнительные файлы
|
|
1. Рисунок 1. Результаты исследования CONCLUDE: гипогликемические события на 100 человеко-лет наблюдения [31, 32]. | |
| Тема | ||
| Тип | Рисунок | |
Посмотреть
(326KB)
|
Метаданные ▾ | |
Рецензия
Для цитирования:
Недогода С.В., Барыкина И.Н., Саласюк А.С., Лутова В.О., Попова Е.А. Индивидуализация базальной инсулинотерапии сахарного диабета 2 типа: данные крупных рандомизированных контролируемых исследований. Сахарный диабет. 2022;25(6):564-569. https://doi.org/10.14341/DM12774
For citation:
Nedogoda S.V., Barykina I.N., Salasyuk A.S., Lutova V.O., Popova E.A. Individualisation of basal insulin therapy of type 2 diabetes: evidence from large randomized controlled trials. Diabetes mellitus. 2022;25(6):564-569. (In Russ.) https://doi.org/10.14341/DM12774

Контент доступен под лицензией Creative Commons Attribution-NonCommercial-NoDerivatives 4.0 International License (CC BY-NC-ND 4.0).















































