Перейти к:
Деинтенсификация базис-болюсной инсулинотерапии путем перевода на фиксированную комбинацию инсулин гларгин
https://doi.org/10.14341/DM13381
Аннотация
ОБОСНОВАНИЕ. Деинтенсификация базис-болюсной инсулинотерапии (ББИТ) с упрощением режима лечения является возможной и необходимой терапевтической стратегией для ряда пациентов с сахарным диабетом 2 типа (СД2). Одним из вариантов деинтенсификации является переход на фиксированную комбинацию инсулин гларгин/ликсисенатид (иГларЛикси).
ЦЕЛЬ. Определить эффективность и безопасность деинтенсификации ББИТ у госпитализированных больных СД2 путем перевода на иГларЛикси под контролем непрерывного мониторинга глюкозы (НМГ).
МАТЕРИАЛЫ И МЕТОДЫ. Дизайн: одноцентровое сравнительное наблюдательное исследование в реальной клинической практике. Включено 283 пациента с СД2, получающих ББИТ. У 118 больных проведена деинтенсификация ББИТ по клиническим показаниям под контролем НМГ, 165 больных продолжали получать ББИТ. 30 пациентов обследованы повторно спустя год после деинтенсификации. Оценивали время в целевом диапазоне (TIR), время в диапазоне выше целевого (TAR), время в диапазоне ниже целевого (TBR), а также коэффициент вариабельности (СV), среднюю амплитуду колебаний глюкозы (MAGE), индекс лабильности (LI) и скорость изменения уровня глюкозы (MAG). Эндогенную секрецию инсулина оценивали по уровню С-пептида натощак и через 2 часа после еды. Расчетную скорость утилизации глюкозы (рСУГ) использовали как меру чувствительности к инсулину.
РЕЗУЛЬТАТЫ. Группы были сопоставимы по возрасту, длительности СД, уровню гликированного гемоглобина (HbA1c) и рСУГ. Индекс массы тела (ИМТ) и уровень С-пептида были выше, а длительность инсулинотерапии и исходная суточная доза инсулина (СДИ) — ниже у пациентов группы деинтенсификации (все р≤0,0004). В ходе деинтенсификации СДИ была снижена (с 64 до 30 Ед/сут, р<0,001). Достигнутые значения TIR и TBR не различались у пациентов двух групп. У пациентов на иГларЛикси TAR L2 (>13,9 ммоль/л), CV, MAGE и MAG были ниже (все p<0,05). В многофакторном регрессионном анализе ИМТ, СДИ и С-пептид натощак были ассоциированы с успешной деинтенсификацией. В ROC-анализе наилучшим предиктором оказался С-пептид натощак с точкой отсечения 0,92 нг/мл. Через год после деинтенсификации лечения наблюдалось снижение уровня HbA1c (-0,5%, р=0,001) и массы тела (-2 кг, р=0,003), и повышение постпрандиального уровня С-пептида (р=0,029) без изменений рСУГ.
ЗАКЛЮЧЕНИЕ. Переход на иГларЛикси является эффективной терапевтической опцией для больных СД2 с нормальным уровнем С-пептида, нуждающихся в деинтенсификации ББИТ.
Ключевые слова
Для цитирования:
Климонтов В.В., Яковлева С.А., Королева Е.А., Булумбаева Д.М., Мавлянова К.Р., Раисинежад К. Деинтенсификация базис-болюсной инсулинотерапии путем перевода на фиксированную комбинацию инсулин гларгин. Сахарный диабет. 2025;28(5):424-432. https://doi.org/10.14341/DM13381
For citation:
Klimontov V.V., Yakovleva S.A., Koroleva E.A., Bulumbaeva D.M., Mavlianova K.R., Raisinezhad K. Deintensification of basal-bolus insulin therapy by switching to a fixed-ratio combination of insulin glargine and lixisenatide in patients with type 2 diabetes. Diabetes mellitus. 2025;28(5):424-432. (In Russ.) https://doi.org/10.14341/DM13381
ОБОСНОВАНИЕ
Сахарный диабет 2 типа (СД2) — хроническое прогрессирующее заболевание, течение которого нередко требует интенсификации лечения, вплоть до базис-болюсной инсулинотерапии (ББИТ). Последняя, однако, сопряжена с целым рядом ограничений: повышением риска гипогликемии, прибавкой массы тела, многократными инъекциями инсулина, необходимостью частого самоконтроля уровня глюкозы [1]. У пожилых пациентов интенсивный контроль гликемии нередко сопровождается ятрогенными осложнениями, нивелирующими потенциальную пользу [2][3]. Актуальные клинические рекомендации подчеркивают принцип индивидуализации терапевтических целей и допускают более высокие уровни гликированного гемоглобина (HbA1c) для пациентов высокого риска [4]. В связи с этим возрастает значение стратегии деинтенсификации инсулинотерапии, предусматривающей упрощение схем введения инсулина либо снижение доз инсулина с сохранением приемлемого качества гликемического контроля.
За последние годы сформировались новые терапевтические подходы, позволяющие безопасно снижать интенсивность фармакологического вмешательства при СД2. В практику внедрены высокоэффективные классы препаратов — агонисты рецепторов глюкагоноподобного пептида-1 (арГПП-1) и ингибиторы натрий-глюкозного котранспортера 2 (иНГЛТ-2), а также фиксированные комбинации инсулина с арГПП-1, которые обеспечивают достижение целевых значений HbA1c при меньшей потребности в экзогенном инсулине [1]. Наибольшие успехи в стратегии деинтенсификации связаны с использованием арГПП-1. В отличие от инсулина, арГПП-1 способствуют снижению массы тела, одновременно минимизируя риск гипогликемических эпизодов за счет глюкозозависимого механизма действия. По обобщенным данным, деинтенсификация ББИТ с переводом на комбинации базального инсулина и арГПП-1 у пациентов с СД2 приводит к улучшению гликемического контроля, снижению потребности в инсулине, уменьшению числа инъекций и повышению удовлетворенности лечением [5]. Кроме того, перевод пациентов СД2 с ББИТ на комбинацию базального инсулина с арГПП-1 может уменьшать вариабельность гликемии (ВГ) [6]. Последняя рассматривается как неблагоприятный прогностический фактор, ассоциированный с гипогликемией и сердечно-сосудистыми осложнениями СД [7][8].
Широкое применение получила фиксированная комбинация базального аналога инсулина гларгин 100 Ед/мл и арГПП-1 ликсисенатида (иГларЛикси), обеспечивающая эффективный контроль гликемии без набора массы тела и увеличения риска гипогликемии у больных СД2 [9]. Согласно результатам исследования IDEAL (Insulin therapy DE-intensificAtion with iglarLixi), лечение больных СД2 иГларЛикси позволяет достичь целевых показателей гликемии при одновременном снижении массы тела, суточной дозы инсулина (СДИ) и количества ежедневных инъекций в сравнении с ББИТ. С помощью непрерывного мониторинга глюкозы (НМГ) показано увеличение времени в целевом диапазоне на фоне иГларЛикси [10].
ЦЕЛЬ ИССЛЕДОВАНИЯ
Определить эффективность и безопасность деинтенсификации ББИТ у госпитализированных больных СД2 путем перевода на иГларЛикси под контролем НМГ.
МАТЕРИАЛЫ И МЕТОДЫ
Место и время проведения исследования
Исследование проведено на базе отделения эндокринологии клиники НИИКЭЛ — филиал ИЦиГ СО РАН (федеральное учреждение третьего уровня). Анализировались пациенты, получавшие лечение в период с февраля 2019 по декабрь 2024 гг.
Изучаемые популяции
В исследовании участвовали пациенты с СД2 на ББИТ, получавшие плановую специализированную, в том числе высокотехнологичную, медицинскую помощь по профилю «Эндокринология».
Критерии включения: возраст старше 18 лет; установленный диагноз «СД2»; ББИТ в режиме многократных ежедневных инъекций в сочетании или без сочетания с другими сахароснижающими препаратами.
Критерии исключения: беременность, лактация; острая метаболическая декомпенсация (кетоацидоз, гиперосмолярный гипергликемический синдром, лактатацидоз); 4–5 стадия хронической болезни почек (ХБП); острые инфекции, интоксикации, оперативные вмешательства в момент исследования, документированный панкреатит в анамнезе.
Способ формирования выборки из изучаемой популяции
Выборка сформирована сплошным методом на основе вышеизложенных критериев включения и исключения.
Дизайн исследования
Проведено одноцентровое сравнительное наблюдательное исследование в условиях реальной клинической практики.
Участники исследования разделены на 2 группы: 1) пациенты, у которых продолжена ББИТ с коррекцией (при необходимости) доз инсулина; 2) пациенты, которым по решению лечащего врача проведена деинтенсификация инсулинотерапии с переводом на инъекции иГларЛикси (Соликва СолоСтар®, Санофи). Деинтенсификация рассматривалась в следующих ситуациях: 1) два или более эпизодов тяжелой гипогликемии в течение последнего года или один эпизод на фоне нарушенного распознавания гипогликемии (≥4 балла по шкале Clarkе); 2) повторные эпизоды гипогликемии (с клиническими симптомами или без) в течение последних двух недель; 3) фактический уровень HbA1c ниже индивидуального целевого; 4) прогрессирующая прибавка массы тела на фоне ББИТ; 5) низкая приверженность пациента рекомендациям (неадекватный самоконтроль, отсутствие подсчета углеводов, частые пропуски инъекций инсулина и др.); 6) высокий риск гипогликемии на фоне тяжелой сердечно-сосудистой патологии в пожилом и старческом возрасте; 7) улучшение состояния после острого сопутствующего заболевания, потребовавшего временной интенсификации сахароснижающей терапии. Стартовую дозу иГларЛикси рассчитывали с учетом предшествующей дозы и вида базального инсулина, в соответствии с инструкцией к препарату.
Эффективность и безопасность лечения оценивали с использованием НМГ у всех пациентов. Анализ данных НМГ включал расчет параметров времени в диапазонах и параметров ВГ. Часть пациентов, переведенных на иГларЛикси, обследованы повторно через год, во время следующей плановой госпитализации.
Методы
Пациентам проведено клиническое обследование в соответствии с актуальной версией «Алгоритмов оказания специализированной медицинской помощи больным СД» [4]. Способность к распознаванию симптомов гипогликемии определяли по методу Clarke [11]. Уровень гликированного гемоглобина А1с определяли на биохимическом анализаторе AU480 (Beckman Coulter, США). Для оценки эндогенной секреции инсулина определяли уровень С-пептида в сыворотке крови, взятой натощак и через 2 часа после завтрака, методом хемилюминесцентного твердофазного анализа на иммунологическом анализаторе Immulite 2000 XPi (Siemens Healthineers, Германия). Оценку чувствительности к инсулину проводили на основании расчетной скорости утилизации глюкозы (рСУГ) [12].
НМГ проводили с помощью систем MiniMed Paradigm Real-Time MMT-722 и MiniMed 720G MMT (Медтроник, США). Средняя длительность НМГ составила 5 дней. Анализировали следующие параметры: время в целевом диапазоне (TIR, Time In Range, 3,9–10 ммоль/л), время в диапазоне выше целевого, уровни 1 и 2 (TAR, Time Above Range: TAR L-1 10–13,9 ммоль/л; TAR L-2 >13,9 ммоль/л), время в диапазоне ниже целевого, уровни 1 и 2 (TBR, Time Below Range: TBR L-1 3,0–3,9 ммоль/л; TBR L-2 <3,0 ммоль/л) [13]. Рассчитывали следующие параметры ВГ: коэффициент вариабельности (СV, Coefficient of Variation), средняя амплитуда колебаний уровня глюкозы (MAGE, Mean Amplitude of Glycemic Excursions), индекс лабильности (LI, Lability Index), средняя скорость изменения уровня глюкозы (MAG, Mean Absolute Glucose rate of change). В ряду данных параметров CV является мерой дисперсии значений глюкозы, MAGE отражает амплитуду колебаний, LI и MAG отражают скорость изменений уровня глюкозы [14]. Для расчета параметров времени в диапазонах и ВГ использовали программу экспертного анализа данных НМГ CGMEX (свидетельство о регистрации программы для ЭВМ RU 2021616872 от 16.04.2021 г.).
Статистический анализ
Статистическая обработка данных проводилась с использованием программного обеспечения GraphPad Prism 8 (Insight Partners, США). Распределение признаков проверено с помощью критерия Колмогорова-Смирнова. Большинство анализируемых признаков не соответствовали закону нормального распределения. Количественные данные были выражены в виде медиан, 25-го и 75-го перцентилей. Межгрупповые различия по количественному признаку оценивали с помощью критерия Манна-Уитни. Для изучения динамики изменений признака использовали ранговый тест Вилкоксона для парных сравнений. Для выявления факторов, ассоциированных с возможностью деинтенсификации ББИТ, проводили многофакторный регрессионный анализ. Для определения пороговых значений предикторов использовали ROC-анализ.
Этическая экспертиза
Проведение исследования одобрено этическим комитетом НИИКЭЛ — филиал ИЦиГ СО РАН (протокол №172 от 28.04.2022). Все пациенты подписали информирование согласие для участия в исследовании.
РЕЗУЛЬТАТЫ
Характеристика пациентов
В исследование включены 283 пациента с СД2, 92 мужчины и 191 женщина, в возрасте от 18 до 87 лет, получавшие ББИТ до госпитализации. Во время стационарного лечения часть пациентов продолжила получать ББИТ (группа 1, n=165), другая часть по решению лечащего врача была переведена на терапию иГларЛикси (группа 2, n=118).
Группы пациентов были сопоставимы по возрасту, длительности заболевания, уровню HbA1c, отношению «окружность талии/окружность бедер» (ОТ/ОБ), показателям липидного обмена, расчетной скорости клубочковой фильтрации (рСКФ) и рСУГ (табл. 1). ИМТ и уровень С-пептида был выше, а длительность инсулинотерапии и СДИ — ниже у пациентов группы 2. Распространенность артериальной гипертензии, хронической болезни почек (ХБП), нейропатии, макроангиопатии нижних конечностей, синдрома диабетической стопы, ишемической болезни сердца не различалась между группами (все р>0,05).
Таблица 1. Клинико-лабораторная характеристика пациентов с сахарным диабетом 2 типа на разных режимах инсулинотерапии
|
Параметр |
Группы пациентов |
Р |
|
|
1 (ББИТ) N=165 |
2 (иГларЛикси) N=118 |
||
|
Возраст, годы |
66 [ 60; 72] |
67 [ 59; 72] |
0,927 |
|
Длительность СД, годы |
19,5 [ 13; 24] |
18 [ 13; 23] |
0,203 |
|
Длительность инсулинотерапии, годы |
11 [ 6,5; 17] |
9 [ 4; 14] |
0,0002 |
|
ИМТ, кг/м² |
32,3 [ 28,9; 36,6] |
33,6 [ 30,1; 39,1] |
0,026 |
|
ОТ/ОБ |
0,99 [ 0,93; 1,06] |
1,01 [ 0,94; 1,07] |
0,382 |
|
СДИ, Ед |
74 [ 58; 98] |
64 [ 49,3; 83,5] |
0,0004 |
|
СДИ, Ед/кг |
0,84 [ 0,65; 1,05] |
0,67 [ 0,54; 0,90] |
<0,0001 |
|
HbA1c, % |
8,88 [ 7,90; 9,95] |
8,52 [ 7,51; 9,79] |
0,098 |
|
Холестерин, ммоль/л |
4,72 [ 3,88; 5,69] |
5 [ 3,91; 6,12] |
0,159 |
|
Холестерин ЛПНП, ммоль/л |
3,12 [ 2,36; 3,88] |
3,28 [ 2,53; 4,11] |
0,091 |
|
Холестерин ЛПВП, ммоль/л |
1,18 [ 0,98; 1,36] |
1,17 [ 1,01; 1,32] |
0,618 |
|
Триглицериды, ммоль/л |
1,84 [ 1,35; 2,71] |
1,99 [ 1,45; 2,82] |
0,192 |
|
рСКФ, мл/мин/1,73 м² |
65 [ 50; 79] |
63 [ 48; 80] |
0,559 |
|
рСУГ, мг/кг/мин |
3,13 [ 2,02; 4,47] |
3,19 [ 1,92; 4,09] |
0,336 |
|
С-пептид натощак, нг/мл |
0,82 [ 0,16; 1,94] |
1,43 [ 0,92; 2,31] |
<0,0001 |
|
С-пептид через 2 ч. после еды, нг/мл |
1,07 [ 0,32; 2,56] |
2,78 [ 1,7; 4,27] |
<0,0001 |
Примечания: HbA1c — гликированный гемоглобин А1с; ББИТ — базис-болюсная инсулинотерапия; ИМТ — индекс массы тела; ЛПНП — липопротеиды низкой плотности; ЛПВП — липопротеиды высокой плотности; ОТ/ОБ — отношение окружность талии/окружность бедер; рСКФ — расчетная скорость клубочковой фильтрации; рСУГ — расчетная скорость утилизации глюкозы; СД — сахарный диабет; СДИ — суточная доза инсулина.
Пациенты группы 1 получали инсулин NPH (n=28) или аналоги инсулина: гларгин 100 Ед/мл (n=43), гларгин 300 Ед/мл (n=65), детемир (n=5), деглудек (n=24), в комбинации с инсулином короткого действия (n=39) или короткодействующими аналогами инсулина (аспарт, лизпро, глулизин, n=126). Кроме инсулина, применялся метформин (n=148), иНГЛТ-2 (n=148).
Пациенты группы 2 до перевода на иГларЛикси получали инсулин NPH (n=20), гларгин 100 Ед/мл (n=64), гларгин 300 Ед/мл (n=17), детемир (n=4) или деглудек (n=13) в комбинации с инсулином короткого действия (n=22) или аналогами инсулина (аспарт, лизпро, глулизин, n=96). В группе 2 терапия включала метформин (n=108), иНГЛТ-2 (n=86).
Доза инсулина
В группе ББИТ наблюдалось снижение СДИ в 1,16 раза (р=0,0003), при нормировании на массу тела — в 1,16 раза (р=0,0004). В группе иГларЛикси СДИ была снижена в среднем в 2,13 раза в сравнении с таковой при поступлении (p<0,0001). На момент выписки СДИ у пациентов, переведенных на иГларЛикси, была меньше в 2,5 раза в сравнении с пациентами на ББИТ (p<0,0001). После нормирования на массу тела СДИ в группе иГларЛикси уменьшилась в 2,3 раза по сравнению с входящими данными (p<0,0001) и оказалась в 3,2 раза ниже, чем в группе 1 на момент выписки (p<0,0001).
Данные НМГ
Достигнутые значения TIR и среднесуточной гликемии не отличались у пациентов двух групп (табл. 2). При этом у пациентов, остававшихся на ББИТ, доля TAR-L2 была значимо больше, чем у получавших иГларЛикси. Показатели TBR-L1 и TBR-L2 не различались между группами и оставались на нулевых либо минимальных значениях. У больных на иГларЛикси были достигнуты меньшие значения параметров ВГ: CV, MAGE и MAG по сравнению с таковыми у пациентов на ББИТ.
Таблица 2. Параметры непрерывного мониторинга глюкозы у пациентов с сахарным диабетом 2 типа на разных режимах инсулинотерапии
|
Параметр |
Группы пациентов |
Р |
|
|
1 (ББИТ) N=165 |
2 (иГларЛикси) N=118 |
||
|
Среднесуточный уровень глюкозы, ммоль/л |
7,77 [ 7,10; 8,66] |
7,88 [ 6,94; 9,10] |
0,730 |
|
TIR, % |
85 [ 72,2; 92,8] |
84,4 [ 70,4; 95,8] |
0,727 |
|
TAR L-1, % |
14,1 [ 6,3; 24,6] |
13,8 [ 2,1; 29,5] |
0,620 |
|
TAR L-2, % |
0,3 [ 0; 2,6] |
0 [ 0; 0,75] |
0,045 |
|
TBR L-1, % |
0 [ 0; 0,7] |
0 [ 0; 0,45] |
0,115 |
|
TBR L-2, % |
0 [ 0; 0] |
0 [ 0; 0] |
0,155 |
|
CV, % |
22,8 [ 19,3; 26,7] |
19,4 [ 15,8; 22,6] |
<0,0001 |
|
MAGE, ммоль/л |
3,05 [ 2,40; 3,93] |
2,11 [ 1,68; 2,73] |
<0,0001 |
|
MAG, ммоль/л/ч |
1,45 [ 1,22; 1,78] |
1,32 [ 1,10; 1,55] |
0,017 |
|
LI, (ммоль/л)²/час |
1,94 [ 0,94; 3,17] |
1,02 [ 0,71; 1,55] |
<0,0001 |
Примечания: TIR — время в целевом диапазоне (3,9–10 ммоль/л); TAR — время в диапазоне выше целевого (L-1 10–13,9 ммоль/л; L-2 >13,9 ммоль/л); TBR — время в диапазоне ниже целевого (L-1 3,0–3,9 ммоль/л; L-2 <3,0 ммоль/л); СV — коэффициент вариабельности; MAGE — средняя амплитуда колебаний уровня глюкозы; LI — индекс лабильности; MAG — средняя скорость изменения уровня глюкозы.
Факторы, ассоциированные с возможностью деинтенсификации ББИТ
С целью верификации факторов, обусловливающих возможность деинтенсификации ББИТ, был проведен многофакторный регрессионный анализ. В качестве независимых переменных в модель включали: длительность СД (от момента постановки диагноза), ИМТ, СДИ в абсолютных значениях и пересчитанную на массу тела, уровень HbA1c, а также концентрации С-пептида натощак и после приема пищи. Зависимой переменной являлась деинтенсификация с достижением индивидуальных целевых значений TIR. Наиболее значимыми предикторами успешной деинтенсификации оказались: ИМТ, СДИ и концентрация С-пептида натощак (β=0,0107, p=0,026; β=-0,0039, p=0,036; β=0,1272, p<0,0001 соответственно; R²=0,1443; p<0,0001).
Для определения пороговых значений статистически значимых показателей (ИМТ, СДИ, базальный и стимулированный С-пептид) в контексте перехода на иГларЛикси был выполнен ROC-анализ (рис. 1). Для базального С-пептида площадь под ROC-кривой (AUC) составила 0,70 (95% ДИ 0,65–0,75), что свидетельствует об умеренной дискриминационной способности, точка разделения оказалась равна 0,92 нг/мл (чувствительность — 76%, специфичность — 60%). Для ИМТ и СДИ AUC составила 0,57 (95% ДИ 0,51–0,63) и 0,61 (95% ДИ 0,55–0,66) соответственно, что указывает на меньшую точность данных параметров как предикторов деинтенсификации.
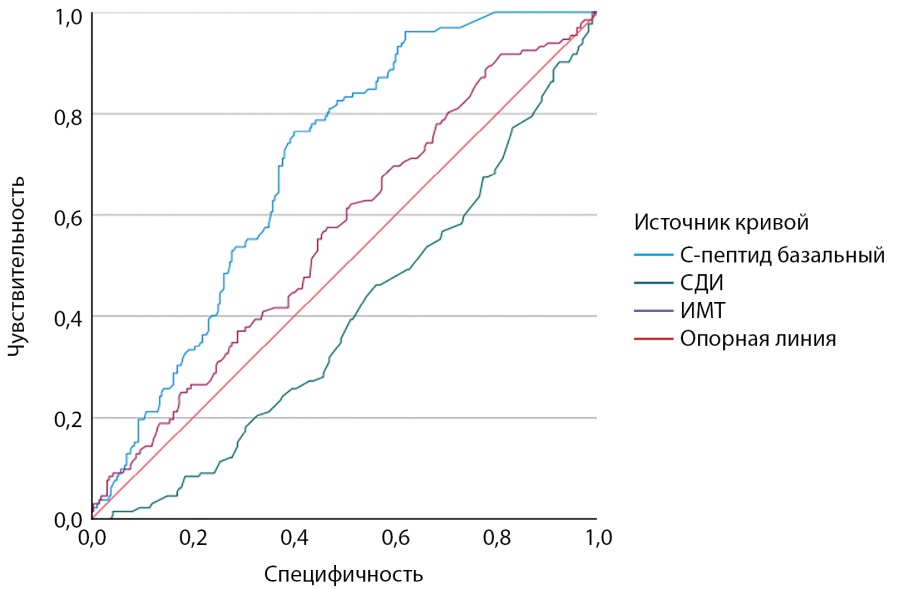
Рисунок 1. Взаимосвязь деинтенсификации базис-болюсной инсулинотерапии с индексом массы тела, суточной дозой инсулина, концентрацией С-пептида натощак у пациентов с сахарным диабетом 2 типа (ROC-анализ).
Примечание: ИМТ — индекс массы тела; СДИ — суточная доза инсулина.
Отдаленные результаты деинтенсификации ББИТ
Отдаленные результаты деинтенсификации лечения представлены в табл. 3. В течение года СДИ иГларЛикси в среднем увеличилась на 4 Ед (0–20 Ед, p=0,003). Двум пациентам потребовалось снижение дозы. При этом средняя СДИ, отнесенная на кг массы тела, снизилась на 0,08 Ед/кг (p<0,0001). Масса тела уменьшилась в среднем на 2 кг (диапазон от 1 до 7 кг, p=0,003). При этом соотношение ОТ/ОБ значимо не изменилось. Уровень HbA1c в среднем снизился на 0,5% от исходного (диапазон от 0 до -3%, p=0,001). Базальный уровень С-пептида увеличился, однако изменение не достигло статистической значимости (р=0,14). При этом уровень постпрандиального С-пептида увеличился значимо, в среднем в 2,5 раза (p=0,029).
Таблица 3. Отдаленные результаты деинтенсификации базис-болюсной инсулинотерапии с переводом на иГларЛикси у больных сахарным диабетом 2 типа
|
Параметр |
Фаза исследования |
Р |
|
|
До деинтенсификации |
Через год после деинтенсификации |
||
|
Масса тела, кг |
86,0 [ 78,0; 99,5] |
85,0 [ 77,5; 92,5] |
0,003 |
|
ОТ/ОБ |
0,99 [ 0,91; 1,05] |
0,99 [ 0,99; 1,04] |
0,387 |
|
HbA1c, % |
8,49 [ 7,69; 9,92] |
8,09 [ 7,33; 8,70] |
0,001 |
|
С-пептид натощак, нг/мл |
0,48 [ 0,26; 1,39] |
0,73 [ 0,37; 1,50] |
0,143 |
|
С-пептид после еды, нг/мл |
1,11 [ 0,47; 2,42] |
2,80 [ 1,29; 5,23] |
0,029 |
|
рСУГ, мг/кг/мин |
3,65 [ 2,65; 4,50] |
3,64 [ 2,81; 4,47] |
0,363 |
Примечания: HbA1c — гликированный гемоглобин А1с; ОТ/ОБ — отношение окружность талии/окружность бедер; рСУГ — расчетная скорость утилизации глюкозы; СДИ — суточная доза инсулина.
Нежелательные явления
У 36 (31%) пациентов, переведенных на фиксированную комбинацию иГларЛикси, наблюдались нежелательные явления в виде тошноты, слабости или головокружения. У двух пациентов зарегистрированы эпизоды рвоты. Указанные симптомы полностью регрессировали в течение трех суток. У одного пациента наблюдалась стойкая гипергликемия более 15 ммоль/л, потребовавшая отмены препарата с повторным назначением ББИТ. У данного пациента зафиксировано низкое значение С-пептида натощак (0,23 нг/мл). В большинстве случаев нежелательные явления не соответствовали критериям тяжелой нежелательной реакции, носили преходящий характер и не требовали отмены препарата.
ОБСУЖДЕНИЕ
Репрезентативность выборок
В исследование включены больные СД2 на ББИТ, проходившие плановое стационарное лечение в специализированном эндокринологическом отделении. Выборка в целом репрезентативна популяции пациентов с СД2 на ББИТ, с учетом некоторых ограничений, обусловленных критериями включения и исключения данного исследования.
Сопоставление с другими публикациями
Одним из современных подходов к деинтенсификации инсулинотерапии при СД2 является замена ББИТ на фиксированную комбинацию базального инсулина с арГПП-1. В нашем исследовании мы оценили эффективность и безопасность деинтенсификации ББИТ у больных СД2 путем перехода на фиксированную комбинацию иГларЛикси во время стационарного лечения. У больных, переведенных на иГЛарЛикси, достигнуты сопоставимые значения TIR (по данным НМГ) и более низкая ВГ (по индексам CV, MAGE, MAG и LI), по сравнению с пациентами, у которых была продолжена ББИТ, при значительном снижении СДИ.
Полученные результаты в целом подтверждают данные литературы. В рандомизированном исследовании BEYOND перевод пациентов с режима многократных инъекций инсулина на одну ежедневную инъекцию иГларЛикси обеспечил сопоставимое снижение уровня HbA1c по сравнению с продолжением ББИТ в течение 6 месяцев, подтвердив возможность упрощения ББИТ без потери эффективности [15]. В рандомизированных исследованиях LixiLan-O и LixiLan-L зафиксировано снижение индексов ВГ (в частности CV, MAGE и MAG), рассчитанных по данным самоконтроля глюкозы крови, у больных СД2 на фоне терапии иГларЛикси [16]. Деинтенсификация терапии сопровождалась рядом клинических преимуществ: существенно снизилось число ежедневных инъекций, количество эпизодов гипогликемии и СДИ [10]. В нашей выборке СДИ в процессе перевода с ББИТ на иГларЛикси снизилась в среднем в 2,13 раза. Заметим, что выраженность первоначального снижения СДИ может уменьшаться с течением времени на фоне титрации дозы иГларЛикси. Однако у большинства наблюдаемых нами пациентов существенного увеличения дозы в течение года после деинтенсификации не потребовалось. В предыдущих исследованиях было продемонстрировано, что в долгосрочной перспективе деинтенсификация ББИТ с использованием иГларЛикси способствует уменьшению уровня HbA1c и ИМТ [10], что согласуется с нашими результатами по оценке отдаленных результатов деинтенсификации. Таким образом, упрощение инсулинотерапии с помощью перехода на фиксированную комбинацию иГларЛикси позволяет поддерживать эффективный гликемический контроль, снижая инъекционную нагрузку, потребность в инсулине и риски, присущие интенсивному режиму лечения.
Практически важным вопросом является выявление пациентов, у которых возможна деинтенсификация ББИТ. Согласно недавно предложенному алгоритму, каждого пациента необходимо оценивать с точки зрения наличия факторов, предрасполагающих к деинтенсификации лечения [17]. В нашем исследовании основаниями для деинтенсификации являлись эпизоды гипогликемии, в том числе на фоне ее нарушенного распознавания, неадекватно низкий уровень HbA1c, прибавка массы тела, низкая приверженность рекомендациям, принадлежность пациента к категории высокого риска (например, тяжелая сердечно-сосудистая патология), а также улучшение состояния после острого сопутствующего заболевания, требовавшего временной интенсификации терапии. При этом мы оценили ряд клинических и лабораторных параметров как возможных предикторов успешной деинтенсификации ББИТ. В многофакторном регрессионном анализе такими предикторами оказались СДИ, ИМТ и концентрация С-пептида натощак. В дополнительном ROC-анализе наиболее значимым предиктором был С-пептид, в то время как ИМТ и СДИ оказались менее надежными индикаторами.
Ранее было продемонстрировано, что деинтенсификация ББИТ может быть успешно проведена у больных СД2 с различным ИМТ. При этом у пациентов с ожирением на фоне отмены болюсного инсулина и добавления арГПП-1 обычно достигается существенное снижение массы тела [18][19]. Возможно, снижение массы тела после деинтенсификации инсулинотерапии сопровождается улучшением чувствительности к инсулину. В данном исследовании мы не смогли подтвердить это предположение, поскольку величина рСУГ, косвенно отражающая чувствительность к инсулину, практически не изменилась через год после деинтенсификации. Соотношение ОТ/ОБ также значимо не изменилось, что указывает на стабильность абдоминального распределения жировой ткани и снижения чувствительности к инсулину. По нашим данным, СДИ сама по себе не позволяет надежно идентифицировать пациентов, нуждающихся в деинтенсификации, что может объясняться различной чувствительностью к инсулину у разных больных.
Наиболее значимым предиктором успешной деинтенсификации ББИТ оказался уровень С-пептида с «точкой разделения» 0,92 нг/мл. Известно, что секреция инсулина — значимый предиктор достижения TIR у пациентов с СД2 [20]. Данные о важности использования концентрации С-пептида как маркера успешной деинтенсификации инсулинотерапии получены нами впервые. Кроме того, нами показано повышение постпрандиального уровня С-пептида через год после перевода на иГларЛикси, что можно объяснить влиянием ликсисенатида.
Клиническая значимость результатов
Полученные данные свидетельствуют, что проведенная по клиническим показаниям деинтенсификация ББИТ у больных СД2 с переводом на фиксированную комбинацию иГларЛикси позволяет оптимизировать качество гликемического контроля без повышения риска гипогликемии или гипергликемии при существенном сокращении СДИ и снижении массы тела в перспективе. При определении возможности деинтенсификации ББИТ следует учитывать уровень С-пептида. Предиктором успешной деинтенсификации является концентрация С-пептида в состоянии натощак ≥0,92 нг/мл. Длительность инсулинотерапии, ИМТ и СДИ не должны применяться изолированно как предикторы успеха деинтенсификации.
Ограничения исследования
Очевидными ограничениями нашего исследования является набор пациентов в одном клиническом центре, короткая длительность наблюдения и небольшое количество участников, у которых прослежены отдаленные результаты. Длительность НМГ была меньше рекомендованной [21], что связано с ограниченными сроками стационарного лечения. Исследование выполнено в условиях реальной клинической практики, поэтому деинтенсификация лечения проводилась по клиническим показаниям, а не на основе рандомизации. Это могло привести к более позитивным результатам лечения в группе деинтенсификации.
Направления дальнейших исследований
Результаты работы могут являться обоснованием для дальнейших проспективных исследований большей мощности, направленных на оценку эффективности и выявление предикторов успешной деинтенсификации инсулинотерапии у больных СД2.
ЗАКЛЮЧЕНИЕ
Деинтенсификация ББИТ у больных СД2, проведенная по клиническим показаниям, с переходом на фиксированную комбинацию базального инсулина и арГПП-1 (иГларЛикси) позволяет существенно снизить СДИ и достичь сопоставимых значений TIR при более низкой ВГ (по индексам СV, MAGE, LI, MAG) без увеличения риска гипо- и гипергликемии в сравнении с коррекцией ББИТ во время стационарного лечения. Отдаленные (через год) результаты деинтенсификации включают улучшение качества гликемического контроля (снижение уровня HbA1c), уменьшение массы тела и повышение постпрандиальной эндогенной секреции инсулина. Таким образом, переход на иГларЛикси может являться эффективной терапевтической стратегией у пациентов с СД2, нуждающихся в деинтенсификации ББИТ. Сохранная эндогенная секреция инсулина является условием для успешной деинтенсификации ББИТ у больных СД2.
ДОПОЛНИТЕЛЬНАЯ ИНФОРМАЦИЯ
Источники финансирования. Исследование выполнено за счет средств государственного задания НИИКЭЛ — филиал ИЦиГ СО РАН.
Конфликт интересов. Авторы декларируют отсутствие явных и потенциальных конфликтов интересов, связанных с содержанием настоящей статьи.
Участие авторов. Климонтов В.В. — концепция и дизайн исследования, интерпретация результатов, написание статьи; Яковлева С.А. — сбор данных, статистический анализ, интерпретация результатов, написание статьи; Королева Е.А. — сбор данных, внесение в рукопись существенной правки; Раисинежад К. — сбор и анализ данных, внесение в рукопись существенной правки; Булумбаева Д.М. — сбор данных, внесение в рукопись существенной правки; Мавлянова К.Р. — сбор данных, внесение в рукопись существенной правки. Все авторы одобрили финальную версию статьи перед публикацией, выразили согласие нести ответственность за все аспекты работы, подразумевающую надлежащее изучение и решение вопросов, связанных с точностью или добросовестностью любой части работы.
Список литературы
1. American Diabetes Association Professional Practice Committee. 9. Pharmacologic Approaches to Glycemic Treatment: Standards of Care in Diabetes—2025. Diabetes Care. 2024;48(Suppl.1):S181-S206. doi:10.2337/dc25-S009
2. Климонтов ВВ, Циберкин АИ, Фазуллина ОН, Прудникова МА, Тян НВ, Коненков ВИ. Гипогликемии у пожилых больных сахарным диабетом 2 типа, получающих инсулин: результаты непрерывного мониторирования глюкозы. Сахарный Диабет. 2014;17(1):75-80. doi:10.14341/DM2014175-80
3. Mattishent K, Loke YK. Meta-Analysis: Association Between Hypoglycemia and Serious Adverse Events in Older Patients Treated With Glucose-Lowering Agents. Front Endocrinol. 2021;12:571568. doi:10.3389/fendo.2021.571568
4. Дедов ИИ, Шестакова МВ, Майоров АЮ, et al. Алгоритмы специализированной медицинской помощи больным сахарным диабетом / Под редакцией И.И. Дедова, М.В. Шестаковой, А.Ю. Майорова. 11-й выпуск. Сахарный Диабет. 2023;26(2S):1-157. doi:10.14341/DM13042-10287
5. Frias JP. What is the 'real-world' experience with fixed-ratio combination therapy (insulin + GLP-1 receptor agonist) in routine clinical practice? Take-home messages for clinicians regarding key outcomes. Diabetes Obes Metab. 2025; in press. doi: 10.1111/dom.16593.
6. FLAT-SUGAR Trial Investigators. Glucose Variability in a 26-Week Randomized Comparison of Mealtime Treatment With Rapid-Acting Insulin Versus GLP-1 Agonist in Participants With Type 2 Diabetes at High Cardiovascular Risk. Diabetes Care. 2016;39(6):973-981. doi:10.2337/dc15-2782
7. Martinez M, Santamarina J, Pavesi A, Musso C, Umpierrez GE. Glycemic variability and cardiovascular disease in patients with type 2 diabetes. BMJ Open Diabetes Res Care. 2021;9(1):e002032. doi:10.1136/bmjdrc-2020-002032
8. Klimontov VV, Saik OV, Korbut AI. Glucose Variability: How Does It Work? Int J Mol Sci. 2021;22(15):7783. doi: 10.3390/ijms22157783
9. Liu Y, Li C, Li X, Yang J, Zheng Y, Li F, Wang X. iGlarLixi for type 2 diabetes: a systematic review and meta-analysis. Endocrine. 2024;86(1):135-142. doi: 10.1007/s12020-024-03868-3
10. Novodvorský P, Thieme L, Laňková I, et al. The IDEAL (Insulin therapy DE-intensificAtion with iglarLixi) Randomised Controlled Trial-Study Design and Protocol. Diabetes Ther Res Treat Educ Diabetes Relat Disord. 2024;15(6):1461-1471. doi:10.1007/s13300-024-01582-x
11. Clarke WL, Cox DJ, Gonder-Frederick LA, Julian D, Schlundt D, Polonsky W. Reduced awareness of hypoglycemia in adults with IDDM. A prospective study of hypoglycemic frequency and associated symptoms. Diabetes Care. 1995;18(4):517-522. doi:10.2337/diacare.18.4.517
12. Zhang Z, Zhao L, Lu Y, Xiao Y, Zhou X. Insulin resistance assessed by estimated glucose disposal rate and risk of incident cardiovascular diseases among individuals without diabetes: findings from a nationwide, population based, prospective cohort study. Cardiovasc Diabetol. 2024;23(1):194. doi:10.1186/s12933-024-02256-5
13. Battelino T, Danne T, Bergenstal RM, et al. Clinical Targets for Continuous Glucose Monitoring Data Interpretation: Recommendations From the International Consensus on Time in Range. Diabetes Care. 2019;42(8):1593-1603. doi:10.2337/dci19-0028
14. Kovatchev B. Glycemic Variability: Risk Factors, Assessment, and Control. J Diabetes Sci Technol. 2019;13(4):627-635. doi: 10.1177/1932296819826111
15. Giugliano D, Longo M, Caruso P, et al. Feasibility of Simplification From a Basal-Bolus Insulin Regimen to a Fixed-Ratio Formulation of Basal Insulin Plus a GLP-1RA or to Basal Insulin Plus an SGLT2 Inhibitor: BEYOND, a Randomized, Pragmatic Trial. Diabetes Care. 2021;44(6):1353-1360. doi:10.2337/dc20-2623
16. Aronson R, Umpierrez G, Stager W, Kovatchev B. Insulin glargine/lixisenatide fixed-ratio combination improves glycaemic variability and control without increasing hypoglycaemia. Diabetes Obes Metab. 2019;21(3):726-731. doi:10.1111/dom.13580
17. Munshi M, Kahkoska AR, Neumiller JJ, et al. Realigning diabetes regimens in older adults: a 4S Pathway to guide simplification and deprescribing strategies. Lancet Diabetes Endocrinol. 2025;13(5):427-437. doi:10.1016/S2213-8587(24)00372-3
18. Fejes R, Kádár C, Kovács-Huber R, et al. Efficacy of Simplifying Complex Insulin Regimen on Glycometabolic Parameters and Target Organ Damage in Type 2 Diabetes: A Retrospective Cohort Study. J Diabetes Res. 2025;2025:9141564. doi:10.1155/jdr/9141564
19. Bruinstroop E, Meyer L, Brouwer CB, van Rooijen DE, van Dam PS. Retrospective Analysis of an Insulin-to-Liraglutide Switch in Patients with Type 2 Diabetes Mellitus. Diabetes Ther Res Treat Educ Diabetes Relat Disord. 2018;9(3):1369-1375. doi:10.1007/s13300-018-0438-9
20. Kawaguchi Y, Hajika Y, Rinka M, et al. Comparison of efficacy and safety of insulin degludec/liraglutide and insulin glargine U-100/lixisenatide in individuals with type 2 diabetes mellitus using professional continuous glucose monitoring. J Diabetes Investig. 2024;15(5):598-607. doi:10.1111/jdi.14151
21. Danne T, Nimri R, Battelino T, et al. International Consensus on Use of Continuous Glucose Monitoring. Diabetes Care. 2017;40(12):1631-1640. doi:10.2337/dc17-1600
Об авторах
В. В. КлимонтовРоссия
Климонтов Вадим Валерьевич, д.м.н., профессор РАН
630090, Новосибирск, ул. Арбузова, д. 6
Researcher ID: R-7689-2017
Scopus Author ID: 8295977000
Конфликт интересов:
Авторы декларируют отсутствие явных и потенциальных конфликтов интересов, связанных с содержанием настоящей статьи.
С. А. Яковлева
Россия
Яковлева Софья Александровна
Новосибирск
Researcher ID: JVZ-0405-2024
Scopus Author ID: 57405397600
Конфликт интересов:
Авторы декларируют отсутствие явных и потенциальных конфликтов интересов, связанных с содержанием настоящей статьи.
Е. А. Королева
Россия
Королева Елена Анатольевна, к.м.н.
Новосибирск
Researcher ID: S-1384-2017
Scopus Author ID: 55522435000
Конфликт интересов:
Авторы декларируют отсутствие явных и потенциальных конфликтов интересов, связанных с содержанием настоящей статьи.
Д. М. Булумбаева
Россия
Булумбаева Динара Мухтаровна, к.м.н.
Новосибирск
Researcher ID: R-7904-2017
Scopus Author ID: 57195304317
Конфликт интересов:
Авторы декларируют отсутствие явных и потенциальных конфликтов интересов, связанных с содержанием настоящей статьи.
К. Р. Мавлянова
Россия
Мавлянова Камилла Рустамалиевна
Новосибирск
Конфликт интересов:
Авторы декларируют отсутствие явных и потенциальных конфликтов интересов, связанных с содержанием настоящей статьи.
К. Раисинежад
Россия
Раисинежад Карса
Новосибирск
Конфликт интересов:
Авторы декларируют отсутствие явных и потенциальных конфликтов интересов, связанных с содержанием настоящей статьи.
Дополнительные файлы
|
|
1. Рисунок 1. Взаимосвязь деинтенсификации базис-болюсной инсулинотерапии с индексом массы тела, суточной дозой инсулина, концентрацией С-пептида натощак у пациентов с сахарным диабетом 2 типа (ROC-анализ). | |
| Тема | ||
| Тип | Исследовательские инструменты | |
Посмотреть
(277KB)
|
Метаданные ▾ | |
Рецензия
Для цитирования:
Климонтов В.В., Яковлева С.А., Королева Е.А., Булумбаева Д.М., Мавлянова К.Р., Раисинежад К. Деинтенсификация базис-болюсной инсулинотерапии путем перевода на фиксированную комбинацию инсулин гларгин. Сахарный диабет. 2025;28(5):424-432. https://doi.org/10.14341/DM13381
For citation:
Klimontov V.V., Yakovleva S.A., Koroleva E.A., Bulumbaeva D.M., Mavlianova K.R., Raisinezhad K. Deintensification of basal-bolus insulin therapy by switching to a fixed-ratio combination of insulin glargine and lixisenatide in patients with type 2 diabetes. Diabetes mellitus. 2025;28(5):424-432. (In Russ.) https://doi.org/10.14341/DM13381

Контент доступен под лицензией Creative Commons Attribution-NonCommercial-NoDerivatives 4.0 International License (CC BY-NC-ND 4.0).















































