Перейти к:
Диагностика артифициальной гипогликемии вследствие приема пероральных сахароснижающих препаратов методом высокоэффективной жидкостной хроматографии с тандемным масс-спектрометрическим детектированием
https://doi.org/10.14341/DM13119
Аннотация
ВВЕДЕНИЕ. Артифициальная гипогликемия (АрГ) — это снижение уровня глюкозы крови менее 3 ммоль/л вследствие умышленного применения сахароснижающих препаратов пациентом вне врачебных назначений. Своевременная диагностика такого рода гипогликемий позволяет избежать излишних многочисленных обследований и госпитализаций. Однако выявление АрГ до сих пор остается крайне сложной задачей как для медицинского учреждения, так и для лечащего врача. В зарубежной литературе описаны случаи успешного выявления преднамеренного приема пероральных сахароснижающих препаратов (ПССП) с помощью высокоэффективной жидкостной хроматографии с тандемным масс-спектрометрическим детектированием (ВЭЖХ-МС/МС). Таким образом, актуальна разработка и валидация метода определения ПССП с помощью ВЭЖХ-МС/МС.
ЦЕЛЬ ИССЛЕДОВАНИЯ. Оптимизация диагностики АрГ вследствие приема ПССП.
МАТЕРИАЛЫ И МЕТОДЫ. Всего обследовано 92 пациента. Разработка метода ВЭЖХ-МС/МС для обнаружения исследуемых ПССП (иПССП) (n=1-глибенкламид, n=1-гликвидон, n=1-гликлазид, n=1-глимепирид, n=1-глипизид, n=1-натеглинид и n=1-репаглинид) в крови осуществлена на группе пациентов с сахарным диабетом 2 типа (n=7), которые получали иПССП, и группе условно здоровых, не получавших никакие лекарственные препараты (n=7). Для валидации метода определение субстанций иПССП осуществлено на группах пациентов с гиперинсулинемической недиабетической гипогликемией (НДГ) неясного генеза (n=11) и с инсулиномой (n=67).
РЕЗУЛЬТАТЫ. При исследовании образцов крови методом ВЭЖХ-МС/МС в группе пациентов с сахарным диабетом 2 типа в 100% случаев подтвержден прием препарата, который получал больной, в группе условно здоровых — иПССП не выявлены. Ложноположительный результат не получен ни у условно здоровых и ни у одного пациента с инсулиномой. У 5 из 11 пациентов группы с гиперинсулинемической НДГ неясного генеза диагностирована АрГ, метод идентифицировал иПССП глибенкламид и гликлазид в образцах крови пациентов. У остальных 6 пациентов этой группы были продолжены обследования и диагностированы другие причины НДГ. Чувствительность метода составила 100% [74%; 100%], специфичность — 100% [95%; 100%].
ЗАКЛЮЧЕНИЕ. Метод ВЭЖХ-МС/МС обладает высокой диагностической точностью в обнаружении и идентификации иПССП (глибенкламид, гликвидон, гликлазид, глимепирид, глипизид, натеглинид и репаглинид) в образцах крови пациентов, получающих данные лекарственные препараты. В настоящее время в силу малой доступности метода данное исследование целесообразно применять у пациентов с гиперинсулинемической гипогликемией при отрицательных результатах методов визуализации инсулиномы первого ряда (компьютерная томография с контрастированием, ультразвуковое исследование и магнитно-резонансная томография органов брюшной полости).
Ключевые слова
Для цитирования:
Юкина М.Ю., Трошина Е.А., Нуралиева Н.Ф., Иоутси В.А., Реброва О.Ю., Мельниченко Г.А., Мокрышева Н.Г. Диагностика артифициальной гипогликемии вследствие приема пероральных сахароснижающих препаратов методом высокоэффективной жидкостной хроматографии с тандемным масс-спектрометрическим детектированием. Сахарный диабет. 2024;27(1):50-58. https://doi.org/10.14341/DM13119
For citation:
Yukina M.Y., Troshina E.A., Nuralieva N.F., Ioutsi V.A., Rebrova O.Y., Mel’nichenko G.A., Mokrysheva N.G. Diagnosis of artificial hypoglycemia due to oral hypoglycemic drugs by high-performance liquid chromatography with tandem mass spectrometric detection. Diabetes mellitus. 2024;27(1):50-58. (In Russ.) https://doi.org/10.14341/DM13119
АКТУАЛЬНОСТЬ
Синдром Мюнхгаузена (СМ) — это собирательный термин, объединяющий артифициальные заболевания («артифициальный» — artificial — искусственный, рукотворный, ненастоящий). При СМ человек умышленно производит или симулирует физические/психические признаки и симптомы определенной патологии с целью признания окружающими его больным без каких-либо внешних стимулов для подобного поведения [1].
Артифициальный гипогликемический синдром или артифициальная гипогликемия (АрГ) является одним из самых известных «искусственных заболеваний» [2] и представляет собой преднамеренное применение препаратов инсулина или пероральных сахароснижающих препаратов (ПССП) с целью снижения уровня глюкозы крови [3]. Данное состояние описано как у лиц без нарушений углеводного обмена, так и у пациентов с сахарным диабетом (СД) [2][4][5]; нередко встречается у работников в сфере здравоохранения [4], а также у пациентов, родственники которых страдают СД. Часто имеют место коморбидные психиатрические заболевания и социально-психологические проблемы [4][6][7][8]. Для артифициальных патологий характерны неадекватные изменения симптомов и течения заболевания, в том числе во время лечения, многократные госпитализации и наблюдение у различных специалистов. Нередко наступает необъяснимая длительная «ремиссия» эпизодов гипогликемии с последующим их возобновлением [9]. Важно отметить, что больные с СМ могут предоставить подделанные результаты лабораторных исследований или иную медицинскую документацию [6].
Как правило, пациенты с АрГ отрицают экзогенное введение сахароснижающих препаратов, не признают данный факт и после предоставления им «доказательств» (например, результатов лабораторных анализов) [2]. Своевременная диагностика СМ — это в первую очередь возможность обсудить с пациентом ситуацию, рассказать о вероятности необратимого повреждения здоровья, а также летального исхода. Кроме того, при установлении факта «искусственного заболевания» нет необходимости в проведении разнообразных диагностических мероприятий с целью поиска причин снижения гликемии, которые зачастую включают в себя инвазивные и дорогостоящие, в том числе оперативные вмешательства. При ведении таких больных требуется мультидисциплинарный подход с обязательным участием психиатра [3][6][7][8].
Диагностика АрГ сложна, так как лабораторные признаки схожи с другими заболеваниями, ассоциированными с недиабетической гипогликемией (НДГ), например, с инсулиномой. Только при абсолютном круглосуточном наблюдении за пациентом и исключении использования личных вещей удавалось подтвердить АрГ. Но такие мероприятия должны проводиться при согласии пациента, которое он обычно не дает, а также при наличии возможностей стационара обеспечить круглосуточный пост. В итоге до недавнего времени пациенты с АрГ в России в большинстве случаев оставались с неуточненным диагнозом. При этом, по данным зарубежной литературы, описаны случаи успешного выявления преднамеренного приема ПССП с помощью высокоэффективной жидкостной хроматографии с тандемным масс-спектрометрическим детектированием (ВЭЖХ-МС/МС) [10].
ЦЕЛЬ ИССЛЕДОВАНИЯ
Учитывая актуальность проблемы, целью настоящего исследования является оптимизация диагностики АрГ вследствие приема ПССП с помощью ВЭЖХ-МС/МС.
МАТЕРИАЛЫ И МЕТОДЫ
Место и время проведения исследования
ГНЦ РФ ФГБУ «НМИЦ эндокринологии» МЗ РФ, 2017–2022 гг.
Изучаемая популяция
Пациенты, проходившие обследование в ГНЦ РФ ФГБУ «НМИЦ эндокринологии» МЗ РФ.
Критериями включения для всех групп являлись: мужской или женский пол; возраст — 18 лет и старше. Критериев исключения не было.
Дизайн исследования
Одноцентровое, экспериментальное.
Методы
Работа состояла из двух этапов, на каждом из которых формировались пары групп пациентов.
Этап 1: разработка метода ВЭЖХ-МС/МС для обнаружения иПССП в крови в группе пациентов с СД 2 типа (СД2), которые получали исследуемые ПССП (иПССП), и в группе условно здоровых пациентов.
Порядок выполнения исследования представлен на рисунке 1.
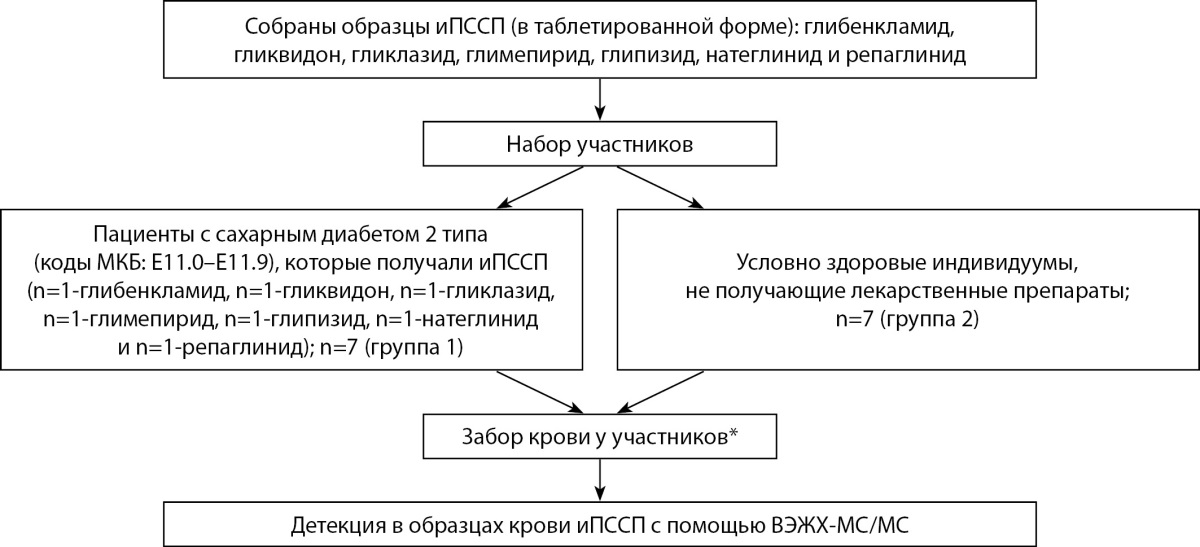
Рисунок 1. Порядок выполнения исследования на этапе 1.
Примечание. иПССП — исследуемые пероральные сахароснижающие препараты;
ВЭЖХ-МС/МС — высокоэффективная жидкостная хроматография
с тандемным масс-спектрометрическим детектированием;
* в группе 1 забор образца крови производился утром натощак
через 1 час после приема препарата, в группе 2 — утром натощак.
Время забора крови через 1 час после приема иПССП у пациентов группы 1 было выбрано с учетом времени, при котором любой лекарственный препарат, принятый внутрь, уже начал всасываться в ЖКТ и поступать в кровоток [11][12][13][14][15][16]. Минимальное количество препарата достаточно для его определения методом ВЭЖХ-МС/МС с учетом его высокой чувствительности — порядка 10 пг/мл по каждому компоненту, что позволяет выявить следы препарата даже спустя неделю после приема.
Этап 2: валидация метода детектирования иПССП с помощью ВЭЖХ-МС/МС в группе пациентов с гиперинсулинемической НДГ.
Порядок выполнения исследования на этапе 2 представлен на рисунке 2.

Рисунок 2. Порядок выполнения исследования на этапе 2.
Примечание. иПССП — исследуемые пероральные сахароснижающие препараты;
ВЭЖХ-МС/МС — высокоэффективная жидкостная хроматография
с тандемным масс-спектрометрическим детектированием;
КТ — компьютерная томография; МРТ — магнитно-резонансная томография;
УЗИ —ультразвуковое исследование.
* Манифестная гипогликемия констатировалась при условии достижения
уровня глюкозы в венозной крови менее 3 ммоль/л;
гиперинсулинемический вариант гипогликемии —
при уровне С-пептида ≥0,6 нг/мл, а инсулина ≥3 мкМЕ/мл;
гипоинсулинемический вариант —
при уровне С-пептида <0,6 нг/мл, а инсулина <3 мкМЕ/мл [10].
Забор крови производился на фоне манифестной гипогликемии
в ходе пробы с голоданием или при спонтанной гипогликемии.
Образцы сыворотки пациентов с гиперинсулинемической гипогликемией
направлялись в работу для выявления иПССП.
Не дожидаясь результатов данного анализа,
пациентам проводилось стандартное визуализирующее обследование.
Лабораторные исследования
Биохимические и гормональные исследования проводились в клинико-диагностической лаборатории ГНЦ РФ ФГБУ «НМИЦ эндокринологии» Минздрава России. Забор крови производился в вакуумные пробирки с инертным гелем. Полученные пробы центрифугировались не позднее чем через 15 мин после забора с использованием центрифуги Eppendorf 5810R при температуре 4 °С на скорости 3000 оборотов в минуту в течение 15 минут и затем поступали в работу. Исследование инсулина, С-пептида осуществлялось методом усиленной хемилюминесценции на анализаторе COBAS 6000 (Roche Diagnostics, Швейцария). Биохимическое исследование крови выполнялось на анализаторе Architect plus C 4000 (Abbott Diagnostics, США).
Выявление иПССП (глибенкламида, гликвидона, гликлазида, глимепирида, глипизида, натеглинида и репаглинида) в образце крови пациента осуществлялось методом ВЭЖХ-МС/МС. Для этого использовали жидкостный хроматограф Agilent 1290 Infinity II (Agilent Technologies, Германия), оснащенный четырехканальным насосом, автосемплером и термостатом колонок, и гибридный трехквадрупольный масс-спектрометр AB Sciex QTrap 5500 (AB Sciex, Сингапур), способный работать в режиме линейной ионной ловушки.
Образцы сыворотки крови готовили методом жидкостной экстракции с высаливанием (SALLE). Для этого к 200 мкл сыворотки добавляли 400 мкл ацетонитрила, перемешивали смесь в шейкере в течение 10 мин., а затем центрифугировали 1 мин. при 14 800 об/мин при 5 ºС. К полученному раствору добавляли 200 мкл 5М ацетата аммония (Fluka, >99%, Нидерланды), перемешивали 3 мин. в шейкере и центрифугировали 2 мин. при 14 800 об/мин и 5 ºС. После этого отбирали 50 мкл верхнего органического слоя, помещали в 96-луночный планшет, добавляли 50 мкл деионизированной воды и перемешивали пипетированием. В таком виде раствор использовали для хромато-масс-спектрометрического анализа.
Хроматографическое разделения компонентов проводили на колонке Accucore PFP 2,1х50 мм, 2,6 мкм диаметр частиц (Thermo Scientific, США). В качестве элюентов были применены ацетонитрил (Honeywell, for LC-MS, Германия) и деионизированная вода (MilliQ Advantage A10, Millipore, Германия). Разделение проводили в градиентном режиме с градиентом органической фазы от 5 до 60% с 1 по 6 мин., с изократическим участком с 6 по 7 мин. на 60% ацетонитрила и возврат на исходные 5% с 7 по 8 мин. с последующим уравновешиванием колонки до 11 мин. Поток элюента составлял 0,4 мл/мин., температура колонки — 20 ºС, объем ввода образца — 20 мкл.
Масс-спектрометрическое детектирование проводили в режиме мониторинга множественных реакций (MRM), совмещенного с информационно-зависимым мониторингом (IDA), который был реализован на линейной ионной ловушке. Для ионизации использовали источник химической ионизации при атмосферном давлении (APCI) в режиме положительных ионов. MRM-переходы подбирали для каждого компонента индивидуально путем ввода стандартного образца в хроматографическом потоке непосредственно в источник ионизации и последовательного варьирования параметров фрагментации. Для каждого компонента регистрировали по два MRM-перехода.
Критериями идентичности субстанции из образца пациента с субстанцией в образце контроля считается совпадение времен удерживания в пределах 0,2 мин., соотношение площадей под хроматографическими пиками по двум MRM-переходам для определяемой субстанции, а также совпадение спектров фрагментных ионов для компонента образца и контроля.
Управление анализом, сбор и обработку данных проводили с использованием программного пакета Analyst 1.6.3 (AB Sciex, Канада).
Статистический анализ
Статистическая обработка полученных результатов проводилась с помощью стандартных методов статистического анализа с использованием программного обеспечения: STATISTICA v. 13 (TIBCO Inc., США). Для количественных признаков указаны медиана и интерквартильный интервал, а также в некоторых случаях минимальное и максимальное значения. С целью сравнения количественных данных двух независимых выборок применялся критерий Манна-Уитни. Критический уровень статистической значимости при проверке статистических гипотез был принят равным 0,05. Для коррекции проблемы множественных сравнений применялась поправка Бонферрони. После применения поправки значения Р в диапазоне между рассчитанным и 0,05 интерпретировались как статистическая тенденция.
Этическая экспертиза
Исследование одобрено локальным этическим комитетом ФГБУ «НМИЦ эндокринологии» МЗ РФ (протокол №1 от 27.01.2016 г.). Все пациенты подписали информированное согласие для участия в исследовании.
РЕЗУЛЬТАТЫ
Этап 1. В группы 1 и 2 включено по 7 последовательных пациентов. Возраст пациентов группы 1 составил 59 [ 54; 67] лет, группы 2 — 45 [ 41; 51] лет. В каждую группу включено по 4 женщины и 3 мужчины.
При исследовании образцов крови пациентов группы 1 методом ВЭЖХ-МС/МС в 100% случаев подтвержден прием препарата, который получал больной: n=1-глибенкламид, n=1-гликвидон, n=1-гликлазид, n=1-глимепирид, n=1-глипизид, n=1-натеглинид и n=1-репаглинид. При исследовании образцов крови группы 2 методом ВЭЖХ-МС/МС иПССП не выявлены.
Этап 2. Забор крови на фоне манифестной гипогликемии выполнен 116 пациентам, из них у 38 выявлена гипоинсулинемическая гипогликемия, и эти пациенты были исключены из дальнейшего исследования. У оставшихся 78 пациентов было выполнено визуализирующее обследование с целью поиска инсулин-продуцирующей опухоли: компьютерная томография (КТ) с контрастным усилением и/или МРТ — магнитно-резонансная томография (МРТ) и/или ультразвуковое исследование (УЗИ) органов брюшной полости. У 11 пациентов диагностирована гипогликемия неясного генеза (группа 3), а у 67 пациентов — инсулинома (группа 4).
Возраст пациентов группы 3 составил 43 [ 35; 56] года, группы 4 — 51 [ 34; 62] год. В группу 3 включено 9 женщин и 2 мужчин, в группу 4 — 52 женщины и 15 мужчин.
Ложноположительный результат не получен ни у одного пациента из группы 4. Метод идентифицировал иПССП (глибенкламид и гликлазид) в образцах крови 5 из 11 пациентов группы 3 (подгруппа 3а). Хроматограммы двух из таких пациентов представлены на рисунках 3 и 4.
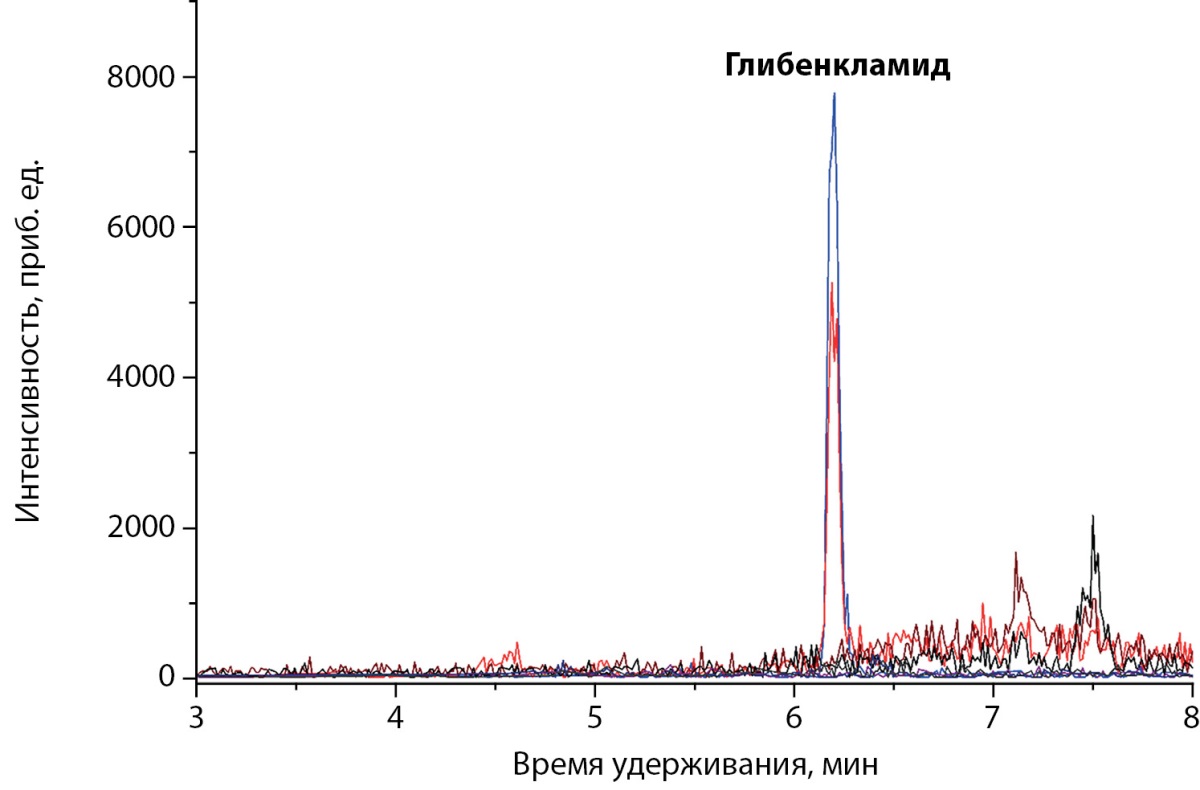
Рисунок 3. Хроматограмма образца крови
пациента с артифициальной гипогликемией вследствие приема глибенкламида [17].
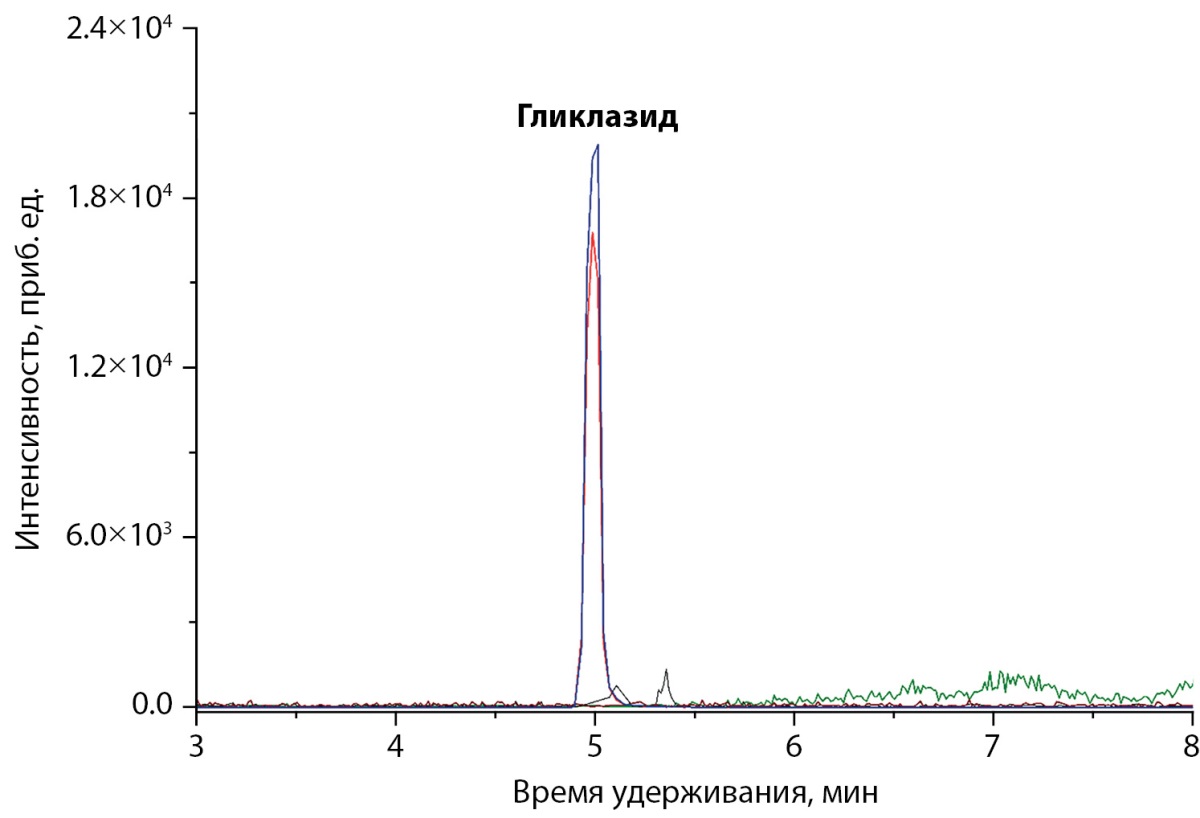
Рисунок 4. Хроматограмма образца крови
пациента с артифициальной гипогликемией вследствие приема гликлазида.
У 6 пациентов группы 3, у которых не выявлены иПССП (подгруппа 3б), продолжены обследования и диагностированы следующие причины НДГ: инсулинома (всего n=4; с помощью сцинтиграфии с ОФЭКТ/КТ с 99mTc-Тектротидом (n=3) и эндоскопического УЗИ (n=1)), врожденный гиперинсулинизм вследствие мутации в гене ABCC8 (n=1) и неинсулиномная панкреатогенная гипогликемия (n=1; подтверждена по результатам артериально-стимулированного венозного забора крови).
Таким образом, у пациентов групп 1 (n=7) и 3а (n=5) в крови обнаружены препараты иПССП, у пациентов групп 2 (n=7), 4 (n=67) и 3б (n=6) — не обнаружены. Для расчета операционных характеристик метода ВЭЖХ-МС/МС в выявлении иПССП составлена таблица кросс-табуляции частот в объединенных группах: пациенты с СД2, получающие иПССП, и пациенты с НДГ, у которых инсулинома исключена стандартными методами (n=12); пациенты с уточненными причинами НДГ и здоровые (n=80) (таблица 1). Чувствительность метода составила 100%, 95% ДИ (74%; 100%), специфичность — 100%, 95% ДИ (95%; 100%).
Таблица 1. Кросс-табуляция частот для расчета операционных характеристик
высокоэффективной жидкостной хроматографии с тандемной масс-спектрометрией
в выявлении исследуемых пероральных сахароснижающих препаратов
|
Результат ВЭЖХ-МС/МС |
Группы 1+3a n=12 |
Группы 2+4+3б n=80 |
|
Минимум один иПССП обнаружен |
12 (ИП) |
0 (ЛП) |
|
иПССП не обнаружены |
0 (ЛО) |
80 (ИО) |
Примечание. иПССП — исследуемые пероральные сахароснижающие препараты;
ВЭЖХ-МС/МС — высокоэффективная жидкостная хроматография
с тандемным масс-спектрометрическим детектированием;
ИП — истинноположительный результат; ЛП — ложноположительный результат;
ЛО — ложноотрицательный результат; ИО — истинноотрицательный результат.
С целью выявления дополнительных серологических маркеров АрГ вследствие приема иПССП, которые помогли бы дифференцировать это состояние от лабораторных показателей при инсулиноме, проведен сравнительный анализ показателей инсулина, глюкозы и С-пептида на фоне манифестной гипогликемии в группе 3а (n=5) и в объединенной группе пациентов с инсулиномой (группа 2, n=67) и другими причинами неартифициальной гиперинсулинемической НДГ (группа 3б; n=6). Уровень инсулина в группе 3а был статистически значимо ниже, чем в группе 2+3б, в то время как уровни глюкозы и С-пептида не различались (таблица 2).
Таблица 2. Показатели глюкозы, инсулина и С-пептида на фоне манифестной гипогликемии
в группах 3а и 2+3б (Me [Q1; Q3], (min, max))
|
Группа 3а, n=5 |
Группы 2+3б, n=73 |
Р*, U-тест |
|
|
Глюкоза, ммоль/л |
2,18 [ 2,13; 2,61], (2,00, 2,72) |
2,16 [ 1,66; 2,41], (0,41, 2,90) |
0,289 |
|
Инсулин, мкЕ/мл |
8,99 [ 6,05; 16,20], (5,91, 21,39) |
24,13 [ 16,00; 35,00], (4,09, 387,30) |
0,009 |
|
С-пептид, нг/мл |
2,30 [ 1,33; 3,15], (1,03, 23,91) |
4,00 [ 2,79; 5,52], (0,67, 40,00) |
0,153 |
*Пороговый Р0=0,05:3≈0,017.
При анализе уровня инсулина на фоне манифестной гипогликемии в группе 3а обращало на себя внимание значительное повышение гормона у пациентов №2 и №3 по сравнению с другими больными (табл. 3). Предположено, что на уровень инсулина может влиять наличие инсулинорезистентности у пациента. Для уточнения этой гипотезы у всех больных группы 3а был рассчитан показатель HOMA-IR (Homeostasis Model Assessment of Insulin Resistance) после ночного голодания на фоне нормогликемии, который не превышал показатели нормы 2,7 (табл. 3).
Таблица 3. Результаты обследования пациентов группы 3а на фоне гипо- и нормогликемии
|
Пациент |
Манифестная гипогликемия |
Нормогликемия |
||
|
Глюкоза, ммоль/л |
Инсулин, мкЕ/мл |
С-пептид, нг/мл |
HOMA-IR |
|
|
№1 |
2,72 |
8,99 |
2,3 |
1,833 |
|
№2 |
2,18 |
21,39 |
23,91 |
2,321 |
|
№3 |
2,13 |
16,2 |
3,15 |
1,855 |
|
№4 |
2 |
5,91 |
1,03 |
2,041 |
|
№5 |
2,61 |
6,05 |
1,33 |
1,877 |
Примечание. HOMA-IR – Homeostasis Model Assessment of Insulin Resistance.
Значительное повышение инсулина (как и С-пептида) у пациента №2 было обусловлено терминальной стадией хронической болезни почек вследствие замедленной элиминации гормонов (особенно С-пептида) [18]. В связи с этим проведен сравнительный анализ показателей С-пептида на фоне манифестной гипогликемии в группе 3а с исключением пациента №2 и объединенной группы 2+3б. Уровень С-пептида в группе 3а (1,82 [1,18; 2,73]) оказался ниже, чем в группе 2+3б (р=0,015, U-тест).
ОБСУЖДЕНИЕ
Результаты этапа 1 продемонстрировали возможность применения метода ВЭЖХ-МС/МС в детекции и идентификации субстанций ПССП в клинической практике. При валидации метода в группе пациентов с гиперинсулинемической гипогликемией в рамках этапа 2 нами, как и другими авторами [19][20][21][22], подтверждена высокая диагностическая точность ВЭЖХ-МС/МС в выявлении субстанций ПССП, в том числе при АрГ. Таким образом, метод может быть применен для диагностики преднамеренного приема данной группы лекарственных средств и дифференциальной диагностики с другими причинами гиперинсулинемического варианта НДГ. Однако с учетом относительно редкой встречаемости АрГ среди пациентов без СД (до 3,5%) [23], низкой доступности ВЭЖХ-МС/МС в России (преимущественно в специализированных центрах), рутинное выполнение исследования у всех пациентов с подозрением на НДГ, как предлагается зарубежными экспертами [10], нецелесообразно. Поэтому, по нашему мнению, детекция субстанций ПССП у пациентов с гиперинсулинемической гипогликемией рациональна только при отрицательных результатах стандартных методов визуализации инсулиномы (КТ с контрастным усилением, МРТ, УЗИ органов брюшной полости и забрюшинного пространства).
Отсутствие возможности выполнения данного исследования во всех эндокринологических стационарах определяет необходимость поиска других, более доступных маркеров АрГ. Несмотря на то, что в нашем исследовании показано, что при АрГ, в отличие других причин гиперинсулинемической гипогликемии, уровень инсулина значимо ниже (8,99 [ 6,05; 16,20]), с учетом небольшого числа пациентов с АрГ эти данные необходимо интерпретировать с осторожностью, требуется дальнейшее накопление материала и проведение исследования на большей группе больных.
Важно отметить, что более низкие показатели инсулина зафиксированы не у всех больных с АрГ. Помимо пациента №2, у которого значительное повышение показателей инсулина и С-пептида (21,39 мкЕд/мл и 23,91нг/мл соответственно) обусловлено терминальной стадией хронической болезни почек, сравнительно высокий уровень инсулина также отмечен у пациента №3 (16,2 мкЕд/мл). Наша версия о возможном влиянии инсулинорезистентности на более высокий показатель инсулина, после подсчета индекса НОМА у всех больных с АрГ, была отклонена — инсулинорезистентность не выявлена ни у одного пациента группы 3а. По нашему мнению, разный уровень инсулина, наиболее вероятно, обусловлен дозой принимаемого препарата или различной чувствительностью к ПССП. В отличие от других авторов [22], мы не проводили количественную оценку содержания субстанций ПССП в крови пациентов, так как это не являлось целью нашего исследования, но может быть полезно, например, для оптимизации тактики ведения при купировании гипогликемии.
Вместе с тем в отношении уровня С-пептида после исключения пациента №2 выявлена статистически значимая разница в группах пациентов с АрГ и другими причинами гиперинсулинемической НДГ (Me уровня С-пептида в группе пациентов с АрГ составила 1,82 [ 1,18; 2,73]). Таким образом, С-пептид в перспективе также может рассматриваться как дополнительный показатель при дифференциальной диагностике данных состояний.
Необходимо подчеркнуть, что нами проводилось определение только 7 субстанций, в отличие от других исследователей [19, 21, 22], которые анализировали наличие в сыворотке крови пациентов большего числа ПССП. Выбор ограниченного числа субстанций обусловлен их доступностью в РФ. По мере появления новых зарегистрированных ПССП следует рассмотреть вопрос об их включении в разработанную нами панель иПССП. Также перспективно исследовать другие ПССП (метформин, дапаглифлозин, вилдаглиптин, лираглутид и пр.), которые мы не включили в испытания из-за их маловыраженного влияния на возможность вызвать манифестную гипогликемию. Но не исключается, что такого эффекта можно достичь, например, при приеме чрезмерно высоких доз данных лекарственных препаратов.
ЗАКЛЮЧЕНИЕ
Метод ВЭЖХ-МС/МС обладает высокими диагностическими чувствительностью и специфичностью в обнаружении и идентификации иПССП (глибенкламид, гликвидон, гликлазид, глимепирид, глипизид, натеглинид и репаглинид) в образцах крови пациентов, получающих данные лекарственные препараты. В настоящее время, в силу малой доступности метода, данное исследование целесообразно применять у пациентов с гиперинсулинемической гипогликемией при отрицательных результатах методов визуализации инсулиномы первого ряда.
Требуется проведение дальнейших исследований на расширенной группе больных с АрГ для подтверждения полученных нами данных о возможности использования показателей инсулина и С-пептида на фоне манифестной гипогликемии в качестве дополнительных маркеров данного состояния.
Перспективным направлением дальнейших исследований также является изучение вопроса о включении в разработанную панель иПССП новых сахароснижающих препаратов по мере их регистрации и появления на российском фармацевтическом рынке, а также доступных в настоящее время лекарственных препаратов, не относящихся к группам производных сульфонилмочевины или глинидов.
ДОПОЛНИТЕЛЬНАЯ ИНФОРМАЦИЯ
Конфликт интересов. Авторы декларируют отсутствие явных и потенциальных конфликтов интересов, связанных с публикацией настоящей статьи.
Источник финансирования. Исследование выполнено при поддержке гранта Министерства науки и высшего образования Российской Федерации (соглашение №075 — 15 — 2022 — 310 от 20.04.2022).
Участие авторов: Юкина М.Ю. — разработка концепции исследования; проведение обследования участникам исследования; сбор материала; участие в проведении лабораторного обследования; получение, анализ и интерпретация результатов; написание статьи; Трошина Е.А. и Мельниченко Г.А. — согласование концепции исследования; внесение в рукопись существенной (важной) правки с целью повышения научной ценности статьи; Нуралиева Н.Ф. — участие в сборе материала; подготовка статьи к публикации; Иоутси В.А. — проведение лабораторного обследования участников исследования; Реброва О.Ю. — внесение существенной (важной) правки в анализ и интерпретацию результатов; Мокрышева Н.Г. — одобрение финальной версии рукописи.
Все авторы одобрили финальную версию статьи перед публикацией, выразили согласие нести ответственность за все аспекты работы, подразумевающую надлежащее изучение и решение вопросов, связанных с точностью или добросовестностью любой части работы.
Список литературы
1. Kinns H, Housley D, Freedman DB. Review Article Munchausen syndrome and factitious disorder: the role of the laboratory in its detection and diagnosis. Ann Clin Biochem. 2013;50:194–203. https://doi.org/10.1177/0004563212473280
2. Neal JM, Han W. Insulin Immunoassays in the Detection of Insulin Analogues in Factitious Hypoglycemia. Endocr Pract. 2008;14(8):1006-1010
3. Ameh V, Speak N. Factitious hypoglycaemia in a nondiabetic patient. European Journal of Emergency Medicine. 2008;15:59-60
4. Bauman V, Sturkey AC, Sherafat-Kazemzadeh R, et al. Factitious Hypoglycemia in Children and Adolescents with Diabetes. Pediatr Diabetes. 2019;19(4):823-831. https://doi.org/10.1111/pedi.12650
5. Guedes BV, Acosta CS, Cabrera F, et al. Factitious Hypoglycemia in Pregnancy in a Patient With Type 2 Diabetes. Obstet Gynecol. 2014;124:456-458. https://doi.org/10.1097/AOG.0000000000000138
6. Patel A, Daniels G. Hypoglycemia secondary to factitious hyperinsulinism in a foster care adolescent - a case report of munchausen syndrome in a community hospital emergency department setting. BMC Emergency Medicine. 2018;18:53. https://doi.org/10.1186/s12873-018-0208-z
7. Akbari M, Soltani A, Mohajeri-tehrani MR, et al. Factitious Hypoglycemia Caused by a Unique Pattern of Drug Use: A Case Report. Int J Endocrinol Metab. 2018;16(1):4-7. https://doi.org/10.5812/ijem.62591
8. Joshi T, Caswell A, Acharya S. Case Report A difficult case of recurrent hypoglycaemia: role of insulin assays in establishing the diagnosis. Diabet. Med. 2016:е36-е39. https://doi.org/10.1111/dme.13146
9. Giurgea I, Ulinski T, Touati G, et al. Factitious Hyperinsulinism Leading to Pancreatectomy: Severe Forms of Munchausen Syndrome by Proxy. Pediatrics. 2005;116(1). https://doi.org/10.1542/peds.2004-2331
10. Cryer PE, Axelrod L, Grossman AB, et al. Evaluation and management of adult hypoglycemic disorders: an endocrine society clinical practice guideline. J Clin Endocrinol Metab. 2009;94(3):709-728. https://doi.org/10.1210/jc.2008-1410
11. Glyburide Tablets Prescribing Information. Доступно по: https://www.drugs.com/pro/glyburide-tablets.html. Ссылка активна на 07.01.2024
12. Государственный реестр лекарственных средств. Доступно по: https://grls.rosminzdrav.ru/Grls_View_v2.aspx?routingGuid=cb385cce-5a4f-46a0-a838-500dfff16611. Ссылка активна на 07.01.2024
13. Luna B, Feinglos MN. Oral agents in the management of type 2 diabetes mellitus. Am Fam Physician. 2001;63(9):1747-56
14. Guide to Prescribing and Titrating Gliclazide Therapy. Доступно по: https://www.bucksformulary.nhs.uk/docs/avc/Link%2012a%20Guideline%20for%20Prescribing%20and%20Titrating%20Gliclazide%20Therapy.pdf. Ссылка активна на 07.01.2024
15. Correa R, Quintanilla Rodriguez BS, Nappe TM. Glipizide. StatPearls [Internet]. Treasure Island (FL): StatPearls Publishing; 2023 Jan
16. AMARYL. Доступно по: https://www.accessdata.fda.gov/drugsatfda_docs/label/2009/020496s021lbl.pdf. Ссылка активна на 07.01.2024
17. Юкина М.Ю., Нуралиева Н.Ф., Трошина Е.А., Иоутси В.А. Клинический случай артифициальной гипогликемии // Медицинский совет. 2020;(7):130–136. https://doi.org/10.21518/2079-701X-2020-7-130-136
18. Imamura Y, Yokono K, Shii K, et al. Plasma levels of proinsulin, insulin and C-peptide in chronic renal, hepatic and muscular disorders. Jpn J Med. 1984;23(1):3-8. https://doi.org/10.2169/internalmedicine1962.23.3
19. Hoizey G, Lamiable D, Trenque T, et al. Identification and quantification of 8 sulfonylureas with clinical toxicology interest by liquid chromatography-ion-trap tandem mass spectrometry and library searching. Clin Chem. 2005;51(9):1666-72. https://doi.org/10.1373/clinchem.2005.050864
20. Zhong GP, Bi HC, Zhou S, et al. Simultaneous determination of metformin and gliclazide in human plasma by liquid chromatography-tandem mass spectrometry: application to a bioequivalence study of two formulations in healthy volunteers. J Mass Spectrom. 2005;40(11):1462-71. https://doi.org/10.1002/jms.907
21. Hess C, Musshoff F, Madea B. Simultaneous identification and validated quantification of 11 oral hypoglycaemic drugs in plasma by electrospray ionisation liquid chromatography-mass spectrometry. Anal Bioanal Chem. 2011;400(1):33-41. https://doi.org/10.1007/s00216-011-4698-8
22. Yang HS, Wu AHB, Johnson-Davis KL, Lynch KL. Development and validation of an LC-MS/MS sulfonylurea assay for hypoglycemia cases in the emergency department. Clin Chim Acta. 2016;454:130-4. https://doi.org/10.1016/j.cca.2016.01.007
23. Yukina M, Nuralieva N, Zelenkova-Zakharchuk T, et al. Factitious hypoglycemia: psychosocial characteristics of patients. Endocrine Abstracts. 2023;90:EP1119. https://doi.org/10.1530/endoabs.90.EP1119
Об авторах
М. Ю. ЮкинаРоссия
Юкина Марина Юрьевна - к.м.н.; Researcher ID: P-5181-2015; Scopus Author ID: 57109367700
117036, Москва, ул. Дмитрия Ульянова, д. 11
Конфликт интересов:
Авторы декларируют отсутствие явных и потенциальных конфликтов интересов, связанных с публикацией настоящей статьи
Е. А. Трошина
Россия
Трошина Екатерина Анатольевна - д.м.н., профессор, член-корр. РАН.
Москва
Конфликт интересов:
Авторы декларируют отсутствие явных и потенциальных конфликтов интересов, связанных с публикацией настоящей статьи
Н. Ф. Нуралиева
Россия
Нуралиева Нурана Фейзуллаевна
Москва
Конфликт интересов:
Авторы декларируют отсутствие явных и потенциальных конфликтов интересов, связанных с публикацией настоящей статьи
В. А. Иоутси
Россия
Иоутси Виталий Алексеевич - к.х.н.
Москва
Конфликт интересов:
Авторы декларируют отсутствие явных и потенциальных конфликтов интересов, связанных с публикацией настоящей статьи
О. Ю. Реброва
Россия
Реброва Ольга Юрьевна - д.м.н.
Москва
Конфликт интересов:
Авторы декларируют отсутствие явных и потенциальных конфликтов интересов, связанных с публикацией настоящей статьи
Г. А. Мельниченко
Россия
Мельниченко Галина Афанасьевна - д.м.н., профессор, академик РАН.
Москва
Конфликт интересов:
Авторы декларируют отсутствие явных и потенциальных конфликтов интересов, связанных с публикацией настоящей статьи
Н. Г. Мокрышева
Россия
Мокрышева Наталья Георгиевна - д.м.н., профессор, член-корр. РАН.
Москва
Конфликт интересов:
Авторы декларируют отсутствие явных и потенциальных конфликтов интересов, связанных с публикацией настоящей статьи
Дополнительные файлы
|
|
1. Рисунок 1. Порядок выполнения исследования на этапе 1. | |
| Тема | ||
| Тип | Исследовательские инструменты | |
Посмотреть
(256KB)
|
Метаданные ▾ | |
|
|
2. Рисунок 2. Порядок выполнения исследования на этапе 2. | |
| Тема | ||
| Тип | Исследовательские инструменты | |
Посмотреть
(250KB)
|
Метаданные ▾ | |
|
|
3. Рисунок 3. Хроматограмма образца крови пациента с артифициальной гипогликемией вследствие приема глибенкламида [17]. | |
| Тема | ||
| Тип | Исследовательские инструменты | |
Посмотреть
(137KB)
|
Метаданные ▾ | |
|
|
4. Рисунок 4. Хроматограмма образца крови пациента с артифициальной гипогликемией вследствие приема гликлазида. | |
| Тема | ||
| Тип | Исследовательские инструменты | |
Посмотреть
(109KB)
|
Метаданные ▾ | |
Рецензия
Для цитирования:
Юкина М.Ю., Трошина Е.А., Нуралиева Н.Ф., Иоутси В.А., Реброва О.Ю., Мельниченко Г.А., Мокрышева Н.Г. Диагностика артифициальной гипогликемии вследствие приема пероральных сахароснижающих препаратов методом высокоэффективной жидкостной хроматографии с тандемным масс-спектрометрическим детектированием. Сахарный диабет. 2024;27(1):50-58. https://doi.org/10.14341/DM13119
For citation:
Yukina M.Y., Troshina E.A., Nuralieva N.F., Ioutsi V.A., Rebrova O.Y., Mel’nichenko G.A., Mokrysheva N.G. Diagnosis of artificial hypoglycemia due to oral hypoglycemic drugs by high-performance liquid chromatography with tandem mass spectrometric detection. Diabetes mellitus. 2024;27(1):50-58. (In Russ.) https://doi.org/10.14341/DM13119

Контент доступен под лицензией Creative Commons Attribution-NonCommercial-NoDerivatives 4.0 International License (CC BY-NC-ND 4.0).















































