Перейти к:
Классификация нейроостеоартропатии Шарко: эволюция взглядов и нерешенные проблемы
https://doi.org/10.14341/DM13118
Аннотация
Диабетическая нейроостеоартропатия Шарко — проявление синдрома диабетической стопы, сопровождающееся высоким риском образования трофических язв и ампутации. Многие аспекты этой патологии ввиду ее особенностей остаются плохо изученными, что ведет к сложностям в определении тактики лечения пациентов. В обзоре проводится анализ классификаций артропатии Шарко, построенных по анатомическому и «функциональному» принципам. Основное внимание уделено поражениям среднего отдела стопы как наиболее тяжелым по своим последствиям. Проанализированы преимущества и недостатки разных подходов к описанию рентгенологической картины заболевания на разных его стадиях. Систематизация литературы позволяет сделать вывод о том, что существующие подходы к классификации относительно приемлемы с точки зрения планирования консервативного лечения. В то же время подробные анатомо-рентгенологические классификации не помогают в выборе тактики реконструктивного хирургического лечения. В свете увеличения доступности реконструктивной хирургии при тяжелых деформациях вследствие артропатии Шарко представляется целесообразной разработка классификационных систем, которые могли бы стать инструментом определения хирургической тактики при данной патологии.
Ключевые слова
Для цитирования:
Бреговский В.Б., Оснач С.А., Оболенский В.Н., Демина А.Г., Рыбинская А.Л., Процко В.Г. Классификация нейроостеоартропатии Шарко: эволюция взглядов и нерешенные проблемы. Сахарный диабет. 2024;27(4):384-394. https://doi.org/10.14341/DM13118
For citation:
Bregovskiy V.B., Osnach S.A., Obolenskiy V.N., Demina A.G., Rybinskaya A.L., Protsko V.G. Classification of the Charcot neuroosteoarthropathy: evolution of views and unsolved problems. Diabetes mellitus. 2024;27(4):384-394. (In Russ.) https://doi.org/10.14341/DM13118
ВВЕДЕНИЕ
Несмотря на значительный и все увеличивающийся объем доступной литературы, посвященной диабетической нейроостеоартропатии Шарко (ДНОАП), большинство аспектов этой патологии остаются недостаточно известными в среде врачей терапевтических и хирургических специальностей. В этом контексте вопросы классификации ДНОАП не являются исключением.
Очевидно, что создание классификации предполагает не только описание стадийности процесса, его характерных черт, проявляющихся клинически, но и соответствующих этим стадиям результатов дополнительных исследований. Клинические критерии различных стадий ДНОАП достаточно освещены в литературе, однако, например, величина такого важного параметра, как температурный градиент, до сих является предметом дискуссии, и даже в последней версии Международного соглашения по диабетической стопе величина 2–2,2 градуса С характеризуется экспертами как условная с низкой достоверностью доказательств [1].
В этом плане, казалось бы, ключевым моментом является рентгенологическая и магнитно-резонансная визуализация ДНОАП. Тем не менее трактовка данных этих исследований также имеет ограничения, а также подвержена значительному субъективизму, особенно сильно влияющему на определение стадийности процесса. Влияние субъективных факторов возрастает еще и в том случае, если лечащий врач и специалист в области лучевой диагностики не взаимодействуют при установлении диагноза.
Валидная в клинической практике классификация также должна опираться на патогенетические особенности развития тех или иных вариантов заболевания. Возможно, что несовершенство современных классификаций ДНОАП и неудовлетворенность ими специалистов в значительной степени связаны с пробелами в представлениях о патогенезе этого осложнения сахарного диабета (СД). В предлагаемом читателю обзоре систематизируются классификации этого осложнения СД и их влияние на выбор тактики лечения.
С достаточной долей условности все классификации можно разделить на две категории. Первые опираются преимущественно на рентгенологический анализ пораженных костно-суставных структур и описывают различные локализации и сочетания деструкций и дислокаций. Вторые основаны на трактовке визуализирующих методик с точки зрения стадии деструктивно-воспалительного процесса и степени его выраженности.
Классификации диабетической нейроостеоартропатии на основе локализации поражения
Анализ литературы показывает, что существует два подхода к описанию структурных изменений: по преимущественному вовлечению тех или иных костей и по группировке пораженных структур по отделам стопы.
По-видимому, самой ранней попыткой классифицировать стопу Шарко по локализации поражения (по преимущественному вовлечению определенных костей) является работа Harris JR, Brand PW., 1966 [2]. Авторы изучали варианты поражения стопы при лепре (болезни Хансена), которые, с учетом специфики патологии, могут быть применимы и к ДНОАП. У 147 пациентов они выделили 5 вариантов поражения: 1 — деструкция пяточной кости, 2 — деструкция тела таранной кости, 3 — деструкция головки таранной кости, ладьевидной и/или медиальной клиновидной костей (поражение медиального свода), 4 — деструкция пяточно-кубовидного сустава и подвывих кубовидной кости с поражением латерального свода стопы и 5 — деструкция клиновидных костей (рис. 1). Эту систему нельзя считать полной, так как в нее не попали другие варианты, например, поражения плюснефаланговых суставов и сустава Лисфранка. Наиболее вероятно это объясняется смещенной выборкой исследования. Тем не менее для своих пациентов авторы впервые сформулировали предположение о последовательности развития деструкций при поражениях среднего отдела: разрушение таранно-ладьевидного сочленения ведет к деструкции ладьевидной кости и — вторично — к нарушению соотношения ладьевидной и 1 и 2 клиновидных костей, вызывая их диастаз, затем дислокацию и т.д. [2].
Иначе подошли к описанию последовательности артропатического процесса Sella, Barrette (1999 г.), представившие свою классификацию стадий ДНОАП с поражением среднего отдела. Они предположили, что поражение медиального свода начинается на ранних стадиях в виде рентгенологически видимого диастаза между 1 и 2 клиновидными костями и соответствующими им основаниями плюсневых костей. Дальнейшее прогрессирование патологии идет через деструкцию — подвывих и дислокацию структур среднего и наружного сводов стопы, и лишь потом развивается поражение в области таранной кости. На основании анализа небольшого числа рентгенограмм (51 стопа) пациентов с поражением медиальной колонны они предложили классифицировать артропатию в зависимости от наличия или отсутствия подвывиха определенных костных структур или их дислокации. Согласно их подходу, стадия 0 идентична рентгенонегативной стадии, 1 стадия характеризуется субхондральными кистами, эрозиями, локальной остеопенией и диастазом, появление подвывихов указывает на переход во 2 стадию, а дислокация костных структур c коллапсом медиального свода — на 3 стадию. 4 стадия отражает неактивную или хроническую фазу течения артропатии. При этом авторы не упоминают о самом характере деструкций костного аппарата стопы, придавая основное значение наличию подвывиха и дислокации [3].
Постепенное накопление опыта работы с диабетической стопой Шарко привело к очевидному выводу: сочетание поражений может быть гораздо разнообразнее. Кроме того, стало понятно, что различные типы поражений сопровождаются разными деформациями, и, хотя полный параллелизм между характером деструкций, количеством пораженных костных структур и тяжестью деформаций отсутствует, определенные поражения все же ассоциированы с неблагоприятным прогнозом для функции конечности и ее сохранности.
В этом контексте первой крупной работой стало исследование, выполненное в клинике Мейо по ретроспективному (1966–1975 гг.) анализу рентгенологической картины у 96 пациентов с ДНОАП (116 стоп) [4]. Эта статья является первым столь скрупулезным описанием клинических характеристик пациентов с ДНОАП и рентгенологических признаков стопы Шарко, а также попыткой их сопоставления. В работе показано, что во многих случаях отмечается сочетание поражений в разных областях стопы.
Так как ДНОАП является редким осложнением, то накопление знаний об особенностях ее клинического течения происходило достаточно медленно. Обобщение практического опыта привело к пониманию того, что разные варианты поражений стопы при ДНОАП не только сопровождаются различными по степени тяжести деформациями, но и различаются по прогнозу для стопы и конечности. Комплексная реализация такого подхода затруднялась в основном смещенной и нередко ограниченной выборкой, на основании анализа которой разные авторы разрабатывали свои системы. Общим для всех систем является признание того, что поражения среднего отдела стопы и голеностопного сустава представляют с клинической точки зрения наибольший интерес. Рассмотрим некоторые классификации, чаще всего упоминаемые в литературе.
Наиболее удачная и широко применяемая классификация ДНОАП по локализации поражения была предложена Sanders L. & Frikberg R. [5]. Они не только выделили основные 5 типов артропатии, но и сопоставили их с вероятностью язвообразования и прогнозом для опороспособности и сохранности стопы. Последовательность типов ДНОАП в этой классификации определялась в направлении от пальцев к пятке, и наиболее частыми вариантами были поражения переднего отдела стопы (1 тип, 15%), области сустава Лисфранка (2 тип, 40%) и ладьевидно-клиновидных суставов, таранно-ладьевидного, пяточно-кубовидного суставов (3 тип, 30%). При этом наиболее неблагоприятным прогнозом характеризовались 2 и 3 типы поражения. В более поздних работах, использовавших эту классификацию, соотношение частоты разных вариантов поражения было примерно таким же, как и у предложивших эту классификацию авторов (табл. 1).
Кроме того, аналогичные заключения делались в отношении прогноза для конечности и, что немаловажно, по вероятности реактивации (рецидива) ДНОАП. Исходя из сопоставления данных этих работ, очевиден вывод: наиболее благоприятное течение ДНОАП отмечается при 1 и 5 типах поражения, а при 2, и в большей степени 3 и 4 типах можно ожидать высокую частоту реактивации и неблагоприятного течения [6].
Очень похожая классификация была предложена Brodsky J. в 1992 г., который расположил типы согласно их встречаемости (рис. 2).
По его данным, 70% поражений составили сустав Лисфранка и ладьевидно-клиновидные суставы (тип 1). Этот вариант поражения сопровождался наибольшей частотой язвообразования, но реже требовал хирургической стабилизации. Тип 2 отмечался в 20% случаев и характеризовался поражениями, вовлекающими в разных комбинациях сустав Шопара, подтаранный, пяточно-кубовидный суставы. Тип 3 вовлекает голеностопный сустав (вариант 3а) и пяточную кость в области бугра (вариант 3в) и встречался автору редко — около 10% случаев. Второй и третий типы характеризовались автором как наиболее часто сопровождающиеся нестабильностью варианты патологии и, следовательно, требующие, с высокой вероятностью, хирургического лечения [8].
Позднее Trepman E. и соавт. добавили к классификации Brodsky комбинированные поражения (тип 4) и поражения переднего отдела, как бы «зеркально» отразив классификацию Sanders, Frikberg [9]. Схематично их классификация представлена на рис. 3.
G. Sammarco, S. Conti на основании анализа данных всего 27 пациентов описали пять вариантов деформаций среднего отдела стопы (рис. 4) [10].
По мнению этих авторов, при типе 1 изменения затрагивают сустав Лисфранка, возникает диастаз между I и II плюсневыми костями с последующей дислокацией переднего отдела стопы латерально и к тылу, при этом I плюсневая кость либо остается в прежнем положении, либо смещается несколько латеральнее относительно оси, проходящей через шейку таранной кости. Второй тип поражения характеризуется изолированной деструкцией первого плюсне-клиновидного сустава. Третий тип описывает изменения, возникающие в ладьевидно-клиновидном суставе: деструкцию промежуточной клиновидной кости и последующим распространением патологического процесса на весь сустав Лисфранка. Четвертый тип включает в себя поражение первого плюсне-клиновидного сустава с развитием диастаза не только между I и II плюсневыми костями, но и в межклиновидных суставах с распространением изменений на плюсне-кубовидный сустав. При пятом типе поражается ладьевидная кость и окружающие ее кости с последующей деструкцией клиновидных и кубовидной костей и поражением сустава Шопара.
Как следует из вышесказанного, поражения среднего отдела стопы встречаются чаще и протекают тяжелее, поэтому вполне закономерной представлялась необходимость разработки отдельной классификации для этой категории пациентов.
Первой (и пока единственной) попыткой создать всеобъемлющую классификацию ДНОАП среднего отдела, объединяющую рентгенологическую картину с характером деформаций, была работа L. Shon и соавт., опубликованная в 1998 г. [11]. Авторами были проанализированы рентгенограммы и характер деформаций 131 стопы у 109 пациентов, из которых 86 страдали СД. Авторы выделили четыре типа поражения среднего отдела стопы. Каждый из типов подразделяется на три стадии в зависимости от степени тяжести деформации продольных сводов стопы: легкой (деформация с частичным сохранением свода, стадия А), умеренной (коллапс свода, стадия В), и тяжелой (пролабирование костных структур с формированием стопы-качалки, стадия С). Кроме того, каждый из типов поражения среднего отдела делится на два варианта: первый — преимущественное поражение медиального и центрального сводов, второй — преимущественное поражение латерального свода. Таким образом, с учетом всех комбинаций, было описано 27 вариантов поражения (рис. 5).
Очевидна сложность интерпретации данных при столь комплексном подходе. Для подтверждения возможности практического применения своей системы Schon LC, Easley ME, Cohen и соавт. предприняли второе исследование, в котором удалось показать удовлетворительную воспроизводимость классификации при оценке рентгенограмм разными рентгенологами [12]. Среди недостатков этой классификации, как, впрочем, и большинства других, — отсутствие четкой связи между типом поражения и тактикой реконструктивного хирургического лечения. Кроме того, рентгенограммы, приведенные авторами в качестве иллюстрации типов поражения, в некоторых случаях не соответствуют этим типам, то есть трактовка изображений все-таки остается субъективной.
Иной подход к классификации поражения среднего отдела предложили Pinzur M. и соавт. на основании ретроспективного анализа характеристик 223 оперированных по поводу поражения среднего отдела стопы и ближайших (в течение года) результатов их оперативного лечения [13]. Не вдаваясь в детальный анализ деструкций, они выделили три варианта: вальгусную, варусную деформации и разрушение с дислокацией таранно-пяточного сочленения. С точки зрения прогноза после оперативной коррекции и стабилизации стопы эти варианты достоверно различались: при вальгусной деформации положительный результат (возможность ходить без применения тутора или аппарата, отсутствие язвы стопы и ампутации) достигнут у 87% пациентов, при поражении таранно-пяточного сустава у 70,3% пациентов, а при варусной деформации лишь в 56,3% случаев. Недостатком этого исследования является изменение оперативной тактики по мере увеличения опыта оперативного лечения, что, несомненно, повлияло на результаты и выводы работы. Кроме того, укрупнение классификационных категорий может быть не совсем корректно с точки зрения трактовки исходов оперативного лечения.
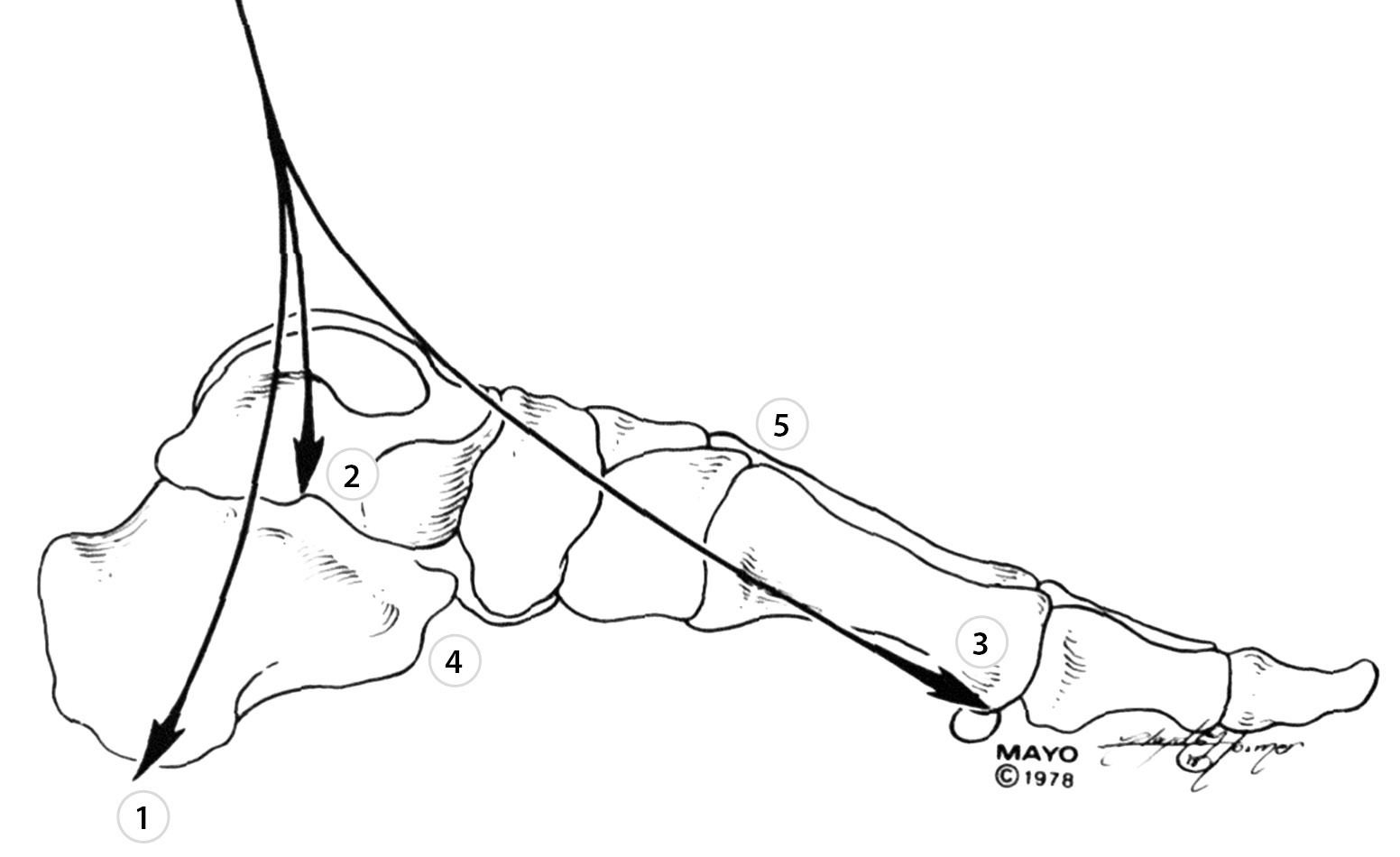
Рисунок 1. Классификация стопы Шарко у пациентов с лепрой (по Harris JR, Brand PW., 1966) [2].
Примечание. 1 — деструкция пяточной кости; 2 — деструкция тела таранной кости; 3 — деструкция головки таранной кости, ладьевидной и/или медиальной клиновидной костей (поражение медиального свода); 4 — деструкция пяточно-кубовидного сустава и подвывих кубовидной кости с поражением латерального свода стопы; 5 — деструкция клиновидных костей.
Таблица 1. Классификация Sanders L., Frikberg R. и частота различных типов поражения [5][6]
|
Тип |
Пораженные структуры |
Частота по Sanders, Frikberg, % [5] |
Частота по Gratwohl, % [6] |
|
I |
Пальцы, плюснефаланговые суставы |
15 |
14 |
|
II |
Сустав Лисфранка |
40 |
47 |
|
III |
Ладьевидно-клиновидные, таранно-ладьевидный, пяточно-кубовидный сустав |
30 |
30 |
|
IV |
Подтаранный, голеностопный суставы |
10 |
6 |
|
V |
Пятка |
5 |
3 |
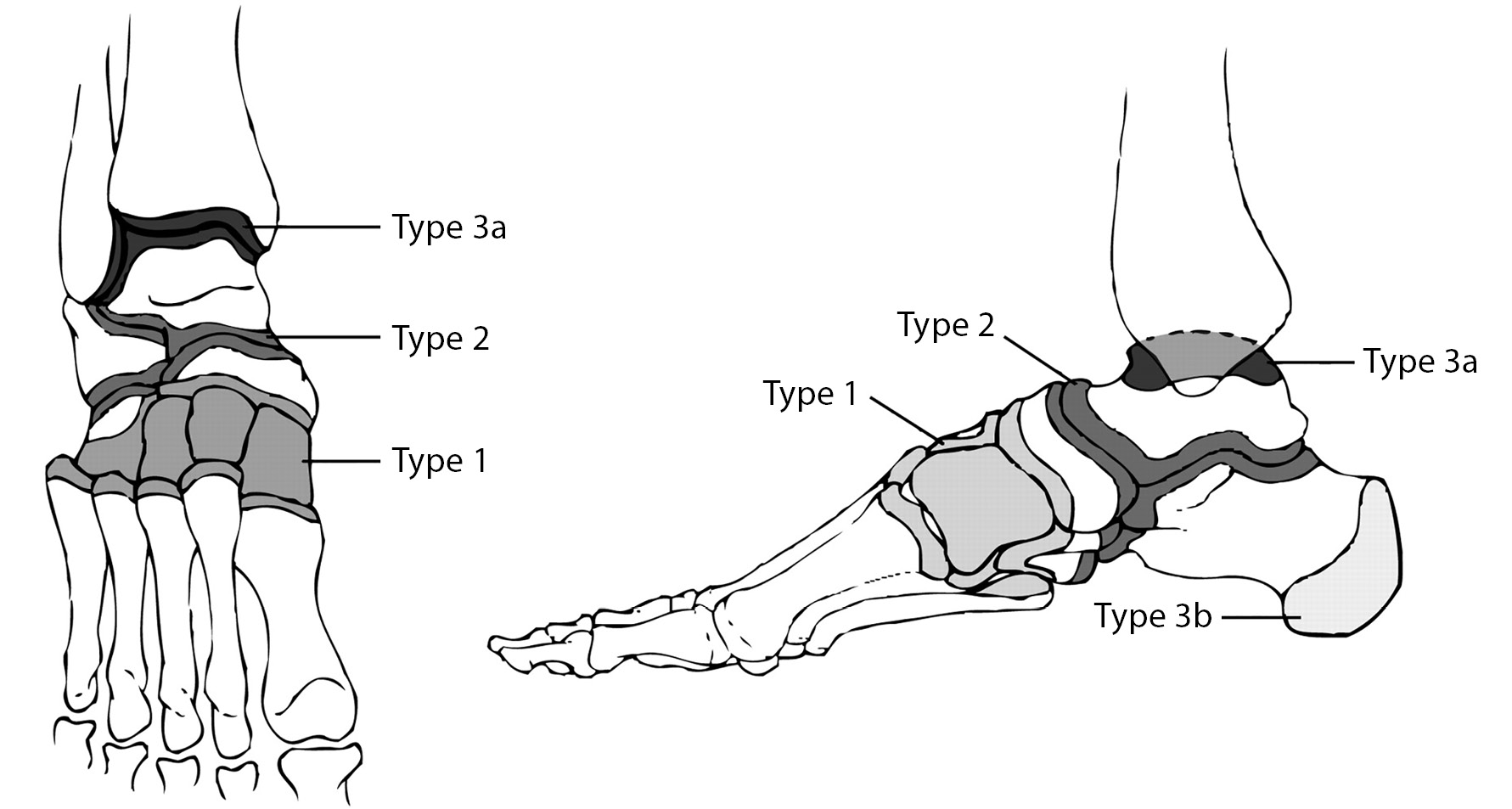
Рисунок 2. Классификация поражений среднего отдела стопы согласно Brodsky [7].

Рисунок 3. Классификация Brodsky J.W. в модификации Trepmann E. и соавт. (2005) [9].
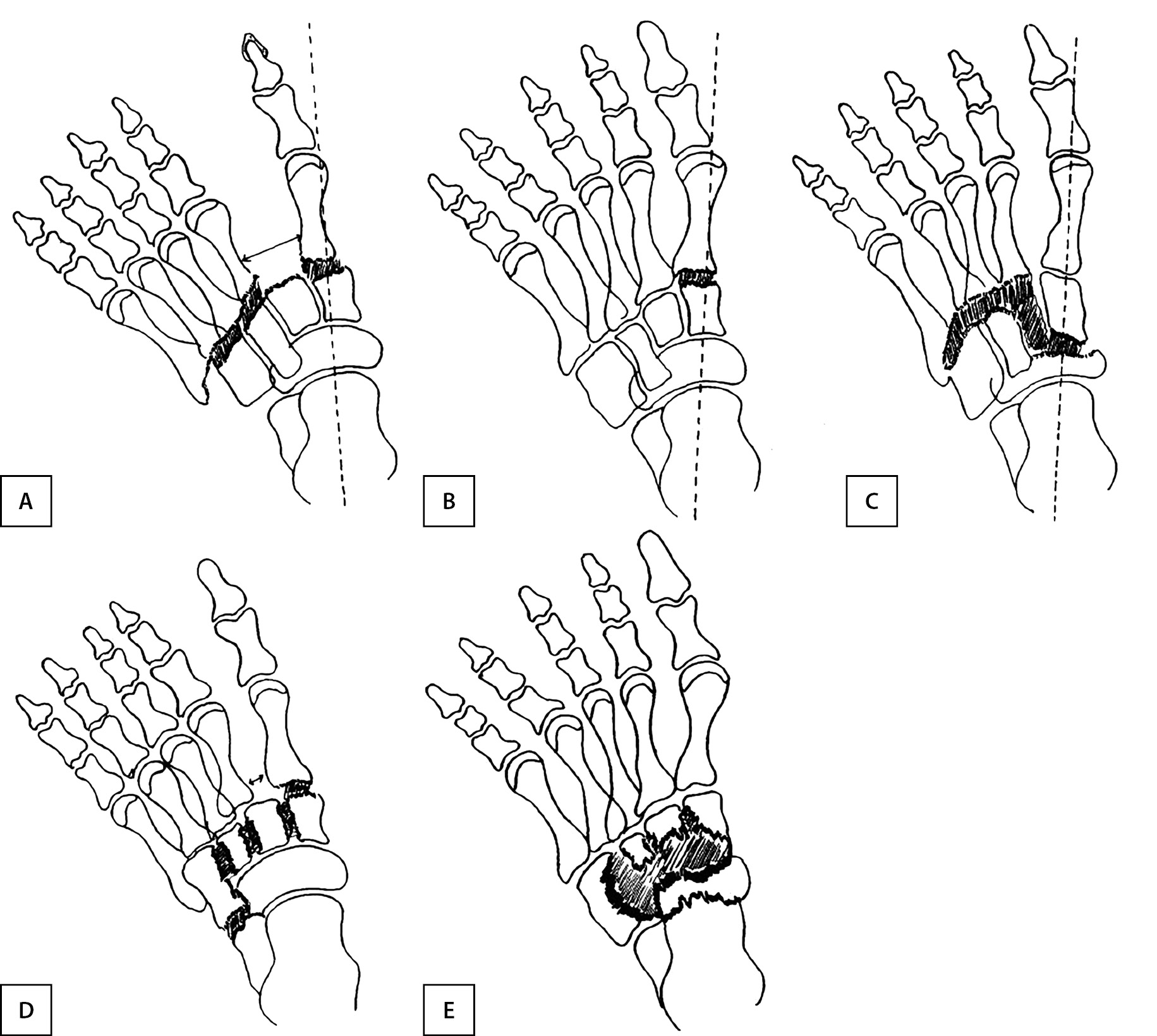
Рисунок 4. Классификация поражений среднего отдела стопы G. Sammarco, S. Conti [10].
Примечание. A, B, C, D, E в авторском тексте соответствуют 1, 2, 3, 4, 5 типам поражения.
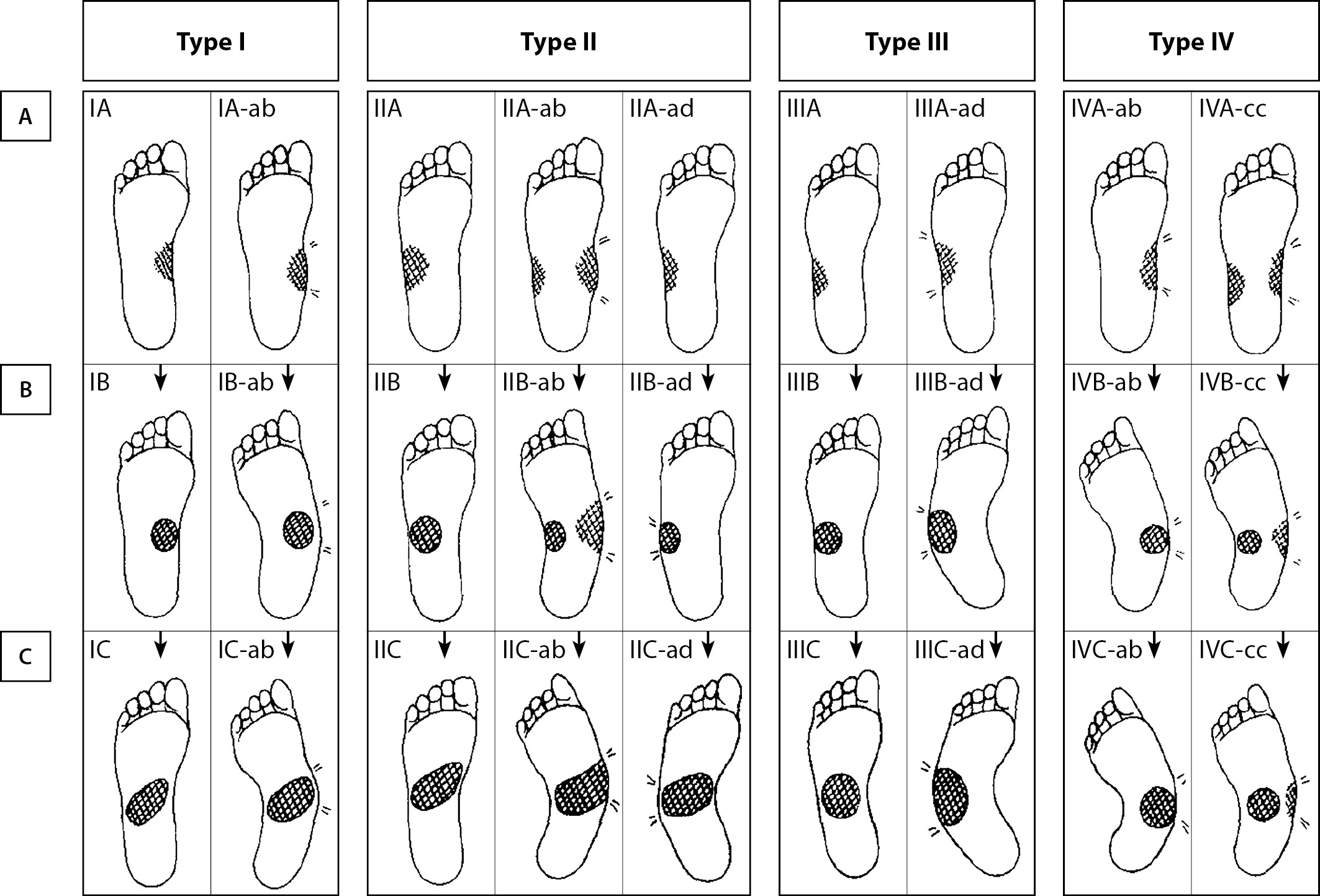
Рисунок 5. Классификация поражений среднего отдела при диабетической нейроостеоартропатии по Shon L. и соавт. [11].
Примечание. Стадия A — легкая деформация; стадия B — умеренная деформация; стадия C — тяжелая деформация.
Классификации, отражающие эволюцию костно-суставного аппарата стопы в зависимости от стадии артропатии
С точки зрения определения тактики лечения пациента с ДНОАП большое значение имеет визуализация стадии процесса и сопоставление полученных данных с клинической картиной. Вероятно, первым в этом отношении были упоминавшиеся выше Harris, Brand, предложившие определенную последовательность в развитии деструктивного процесса. Однако наиболее пригодной на практике и часто цитируемой в литературе оказалась классификация рентгенологической картины артропатии, предложенная Eichenholtz S. в 1966 г. [14]. Он проанализировал 94 сустава с артропатией Шарко, из которых только 12 были поражениями при СД, в 32 случаях был поражен коленный сустав, в 7 — тазобедренный, остальные случаи локализовались в стопе и голеностопном суставе. Eichenholtz выделил 3 стадии: рассасывание, ремоделлинг и коалесценцию — и провел параллель с клинической картиной. Характеристика этих стадий представлена в табл. 2.
Очевидно, что при анализе рентгенограмм и сопоставлении с ними внешнего вида стопы не может быть полного соответствия в каждом случае, однако в целом эта классификация настолько точно отражает суть артропатического процесса, что используется и по настоящее время не только для описания рентгенологической картины, но и для определения тактики лечения. К недостаткам этой классификации можно отнести неотчетливость границ между второй и началом третьей стадии, а также ограничение, связанное с самим методом, — возможностями рентгенографии на ранней стадии артропатии.
Появление магнитно-резонансной томографии (МРТ) позволило в значительной степени улучшить объективизацию поражения на стадии до 1 по Eichenholtz, а также создать объективные предпосылки к оптимизации консервативного лечения, и пересмотреть концепцию ведения ДНОАП. Фактически МРТ отражает не только структурные изменения, но и степень активности процесса.
Ряд авторов дополнили классификацию Eichenholtz стадией «0», то есть рентгенонегативной, но МРТ-позитивной, при которой имеется активный процесс воспаления, однако чувствительность рентгеновского исследования слишком низка для его визуализации. Одна из модификаций этой классификации приведена в табл. 3.
Серийное выполнение МРТ у пациентов с ДНОАП на разных стадиях патологии позволило обосновать новый подход в классификации ДНОАП и тактике лечения, который сводится к простому принципу «есть отек костного мозга — есть активность — нужна иммобилизация». Этот подход был детально изложен в работе Chantelau E., в которой было показано, что иммобилизация на стадии 0 позволяет в 70% случаев избежать клинически значимых деформаций, а значит, предотвращает все последующие осложнения и способствует сохранению качества жизни пациента [16]. Значение диагностики ДНОАП на рентгенонегативной стадии для клинической практики и выбора стратегии лечения в настоящее время не подлежит сомнению и приравнивается к значению диагностики рака in situ [17]. Так, Chantelau E. и Grutzner G., исходя из данных МРТ в динамике и прогноза для формы стопы в зависимости от наличия признаков активности при осмотре и при МРТ, а также учитывая рентгенографическую картину, предложили «функциональную» классификацию ДНОАП, разделяющую процесс на активный и неактивный, рентгенопозитивный и рентгенонегативный (табл. 4). В настоящее время именно этот подход зафиксирован в отечественных клинических рекомендациях [18][19].
Определение сроков завершения активной стадии ДНОАП и возможности перехода к ходьбе является одним из главных вопросов в лечении этой патологии, который до настоящего времени остается предметом дискуссий [1][20]. Необходимость стратификации отека костного мозга по степени выраженности и по распространенности диктуется практической потребностью оценки состояния пораженных костных структур в процессе лечения. Теоретически, динамическая оценка МР-картины в баллах могла бы быть одним из основных параметров, способствующих более обоснованному принятию решения о завершении активной стадии и перехода от иммобилизации к реабилитации. К сожалению, опубликованные исследования на эту тему не позволяют существенно продвинуться в искомом направлении. Так, в работе Meacock L. и соавт. была показана значительная вариабельность между оценками МР-картины разными специалистами [21]. В другом исследовании предсказательная ценность параметров МР-картины была получена только для прогнозирования длительности иммобилизации более 3 месяцев, но не всей длительности активной фазы патологии [22]. Кроме того, стоит упомянуть о неоднородности причин, вызывающих этот феномен [23]. Тем не менее данный вопрос стоит на повестке дня, и общая схема многоцентрового исследования о влиянии серийно выполняемой МРТ на сроки иммобилизации была апробирована в работе Gooday C. и соавт. (2023 г.) [24].
Следует отметить, что приведенные выше морфологические классификации основаны на анализе рентгенограмм, а это означает, что большинство пациентов оценивались авторами этих классификаций на стадии 1 по Chantelau E., Grutzner G., то есть на запущенных стадиях патологии. В большинстве случаев мы не знаем, какие структуры были поражены до первой рентгенограммы, так как проблема позднего обращения пациентов с ДНОАП и задержки постановки правильного диагноза пока не решена, поэтому динамика нарастания деструкций остается малоизученной.
Известно, что область поражения, выявляемая у одного и того же пациента при помощи рентгенограммы, может быть меньше, чем при проведении МРТ, поэтому можно считать, что все рентгенологические классификации с современных позиций весьма неточны. С другой стороны, МРТ — дорогостоящее и далеко не всегда доступное исследование, в отличие от простой рентгенографии, поэтому с точки зрения возможностей первичного звена здравоохранения рентгенограмма является приоритетным методом инструментальной диагностики ДНОАП, и, следовательно, потребность в простой классификации, основанной на анализе рентгенограмм, остается актуальной.
Многообразие сочетаний разных вариантов разрушений костно-суставных структур среднего отдела стопы с клиническими вариантами деформаций, неочевидная связь между рентгенологической картиной и видом и тяжестью итоговой деформации заставляют задуматься о причинах такого большого количества сочетаний. Объяснение этого низкой приверженностью пациента и врача к лечению, временем задержки начала лечения, несомненно, актуально. Вместе с тем, вероятно, могут иметь значение и механизмы, обусловленные индивидуальными особенностями нижних конечностей до развития ДНОАП, расположением и функцией мышц и сухожилий, которые могут играть значительную роль в направлении смещения уже разрушенных или еще не подвергшихся деструкции костных структур. В особенности это может быть важным при отсутствии полной разгрузки пораженной конечности.
Таблица 2. Классификация диабетической нейроостеоартропатии по Eichenholtz S.N. (1966 г.) [14]
|
Стадия |
Клиническая картина |
Рентгенологическая картина |
|
I. Растворение, рассасывание |
Горячая, отечная, гиперемированная стопа (2–3 мес, острая) |
Местная деминерализация, периартикулярная фрагментация, дислокация суставов |
|
II. Коалесценция (сращение) |
Стихание воспаления, отсутствие эритемы, но наличие отека и гипертермии |
Периостальная реакция, костные фрагменты в мягких тканях, участки остеонекроза, остеопролиферация, новообразованная костная ткань, признаки начинающейся консолидации деструкций |
|
III. Ремоделлинг |
Постоянная фиксированная деформация, отсутствие или минимальный отек, связанный с ходьбой, отсутствие гипертермии (6–9 мес, хроническая) |
Сглаживание краев костных фрагментов, остеосклероз, костный или фиброзный анкилоз |
Таблица 3. Модифицированная классификация диабетической нейроостеоартропатии Eichenholtz-Shibata [14][15]
|
Стадия |
Клиническая картина |
Рентгенологическая картина |
|
0. Продромальная |
Горячая, отечная, гиперемированная стопа (0–1 мес, острая) |
Отсутствие видимых переломов, увеличение внутрисуставного объема как расстояния между костями за счет отека. МРТ: отек костного мозга как проявление трабекулярного микроперелома, выпот в сустав |
|
I. Растворение, рассасывание |
Горячая, отечная, гиперемированная стопа (2–3 мес, острая) |
Местная деминерализация, периартикулярная фрагментация, дислокация суставов |
|
II. Коалесценция (сращение) |
Стихание воспаления, отсутствие эритемы, но наличие отека и гипертермии |
Периостальная реакция, костные фрагменты в мягких тканях, участки остеонекроза, остеопролиферация, новообразованная костная ткань, признаки начинающейся консолидации деструкций |
|
III. Ремоделлинг |
Постоянная фиксированная деформация, отсутствие или минимальный отек, связанный с ходьбой, отсутствие гипертермии (6–9 мес, хроническая) |
Сглаживание краев костных фрагментов, остеосклероз, костный или фиброзный анкилоз |
Таблица 4. Классификация диабетической нейроостеоартропатии, основанная на данных магнитно-резонансной томографии (по Chantelau E., Grutzner G., 2014 г.) [18]
|
Стадия/Степень тяжести |
Симптомы |
МРТ-картина |
|
Активная стадия, степень тяжести — 0 |
Легкое воспаление, отек, увеличивающийся при ходьбе (боль не всегда), выраженных деформаций нет |
Облигатные: отек костного мозга, отек мягких тканей (не всегда) Факультативные: субхондральные трабекулярные микропереломы, повреждения связок в месте прикрепления к костям |
|
Активная стадия, степень тяжести — 1 |
Тяжелое воспаление, отек, увеличивающийся при ходьбе (боль не всегда), выраженные деформации |
Облигатные: кортикальные переломы, отек костного мозга, отек мягких тканей Факультативные: остеоартрит, кисты, разрушения хрящей, повреждения связок, участки остеонекроза, остеолизиса, остеопролиферация, тендосиновит, смещение костей, дислокации суставов |
|
Неактивная стадия, степень тяжести — 0 |
Нет воспаления, отсутствие выраженных деформаций |
Отсутствие отека костного мозга, или минимальный отек, субхондральный склероз, кисты, повреждения связок |
|
Неактивная стадия, степень тяжести — 1 |
Воспаления нет, выраженные деформации, анкилоз или ложные суставы |
Резидуальный отек костного мозга, костные мозоли, облитерация и дефигурация суставов, остеофиты, остеосклероз (более отчетливо визуализируется при компьютерной томографии) |
Другие классификации
В практике отделений гнойной хирургии и ортопедии встречаются пациенты с гнойными осложнениями артропатии Шарко: флегмонами, остеомиелитами. При этом область поражения инфекционным процессом нередко совпадает с областью поражения вследствие артропатии. Поэтому идея группировать таких пациентов для выработки дифференцированной хирургической тактики выглядит вполне логичной. В этом плане интересной попыткой представляется объединение в одной системе “SEDW” области поражения (по Sanders), рентгенологической стадии (по Eichenholtz), характера деформации (Deformity: варусная, вальгусная, пресс-папье, эквинус) с глубиной поражения (по Wagner) [25][26].
В литературе неоднократно поднимался вопрос о применении тех или иных геометрических параметров стопы, получаемых при оценке рентгенограмм, для классификации по величине риска образования язвенного дефекта у пациентов с ДНОАП.
Для этого предлагается использовать различные углы и высоты костных структур, измеряемые при рентгенографии под нагрузкой, в частности, высоту кубовидной кости, угол между осями таранной кости и 1 плюсневой кости (угол Мэри), угол между линией, соединяющей подошвенную поверхность пяточного бугра и наиболее низко расположенную точку 5 плюсневой головки, и линией, соединяющей пяточный бугор с наиболее плантарно расположенной точкой переднего отростка пяточной кости (угол наклона пяточной кости) и некоторые другие параметры [10][27][28]. Однако, как заметили авторы одной из таких работ, существуют значительные трудности определения костных ориентиров на двумерных рентгенограммах для трехмерных структур, которые имеют большие деформации костей и суставов вплоть до полного их разрушения. Кроме того, практика показывает, что далеко не все пациенты в состоянии одинаково нагрузить стопу при выполнении рентгенограммы под нагрузкой. В частности, в работе Shon в 22% случаев не удалось выполнить рентгенограмму под нагрузкой в связи с выраженной деформацией или язвой подошвенной поверхности стопы [11]. Поэтому некоторые авторы высказывают сомнения в том, что на основании геометрических измерений, полученных при рентгенографии, можно получить дополнительную информацию, способную изменить представление о стратегии лечения, сложившееся на основании клинического обследования и тем более выбрать способ оперативной коррекции деформации [13][28].
ЗАКЛЮЧЕНИЕ
В заключение необходимо отметить, что все представленные классификации артропатии Шарко имеют описательный характер. Большая часть из них основана на анализе немногочисленных групп пациентов в одном учреждении, как правило, стационарном. Увеличение числа пациентов, включение данных как стационарных, так и амбулаторных учреждений может привести к выявлению большего разнообразия патологии среднего отдела. Кроме того, нам представляется, что основным методическим недостатком морфологических классификаций поражения среднего отдела стопы является обобщение сходных рентгенологичских картин на момент исследования. При этом рентгенологическая картина у конкретного больного могла быть в другой момент времени совершенно иная. Вполне вероятно, что, диагностируя по рентгенограмме определенный тип поражения, мы ошибаемся, так как до обращения характер поражения был иным. Поэтому мы предполагаем, что для создания клинической классификации, пригодной для определения тактики лечения (прежде всего хирургического), следует исходить из закономерностей формирования конкретного типа деформаций стопы, роли сил внешнего воздействия и усилий, создаваемых мышцами и сухожилиями в формировании определенных деформаций. Соединение морфологической картины (характера деструкций) и функционального состояния (активности артропатии), определяемого клинически и в основном по МРТ-картине, помогает в выборе вариантов консервативного лечения, чего нельзя сказать о тактике хирургической реконструкции. По-видимому, расширение когорты обследуемых и более скрупулезное сопоставление данных рентгенографии с клинической картиной позволит не только уточнить особенности поражения среднего отдела, но и разработать рабочую классификацию, которую можно использовать как основу для определения хирургической тактики лечения тяжелых деформаций.
Дополнительная информация
Источники финансирования. Работа выполнена по инициативе авторов без привлечения финансирования.
Конфликт интересов. Авторы декларируют отсутствие явных и потенциальных конфликтов интересов, связанных с содержанием настоящей статьи.
Участие авторов. Бреговский В.Б. — разработка концепции статьи, существенный вклад в концепцию статьи, написание статьи; Оснач С.А. — разработка концепции статьи, интерпретация результатов, написание статьи; Оболенский В.Н. — интерпретация результатов, внесение в рукопись существенной (важной) правки с целью повышения научной ценности статьи; Демина А.Г. — внесение в рукопись существенной (важной) правки с целью повышения научной ценности статьи; Рыбинская А.Л.— интерпретация результатов, внесение в рукопись существенной (важной) правки с целью повышения научной ценности статьи; Процко В.Г. — интерпретация результатов, внесение в рукопись существенной (важной) правки с целью повышения научной ценности статьи.
Все авторы одобрили финальную версию статьи перед публикацией, выразили согласие нести ответственность за все аспекты работы, подразумевающую надлежащее изучение и решение вопросов, связанных с точностью или добросовестностью любой части работы.
Список литературы
1. Guidelines of International Working Group on Diabetic Foot: Charcot’s neuro-osteo-arthropathy (2023 update). Available from: https://iwgdfguidelines.org/charcot-2023
2. Harris JR, Brand PW. PATTERNS OF DISINTEGRATION OF THE TARSUS IN THE ANAESTHETIC FOOT. J Bone Joint Surg Br. 1966;48-B(1):4-16. doi: https://doi.org/10.1302/0301-620X.48B1.4
3. Sella EJ, Barrette C. Staging of Charcot neuroarthropathy along the medial column of the foot in the diabetic patient. J Foot Ankle Surg. 1999;38:34-40. doi: https://doi.org/10.1016/s1067-2516(99)80086-6
4. Cofield RH, Morrison MJ, Beabout JW. Diabetic neuroarthropathy in the foot: patient characteristics and patterns of radiographic change. Foot Ankle. 1983;4:15-22. doi: https://doi.org/10.1177/107110078300400104
5. Sanders LJ, Frykberg RG. Diabetic neuropathic osteoarthropathy: The Charcot foot. In: Frykberg RG editor. The high risk foot in diabetes mellitus. New York: Churchill Livingstone. 1991:297−338
6. Gratwohl V, Jentzsch T, Schöni M, et al. Long-term follow-up of conservative treatment of Charcot feet. Arch Orthop Trauma Surg. 2022;142:2553-2566. doi: https://doi.org/10.1007/s00402-021-03881-5
7. Brodsky JW. The diabetic foot. In Mann R.A., Coughlin M. (ed): Surgery of the Foot and Ankle. St. Louis, C.V . Mosby. 1992
8. Brodsky JW, Rouse AM. Exostectomy for Symptomatic Bony Prominences in Diabetic Charcot Feet. Clin Orthop Relat Res. 1993;296:21-26. doi: https://doi.org/10.1097/00003086-199311000-00005
9. Trepman E, Nihal A, Pinzur MS. Current topics review: Charcot neuroarthropathy of the foot and ankle. Foot Ankle Int. 2005;26:46-63. doi: https://doi.org/10.1177/107110070502600109
10. Sammarco G, Conti S. Surgical treatment of neuroarthropathic foot deformity. Foot Ankle Int. 1998;19:102-109. doi: https://doi.org/10.1177/107110079801900209
11. Schon LC, Weinfeld SB, Horton GA, Resch S. Radiographic and clinical classification of acquired midtarsus deformities. Foot Ankle Int. 1998;19:394-404. doi: https://doi.org/10.1177/107110079801900610
12. Schon LC, Easley ME, Cohen I, et al. The acquired midtarsus deformity classification system-interobserver reliability and intraobserver reproducibility. Foot Ankle Int. 2002;23:30-36. doi: https://doi.org/10.1177/107110070202300106
13. Pinzur MS, Schiff AP. Deformity and clinical outcomes following operative correction of Charcot foot: A new classification with implications for treatment. Foot Ankle Int. 2018;39:265-270. doi: https://doi.org/10.1177/1071100717742371
14. Eichenholtz SN. Charcot joints. With a foreword by P.D. Wilson. Springfield (Ill): Charles C. Thomas. 1966.
15. Shibata T, Tada K, Hashizume C. The results of arthrodesis of the ankle for leprotic neuroarthropathy. J Bone Jt Surg. 1990;72(5):749-756. doi: https://doi.org/10.2106/00004623-199072050-00016
16. Chantelau E, Richter A. The acute diabetic Charcot foot managed on the basis of magnetic resonance imaging – a review of 71 cases. Swiss Med Wkly. 2013;143:w13831. Available at: https://smw.ch/article/doi/smw.2013.13831
17. Frykberg RG, Zgonis T, Armstrong DG, et al. American College of Foot and Ankle Surgeons. Diabetic foot disorders. A clinical practice guideline (2006 revision). J Foot Ankle Surg. 2006;45(5Suppl):S1-66. doi: https://doi.org/10.1016/S1067-2516(07)60001-5
18. Chantelau EA, Grutzner G. Is the Eichenholtz classification still valid for the diabetic Charcot foot? Swiss Med Wkly. 2014;144:1-6. doi: https://doi.org/10.4414/smw.2014.13948
19. Сахарный диабет 2 типа у взрослых. Клинические рекомендации. Доступно по: https://cr.minzdrav.gov.ru/schema/290_2. Ссылка активна на 30.11.23
20. Демина А.Г., Бреговский В.Б., Карпова И.А. Критерии продолжительности иммобилизации пораженной конечности при диабетической нейроостеоартропатии Шарко // Сахарный диабет. — 2014. — №4. — С. 60-65. doi: https://doi.org/10.14341/DM2014460-65
21. Meacock L, Petrova NL, Donaldson A, et al. Novel semiquantitative bone marrow oedema score and fracture score for the magnetic resonance imaging assessment of the active Charcot foot in diabetes. Journal of Diabetes Research. 2017;8504137. doi: https://doi.org/10.1155/2017/8504137
22. Berli MC, Higashigaito K, Götschi T, et al. The «Balgrist Score» for evaluation of Charcot foot: a predictive value for duration of off-loading treatment. Skeletal Radiol. 2021;50:311-320. doi: https://doi.org/10.1007/s00256-020-03541-6
23. Chantelau EA, Antoniou S, Zweck B, Haage P. Follow up of MRI bone marrow edema in the treated diabetic Charcot foot — a review of patient charts. Diabet Foot Ankle. 2018;9:1466611. doi: https://doi.org/10.1080/2000625X.2018.1466611
24. Gooday C, Game F, Woodburn J, Poland F et al. A randomised feasibility study of serial magnetic resonance imaging to reduce treatment times in Charcot neuroarthropathy in people with diabetes (CADOM). J Foot Ankle Res. 2023;26:16(1):2. doi: https://doi.org/10.1186/s13047-023-00601-7
25. Оболенский В.Н., Процко В.Г., Комелягина Е.Ю. К вопросу о классификации синдрома диабетической стопы // Хирург. — 2016. — № 10. — С. 37-47.
26. Оснач С.А., Оболенский В.Н., Процко В.Г., и соавт. Метод двухэтапного лечения пациентов с тотальными и субтотальными дефектами стопы при нейроостеоартропатии Шарко // Гений ортопедии. — 2022. — Т. 28. — №4. — С. 523-531. doi: https://doi.org/1028-4427-2022-28-4-523-531
27. López-Moral M, Molines-Barroso RJ, Sanz-Corbalán I, et al. Predictive Radiographic Values for Foot Ulceration in Persons with Charcot Foot Divided by Lateral or Medial Midfoot Deformity. J Clin Med. 2022;18;11(3):474. doi: https://doi.org/10.3390/jcm11030474
28. Hastings MK, Sinacore DR, Mercer-Bolton N. Precision of foot alignment measures in Charcot arthropathy. Foot Ankle Int. 2011;32(9):867-872. doi: https://doi.org/10.3113/FAI.2011.0867
Об авторах
В. Б. БреговскийРоссия
Бреговский Вадим Борисович - д.м.н.
194354, СПб ул. Сикейроса, д. 10Д; тел.: 8(921)301-14-15
Конфликт интересов:
конфликт интересов отсутствует
С. А. Оснач
Россия
Оснач Станислав Александрович
Москва
Конфликт интересов:
конфликт интересов отсутствует
В. Н. Оболенский
Россия
Оболенский Владимир Николаевич - к.м.н.
Москва
Конфликт интересов:
конфликт интересов отсутствует
А. Г. Демина
Россия
Демина Анастасия Геннадьевна - к.м.н. врач кабинета "Диабетическая стопа"
Конфликт интересов:
конфликт интересов отсутствует
А. Л. Рыбинская
Россия
Рыбинская Анастасия Леонидовна - врач травматолог-ортопед.
Москва
Конфликт интересов:
конфликт интересов отсутствует
В. Г. Процко
Россия
Процко Виктор Геннадьевич - д.м.н. Доцент кафедры травматологии и ортопедии РУДН.
Москва
Конфликт интересов:
конфликт интересов отсутствует
Дополнительные файлы
|
|
1. Рисунок 1. Классификация стопы Шарко у пациентов с лепрой (по Harris JR, Brand PW., 1966) [2]. | |
| Тема | ||
| Тип | Материалы исследования | |
Посмотреть
(173KB)
|
Метаданные ▾ | |
|
|
2. Рисунок 3. Классификация Brodsky J.W. в модификации Trepmann E. и соавт. (2005) [9]. | |
| Тема | ||
| Тип | Материалы исследования | |
Посмотреть
(53KB)
|
Метаданные ▾ | |
|
|
3. Рисунок 2. Классификация поражений среднего отдела стопы согласно Brodsky [7]. | |
| Тема | ||
| Тип | Исследовательские инструменты | |
Посмотреть
(137KB)
|
Метаданные ▾ | |
|
|
4. Рисунок 4. Классификация поражений среднего отдела стопы G. Sammarco, S. Conti [10]. | |
| Тема | ||
| Тип | Исследовательские инструменты | |
Посмотреть
(234KB)
|
Метаданные ▾ | |
|
|
5. Рисунок 5. Классификация поражений среднего отдела при диабетической нейроостеоартропатии по Shon L. и соавт. [11]. | |
| Тема | ||
| Тип | Материалы исследования | |
Посмотреть
(380KB)
|
Метаданные ▾ | |
Рецензия
Для цитирования:
Бреговский В.Б., Оснач С.А., Оболенский В.Н., Демина А.Г., Рыбинская А.Л., Процко В.Г. Классификация нейроостеоартропатии Шарко: эволюция взглядов и нерешенные проблемы. Сахарный диабет. 2024;27(4):384-394. https://doi.org/10.14341/DM13118
For citation:
Bregovskiy V.B., Osnach S.A., Obolenskiy V.N., Demina A.G., Rybinskaya A.L., Protsko V.G. Classification of the Charcot neuroosteoarthropathy: evolution of views and unsolved problems. Diabetes mellitus. 2024;27(4):384-394. (In Russ.) https://doi.org/10.14341/DM13118

Контент доступен под лицензией Creative Commons Attribution-NonCommercial-NoDerivatives 4.0 International License (CC BY-NC-ND 4.0).















































